Clear Sky Science · nl
Multi-omicsprofilering onthult kenmerken van het tumormilieu gekoppeld aan respons op immunotherapie en prognose bij niet-kleincellige longkanker
Waarom deze studie belangrijk is voor mensen met longkanker
Veel mensen met gevorderde longkanker krijgen nu immunotherapie die het immuunsysteem helpt tumoren aan te vallen. Toch profiteert een groot aantal patiënten niet of keert hun kanker terug. Deze studie stelt een eenvoudige maar cruciale vraag: wat verschilt er binnen tumoren die op de behandeling reageren vergeleken met tumoren die dat niet doen, en kan die kennis leiden tot betere zorg voor patiënten met niet-kleincellige longkanker?
In tumoren kijken, cel voor cel
De onderzoekers combineerden meerdere krachtige genetische technieken om een gedetailleerde kaart te maken van longtumoren van patiënten die immunotherapie kregen, vaak in combinatie met chemotherapie. In plaats van signalen over de hele tumor te middelen, analyseerden ze individuele cellen en identificeerden ze immuuncellen, kankercellen en ondersteunende cellen. Door tumoren die sterk krompen na behandeling te vergelijken met tumoren die dat niet deden, vonden ze dat succesvolle responsen sterk samenhingen met de aanwezigheid van een specifieke groep cytotoxische T-cellen en met hoe vriendelijk of vijandig het omliggende tumormilieu was voor immuunaanvallen.
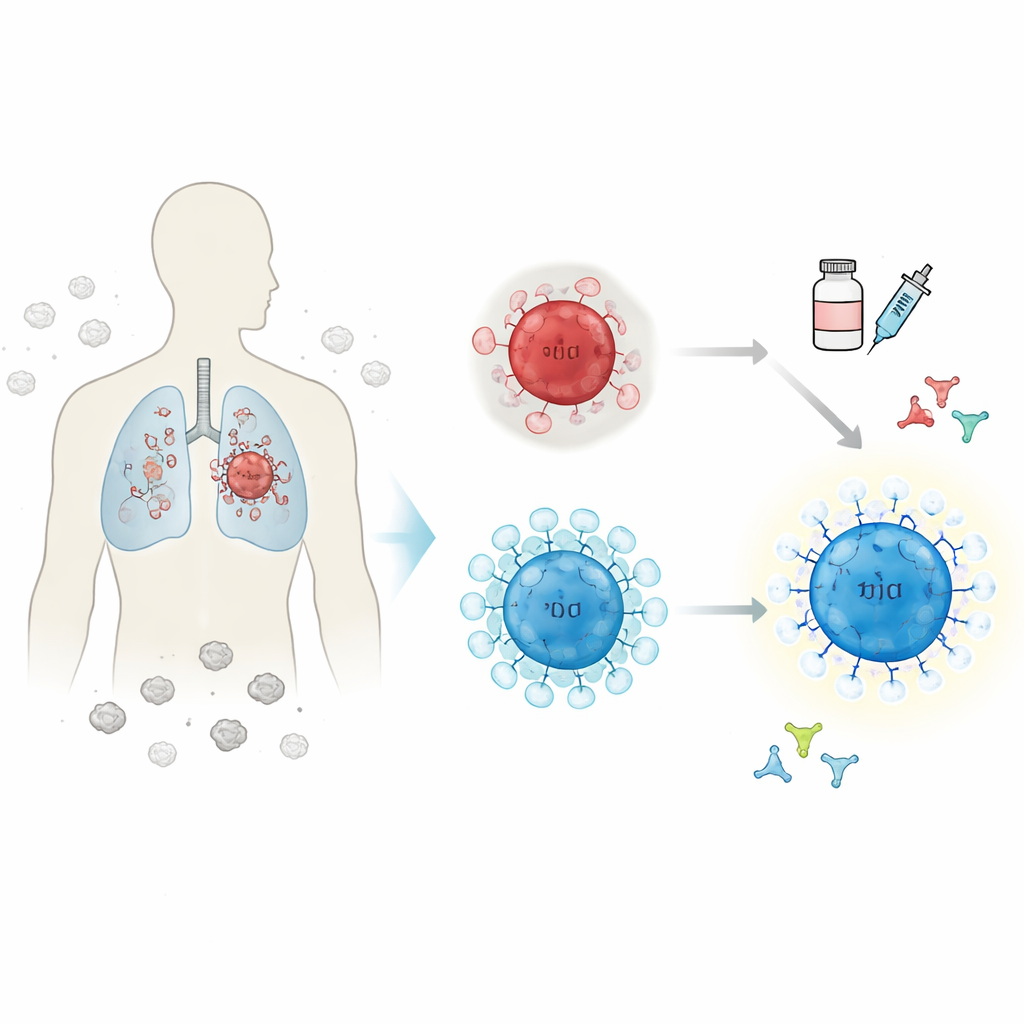
Een speciale groep cytotoxische T-cellen gekoppeld aan betere uitkomsten
Onder alle onderzochte immuuncellen stak één subset van CD8 T-cellen eruit. Deze cellen werden gekenmerkt door hoge expressie van een gen genaamd ZNF683. Tumoren van patiënten die goed op immunotherapie reageerden waren rijk aan deze ZNF683-positieve CD8 T-cellen, terwijl niet-responderende tumoren er veel minder van hadden. Het team toonde, over verschillende kankertypen en grote patiëntencollecties heen, aan dat hogere ZNF683-waarden meestal samengingen met meer immuuneenheden en betere overleving. Ze bouwden vervolgens een risicoscore, gebaseerd op 19 genen gerelateerd aan deze T-celgroep, waarmee patiënten met longadenocarcinoom konden worden ingedeeld in lagere-risico, immuun-"hete" tumoren en hogere-risico, immuun-"koude" tumoren.
Koude tumoren, een onderdrukkend signaal en een nieuw doelwit
Hoge-risico tumoren, zoals gedefinieerd door deze ZNFRS-score, hadden minder behulpzame immuuncellen en meer kankercellen en myeloïde cellen—een patroon dat typisch is voor "koude" tumoren die immunotherapie weerstaan. Toen de onderzoekers onderzochten hoe cellen in deze tumoren met elkaar communiceerden, ontdekten ze dat veel signalen van myeloïde en kankercellen naar T-cellen en natural killer-cellen stroomden. Een belangrijke speler was SPP1, een afgescheiden eiwit dat van myeloïde of kankercellen naar receptoren op immuuncellen reist. Dit SPP1-signaalnetwerk was sterk in niet-responderende en hoge-risico tumoren, maar zwak of afwezig in responderende en lage-risico tumoren, wat suggereert dat SPP1 helpt een immuunsuppressieve niche te creëren die cytotoxische T-cellen wegdrijft of hun activiteit dempt.
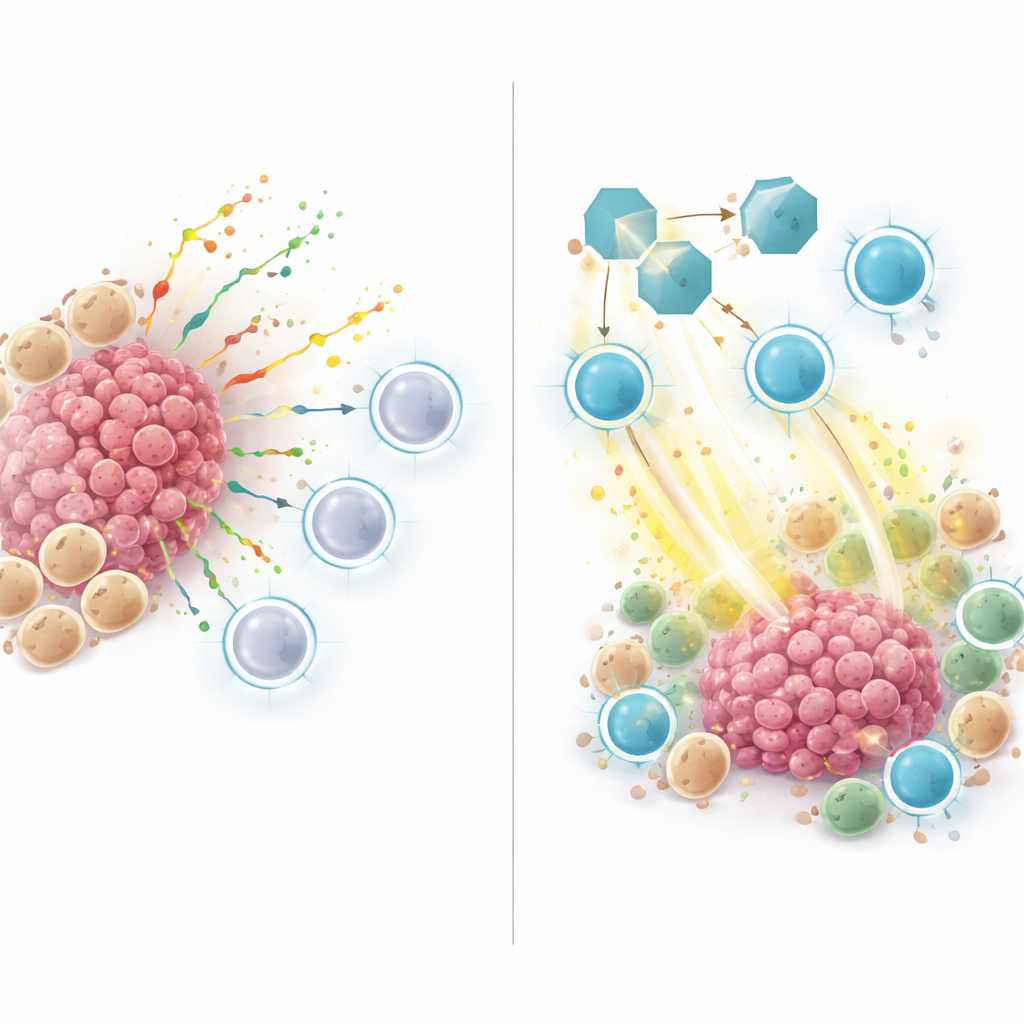
Testen van SPP1-blokkade in diermodellen
Om verder te gaan dan patronen in humane gegevens, schakelde het team over op muismodellen van longkanker. Ze behandelden muizen met tumoren met een antilichaam dat SPP1 blokkeerde, met of zonder een anti-PD-1-immunotherapiedrug. Het blokkeren van SPP1 alleen vertraagde de tumorgroei, en de combinatie met anti-PD-1 werkte het beste. Onder de microscoop en via eencellige analyse bevatten tumoren van muizen met geblokkeerd SPP1 meer actieve CD8 T-cellen die toxische moleculen produceerden die kankercellen doden, en minder zogenoemde M2-achtige macrofagen die gewoonlijk tumorgroei bevorderen. Met andere woorden, het remmen van SPP1 verschuift het microklimaat van een onderdrukkende staat naar een immuun-geactiveerde staat.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialistische lezers is de hoofdboodschap dat niet alle immuuncellen in een tumor gelijk zijn, en dat de omgeving ze kan verwelkomen of afstoten. Deze studie identificeert een speciaal type cytotoxische T-cel gekoppeld aan succesvolle immunotherapie bij longkanker en ontwikkelt een gengebaseerde score die weergeeft hoe warm of koud het immuunklimaat van de tumor is. Daarnaast belicht ze SPP1 als een belangrijk schadelijk signaal dat tumoren helpt zich te verbergen voor het immuunsysteem. Door SPP1 in muizen te blokkeren, konden onderzoekers cytotoxische T-cellen activeren en standaardimmunotherapie effectiever maken. Hoewel meer klinische toetsing nodig is, schetsen deze bevindingen een route naar bloed- en weefseltests die identificeren wie het meest waarschijnlijk baat heeft bij immunotherapie en suggereren ze combinatiebehandelingen die resistente longtumoren omzetbaar kunnen maken in tumoren die het immuunsysteem beter kan aanvallen.
Bronvermelding: Zhang, L., Zeng, J., Wen, J. et al. Multi-omics profiling reveals tumor microenvironment characteristics linked to immunotherapy response and prognosis in non-small cell lung cancer. npj Precis. Onc. 10, 179 (2026). https://doi.org/10.1038/s41698-026-01474-2
Trefwoorden: niet-kleincellige longkanker, immunotherapie, tumormicro‑omgeving, CD8 T-cellen, SPP1-signaleringsroute