Clear Sky Science · tr
Graf sinir ağı modellemesiyle uzamsal tümör-bağışıklık etkileşimleri, küçük hücresel nişlerin prognostik değerini tanımlıyor: küçük hücre dışı akciğer kanserinde
Tümör çevresindeki mahalle neden önemli
Akciğer kanseri genler ve ilaçlar bağlamında sıkça anlatılır, ancak bu çalışma tümör içindeki hücrelerin birbirine komşu olduğu yerin, o hücrelerin ne olduğuyla aynı derecede önemli olabileceğini gösteriyor. Küçük hücre dışı akciğer kanserli hastalardan alınan milyonlarca bireysel hücreye yakın çekim yaparak, araştırmacılar tümör ve bağışıklık hücrelerinin “sosyal ağını” okumak için bir yapay zeka yaklaşımı kullandılar. Belirli yerel hücre mahallelerinin hastaların yaşam süresiyle güçlü şekilde ilişkili olduğunu buldular; bu da daha doğru tahminlere ve potansiyel olarak daha akıllı immünoterapi seçimlerine giden bir yol sunuyor.
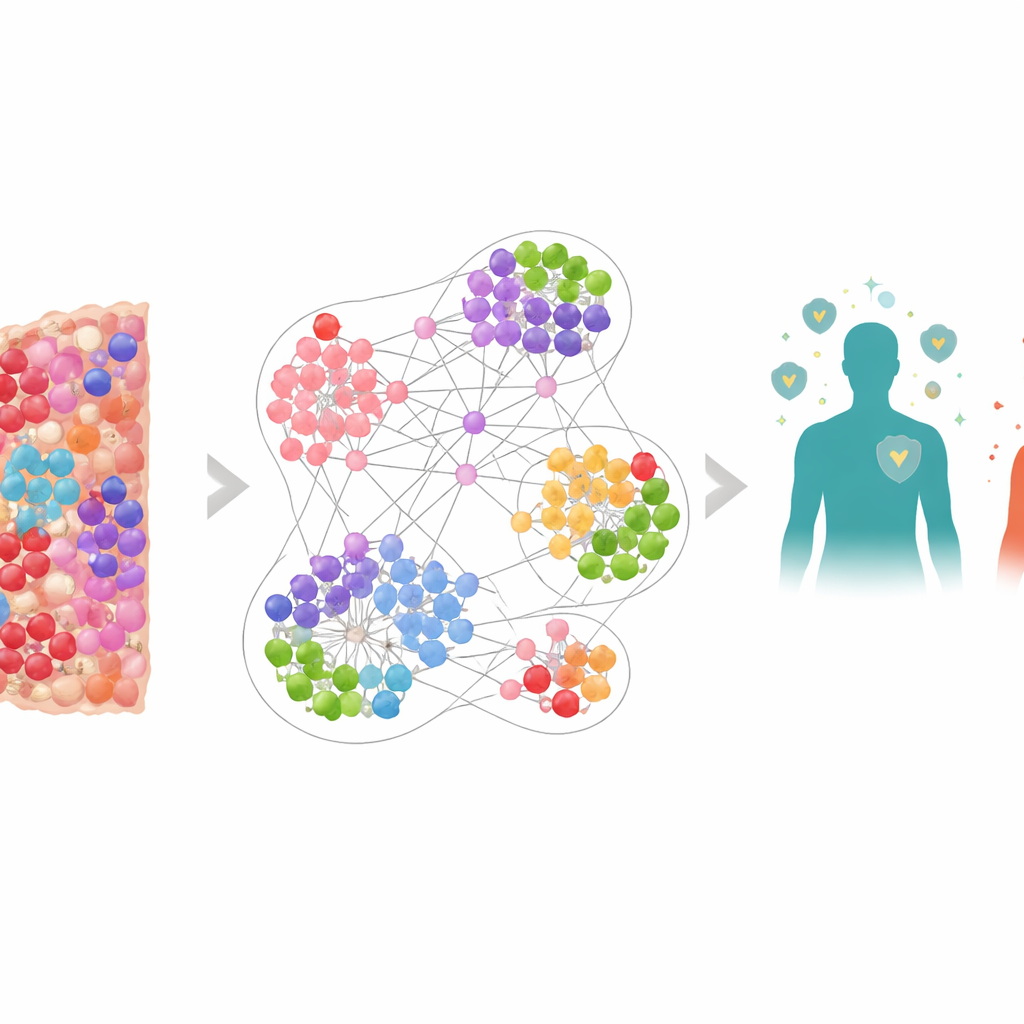
Kanseri yaşayan bir şehir olarak görmek
Tümörü tek tip bir kütle olarak ele almak yerine ekip, onu birçok farklı sakindeki kalabalık bir şehir olarak gördü: kanser hücreleri, savunucu bağışıklık hücreleri ve bağışıklık saldırısını baskılayan hücreler. Birden çok belirteci aynı anda boyayan özel bir görüntüleme yöntemiyle, 506 akciğer kanseri hastasının biyopsi örneklerinden 6,9 milyondan fazla hücre haritalandı. Her hücrenin konumu ve kimliği kaydedildi; bunlar arasında katil T hücreleri (CD8+), PD-1 ve PD-L1 gibi bağışıklık “frenleri” ve FOXP3 ile işaretlenen düzenleyici T hücreleri gibi kilit oyuncular vardı. Bu, tümör mikroçevresinin — tümörlerin ve bağışıklık hücrelerinin sürekli etkileşimde bulunduğu hemen çevrenin — çok ayrıntılı haritalarının oluşturulmasına yol açtı.
Hücre haritalarını ağ modeline dönüştürmek
Böylesi bir karmaşıklığı anlamlandırmak için araştırmacılar ağlar üzerinde çalışmak üzere tasarlanmış bir yapay zeka türü olan graf sinir ağı kurdular. Modellerinde her hücre bir düğümdü ve komşu hücreler bağlantılarla birbirine bağlanarak her hücrenin etrafında çok sayıda örtüşen “mahalle grafiği” oluşturuyordu. Ağ, hangi tür yerel mahallelerin daha uzun veya daha kısa yaşayan hastalarda eğilimli olduğunu öğrenmesi için eğitildi. Modelin mahalle düzeyindeki tahminleri hasta düzeyinde ortalandığında, yaşam süresini çok doğru biçimde tahmin etti; genel olarak kaç katil T hücresi olduğuna dair daha basit ölçütleri veya yalnızca hücrelerin nerede olduğunu bilip ne ifade ettiklerini bilmeyen modelleri geride bıraktı.
Tümör içindeki iyi ve kötü mahalleler
Yapay zekânın öğrendiklerini çözümlerken ekip, hayatta kalma açısından çok farklı sonuçları olan belirgin yerel mahalle türlerini tanımladı. Özellikle tümör hücreleri de bağışıklık aktivasyon belirteçleri gösterdiğinde katil T hücreleri bakımından zengin mahalleler genelde daha iyi sonuçlarla ilişkilendirildi. Ancak kalabalık bağışıklık alanlarının hepsi faydalı değildi. Bazı mahalleler çok sayıda katil T hücresi ile tümör veya yakınındaki bağışıklık hücrelerinde yüksek PD-L1 düzeylerini karıştırarak güçlü bir bağışıklık “kapatması” ve daha kötü sağkalım sinyali veriyordu. Diğer mahalleler ise bağışıklık çöllerine benziyordu; az sayıda savunucu hücre ile baskın olan tümör hücreleri ve bunlar da kötü sonuçlarla ilişkiliydi. Bu desenleri kümeleyerek çalışma, bağışıklık saldırısı ile bağışıklık kaçışı arasında denge kuran birkaç tekrarlayan tümör “durumunu” tanımladı.
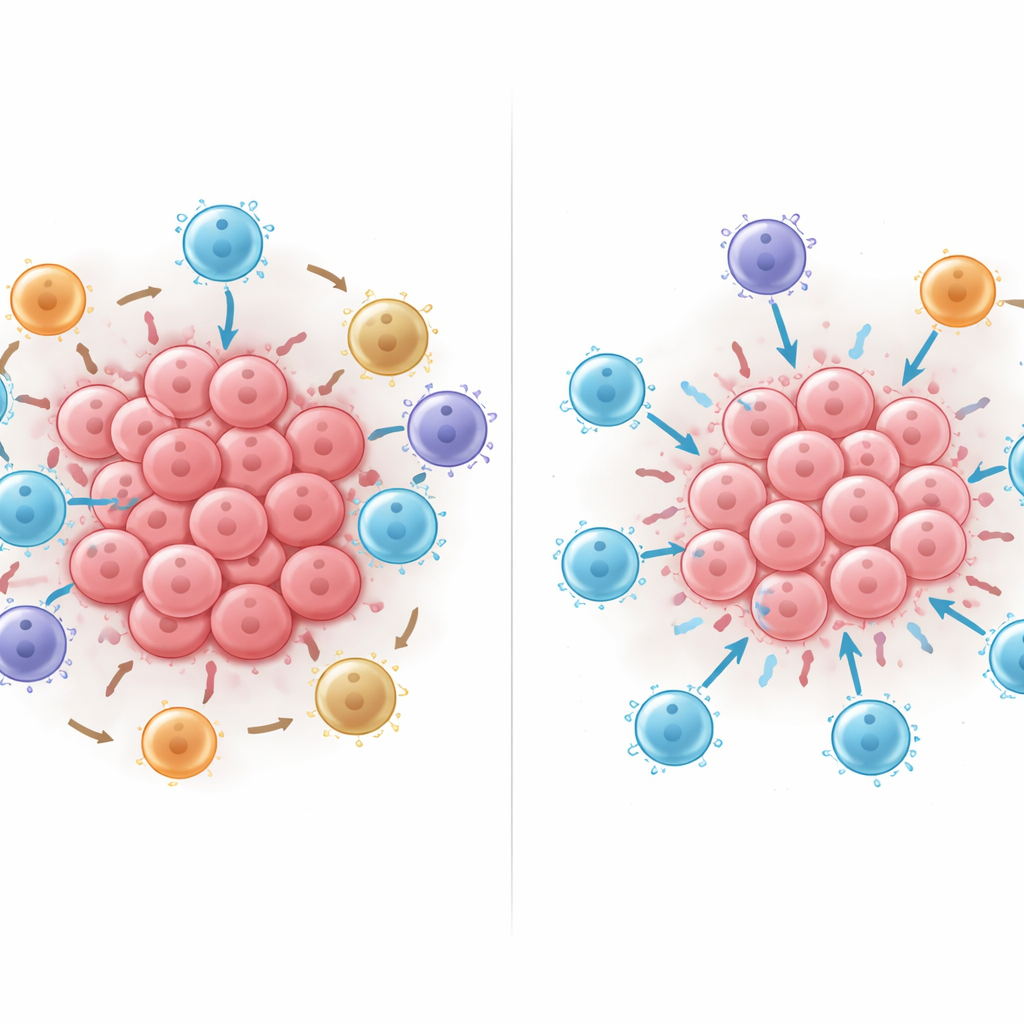
Hücreleri yeniden düzenlediğinizde ne olur
Araştırmacılar daha sonra eğitilmiş yapay zekâ modelini sanal bir laboratuvar gibi kullanarak mahallelere dijital olarak hücre ekleyip, çıkarıp veya taşıyarak öngörülen sağkalımın nasıl değiştiğini gözlemlediler. Katil T hücreleri eklemek neredeyse her zaman yardımcı oldu, ancak bu hücreler tümör hücreleriyle doğrudan temas halindeyse etkisi en yüksekti; uzakta tutulduklarında daha az etkiliydiler. Baskılayıcı PD-L1–pozitif bağışıklık hücrelerini veya FOXP3-pozitif düzenleyici T hücrelerini katil T hücreleriyle yakın temasa taşımak modelin sağkalım tahminini tutarlı biçimde azalttı ve bu tür temaslar arttıkça zarar büyüdü. Bu sayısal deneyler fiziksel temas desenlerinin — kim kime dokunuyor — etkili tümör saldırısı ile bağışıklık baskısı arasındaki dengeyi keskin şekilde eğebileceğini öne sürüyor.
Geleceğin kanser bakımını nasıl şekillendirebilir
Halk için temel mesaj, “çok sayıda bağışıklık hücresi” olan tümörlerin hepsinin eşit olmadığıdır. Bu çalışma, genellikle sadece birkaç düzine hücreden oluşan küçük mahallelerin yerel savaşı bağışıklığın kazanıp kazanmadığına dair güçlü sinyaller taşıyabildiğini ve bu sinyallerin tümör evresi veya immünoterapi alıp almadığı hesaba katıldıktan sonra bile hastaların akıbetini öngördüğünü gösteriyor. Bu uzamsal desenleri gelişmiş yapay zekâyla okumak için bir taslak sunarak, çalışma hücre saymaktan öteye geçip hücrelerin nasıl düzenlendiğini ölçen yeni nesil testlere işaret ediyor. Böyle uzamsal biyobelirteçler, hangi hastaların immün tabanlı tedavilerden yararlanma olasılığının daha yüksek olduğunu ve hangilerinin zararlı hücre mahallelerini bozmayı veya yararlı olanları güçlendirmeyi gerektiren kombinasyon stratejilerine ihtiyaç duyabileceğini daha iyi belirlemede hekimlere yardımcı olabilir.
Atıf: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Anahtar kelimeler: küçük hücre dışı akciğer kanseri, tümör mikroçevresi, graf sinir ağları, uzamsal immünoloji, immünoterapi biyobelirteçleri