Clear Sky Science · pt
Modelagem por redes neurais gráficas das interações tumor‑imunes espaciais identifica nichos celulares prognósticos no câncer de pulmão não pequenas células
Por que o entorno de um tumor importa
O câncer de pulmão costuma ser descrito em termos de genes e medicamentos, mas este estudo mostra que onde as células se posicionam umas em relação às outras dentro de um tumor pode ser tão importante quanto que tipo de células são. Ao ampliar milhões de células individuais de pacientes com câncer de pulmão não pequenas células, os pesquisadores usaram uma abordagem de inteligência artificial para ler a “rede social” de células tumorais e imunes. Eles descobriram que certos bairros celulares locais se associam fortemente ao tempo de sobrevida dos pacientes, oferecendo um caminho para previsões mais precisas e, potencialmente, escolhas mais inteligentes em imunoterapia.
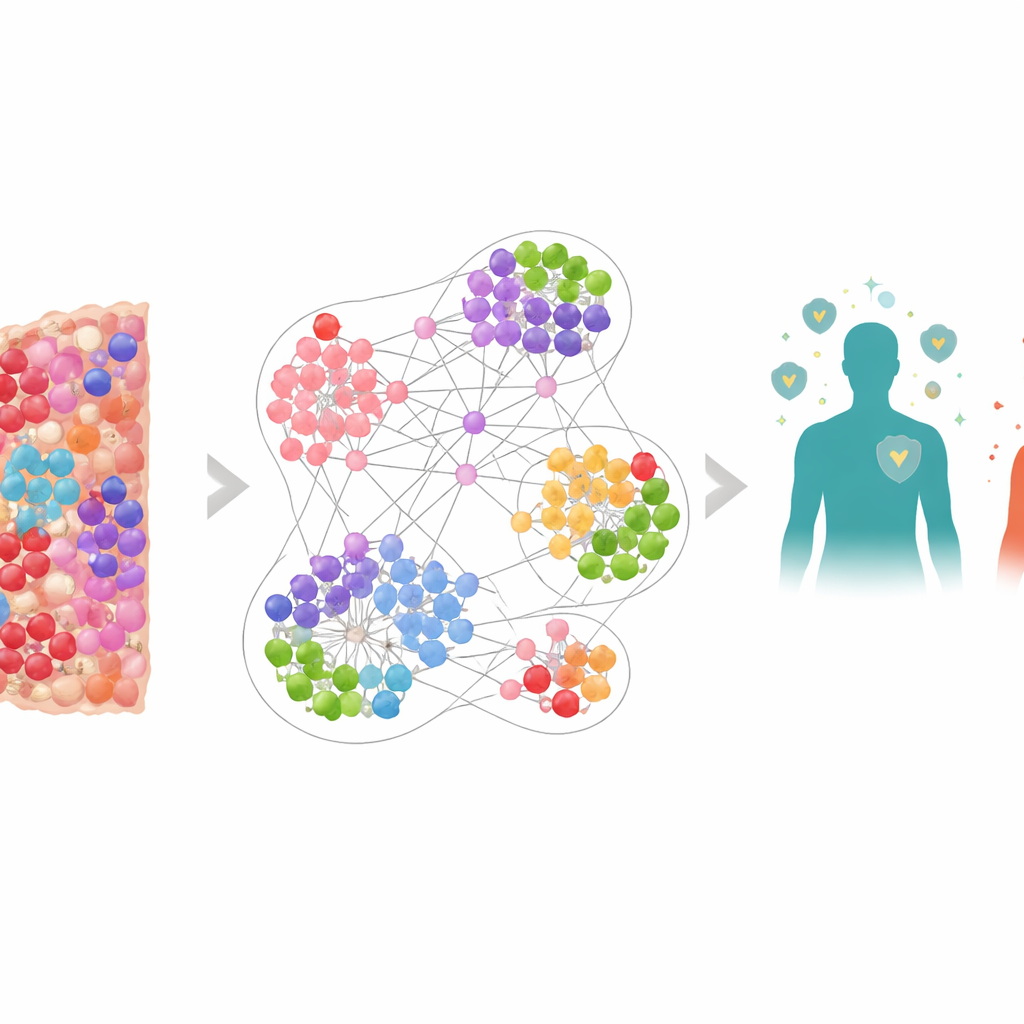
O câncer visto como uma cidade viva
Em vez de tratar um tumor como uma massa uniforme, a equipe o considerou como uma cidade lotada composta por muitos residentes diferentes: células cancerosas, células imunes defensoras e células supressoras que atenuam o ataque imune. Usando um método de imagem especial que marca múltiplos marcadores ao mesmo tempo, mapearam mais de 6,9 milhões de células a partir de biópsias de 506 pacientes com câncer de pulmão. A posição e a identidade de cada célula foram registradas, incluindo atores-chave como linfócitos T citotóxicos (CD8+), “freios” imunes como PD-1 e PD-L1, e linfócitos T reguladores marcados por FOXP3. Isso produziu mapas altamente detalhados do microambiente tumoral, o entorno imediato onde tumores e células imunes interagem constantemente.
Transformando mapas celulares em um modelo de rede
Para entender essa complexidade, os pesquisadores construíram uma rede neural gráfica, um tipo de IA projetada para operar em redes em vez de simples tabelas de números. No modelo, cada célula é um nó e células vizinhas estão conectadas por ligações, formando muitos “grafos de vizinhança” sobrepostos ao redor de cada célula. A rede foi treinada para aprender quais tipos de vizinhanças locais tendiam a aparecer em pacientes que viveram mais versus menos. Quando as previsões ao nível da vizinhança do modelo foram agregadas ao nível do paciente, ele previu a sobrevida com alta precisão, superando medidas mais simples como a contagem global de células T citotóxicas ou modelos que sabiam apenas onde as células estavam mas não o que expressavam.
Bairros bons e ruins dentro do tumor
Ao dissecar o que a IA aprendeu, a equipe identificou tipos distintos de vizinhanças locais com implicações muito diferentes para a sobrevida. Vizinhanças ricas em células T citotóxicas, especialmente quando células tumorais também expressavam marcadores de ativação imune, geralmente se associaram a melhores desfechos. Mas nem todas as áreas imunes densas eram benéficas. Algumas vizinhanças misturavam muitas células T citotóxicas com altos níveis de PD-L1 em células tumorais ou imunes próximas, sinalizando forte “desligamento” imune e pior sobrevida. Outras vizinhanças eram mais como desertos imunes, dominadas por células tumorais com pouquíssimos defensores, e essas também se ligaram a piores desfechos. Ao agrupar esses padrões, o estudo definiu vários “estados” tumorais recorrentes que equilibram ataque imune versus fuga imune.
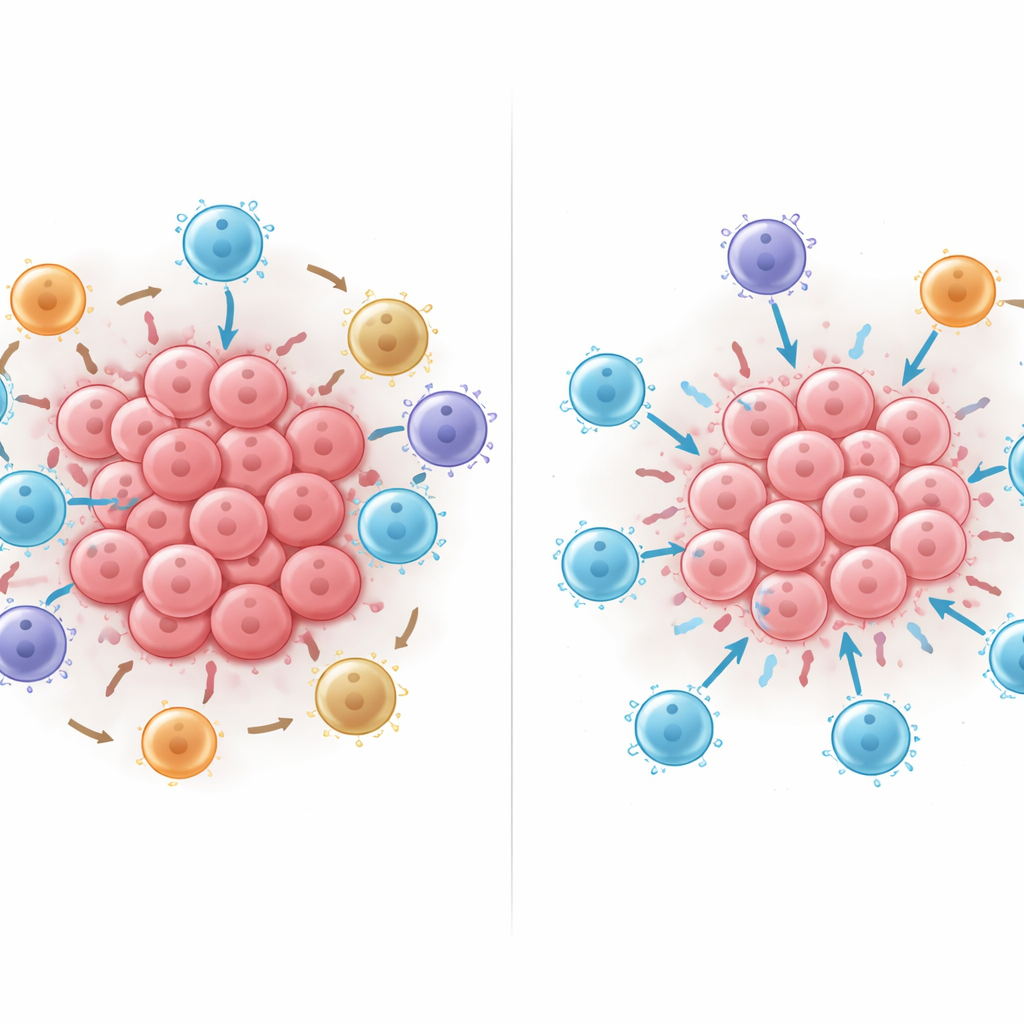
O que acontece quando você rearranja as células
Os pesquisadores então usaram o modelo de IA treinado como um laboratório virtual, adicionando, removendo ou movendo digitalmente células dentro das vizinhanças para ver como a previsão de sobrevida mudava. Adicionar células T citotóxicas quase sempre ajudou, mas ajudou mais quando essas células estavam em contato direto com células tumorais em vez de mantidas à distância. Mover células imunes supressoras PD-L1–positivas ou linfócitos T reguladores FOXP3-positivos para contato próximo com células T citotóxicas reduziu consistentemente a previsão de sobrevida do modelo, e o dano aumentou à medida que mais desses contatos eram criados. Esses experimentos in silico sugerem que padrões de contato físico — quem toca quem — podem inclinar fortemente o equilíbrio entre ataque tumoral eficaz e supressão imune.
Como isso pode moldar o cuidado do câncer no futuro
Para um leigo, a mensagem principal é que nem todos os tumores com “muitas células imunes” são iguais. Este estudo mostra que pequenos bairros — frequentemente apenas algumas dezenas de células — podem carregar sinais poderosos sobre se o sistema imune está vencendo ou perdendo a batalha local, e esses sinais predizem como os pacientes evoluem mesmo após ajustar por estádio tumoral ou pelo fato de terem recebido imunoterapia. Ao fornecer um roteiro para ler esses padrões espaciais com IA avançada, o trabalho aponta para testes de nova geração que vão além da contagem de células para medir como elas estão organizadas. Tais biomarcadores espaciais poderiam ajudar médicos a identificar melhor quais pacientes têm maior probabilidade de se beneficiar de tratamentos baseados no sistema imune e quais podem precisar de estratégias combinadas que desfaçam bairros celulares nocivos ou reforcem os favoráveis.
Citação: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Palavras-chave: câncer de pulmão não pequenas células, microambiente tumoral, redes neurais gráficas, imunologia espacial, biomarcadores de imunoterapia