Clear Sky Science · nl
Grafneurale-netwerkmodellering van ruimtelijke tumor-immuuninteracties identificeert prognostische cellulaire niches bij niet-kleincellige longkanker
Waarom de buurt rond een tumor ertoe doet
Longkanker wordt vaak beschreven in termen van genen en geneesmiddelen, maar deze studie laat zien dat waar cellen ten opzichte van elkaar staan binnen een tumor net zo belangrijk kan zijn als wat die cellen zijn. Door in te zoomen op miljoenen individuele cellen van patiënten met niet-kleincellige longkanker, gebruikte het team een kunstmatige-intelligentiebenadering om het "sociale netwerk" van tumor- en immuuncellen te lezen. Ze vonden dat bepaalde lokale celbuurten sterk samenhangen met hoe lang patiënten leven, wat een route biedt naar preciesere voorspellingen en mogelijk slimmere keuzes voor immunotherapie.
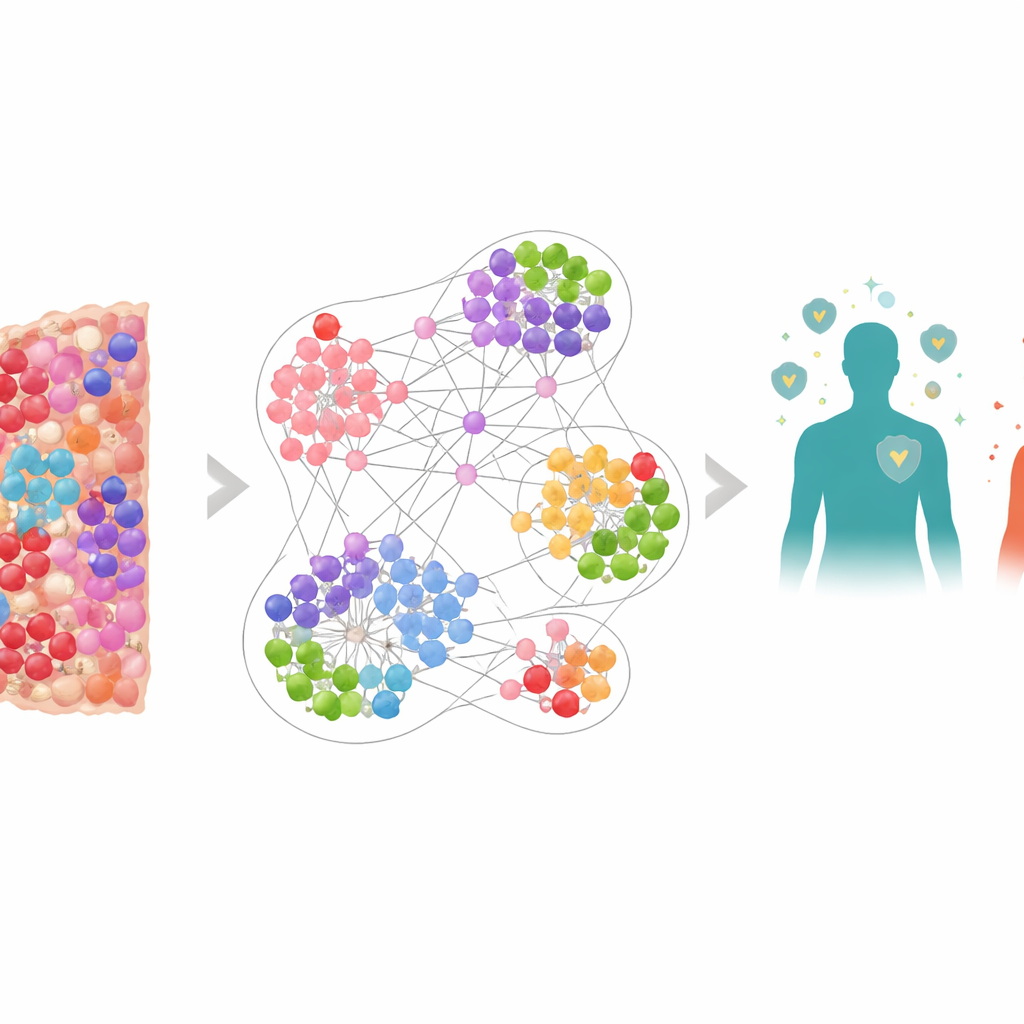
Kanker bekijken als een levende stad
In plaats van een tumor te behandelen als een uniforme massa, zagen de onderzoekers die als een drukke stad met veel verschillende bewoners: kankercellen, verdedigende immuuncellen en remmende cellen die de immuunrespons temperen. Met een speciale afbeeldingsmethode die meerdere markers tegelijk kleurt, hebben ze meer dan 6,9 miljoen cellen uit biopsiemonsters van 506 longkankerpatienten in kaart gebracht. Van elke cel werden positie en identiteit vastgelegd, inclusief sleutelfiguren zoals cytotoxische T-cellen (CD8+), immuun "remmen" zoals PD-1 en PD-L1, en regulerende T-cellen gemarkeerd door FOXP3. Dit leverde zeer gedetailleerde kaarten op van de tumormicro-omgeving, de directe omgeving waar tumoren en immuuncellen constant met elkaar interageren.
Celkaarten omzetten in een netwerkmodel
Om zo’n complexiteit te doorgronden, bouwden de onderzoekers een grafneurale netwerk, een type AI dat is ontworpen om op netwerken te werken in plaats van op eenvoudige tabellen met getallen. In hun model is elke cel een knooppunt en zijn aangrenzende cellen met elkaar verbonden door links, waardoor rond elke cel veel overlappende "buurtgrafieken" ontstaan. Het netwerk werd getraind om te leren welke soorten lokale buurten vaker voorkomen bij patiënten die langer versus korter leefden. Toen de voorspellingen op buurtniveau voor een patiënt werden gemiddeld, voorspelde het model de overleving zeer nauwkeurig en presteerde het beter dan eenvoudigere maatstaven zoals het totale aantal cytotoxische T-cellen of modellen die alleen wisten waar cellen zich bevonden maar niet wat ze tot expressie brachten.
Goede en slechte buurten binnen de tumor
Door te ontleden wat de AI had geleerd, identificeerde het team verschillende typen lokale buurten met zeer verschillende implicaties voor overleving. Buurten rijk aan cytotoxische T-cellen, vooral wanneer tumorerende cellen ook markers van immuunactivatie tot expressie brachten, waren over het algemeen geassocieerd met betere uitkomsten. Maar niet alle immuurrijke gebieden waren gunstig. Sommige buurten mengden veel cytotoxische T-cellen met hoge niveaus van PD-L1 op tumor- of nabijgelegen immuuncellen, wat een sterke immuun "uitschakeling" signaleerde en slechtere overleving. Andere buurten leken meer op immuunwoestijnen, gedomineerd door tumoren met zeer weinig verdedigers, en deze waren ook gekoppeld aan slechte uitkomsten. Door deze patronen te clusteren definieerde de studie meerdere terugkerende tumor"toestanden" die de balans tussen immuunaanval en immuunescape weerspiegelden.
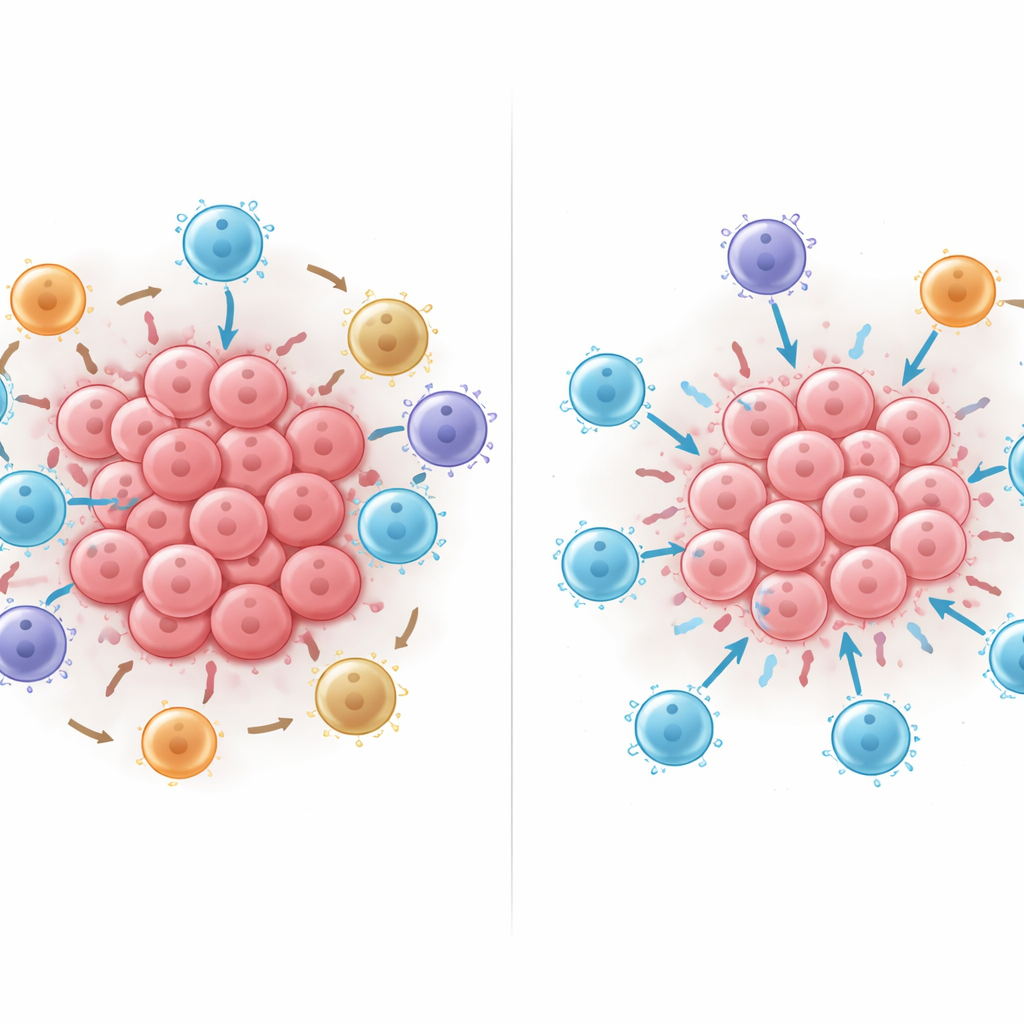
Wat er gebeurt als je de cellen herschikt
Vervolgens gebruikten de onderzoekers het getrainde AI-model als een virtueel laboratorium: ze voegden digitaal cellen toe, verwijderden ze of verplaatsten ze binnen buurten om te zien hoe de voorspelde overleving veranderde. Het toevoegen van cytotoxische T-cellen hielp bijna altijd, maar het hielp het meest wanneer die cellen direct in contact stonden met tumorcellen in plaats van op afstand gehouden te worden. Het dichtbij brengen van onderdrukkende PD-L1-positieve immuuncellen of FOXP3-positieve regulerende T-cellen in contact met cytotoxische T-cellen verminderde consequent de overlevingsvoorspelling van het model, en de schade nam toe naarmate meer van zulke contacten werden gecreëerd. Deze in-silico experimenten suggereren dat fysieke contactpatronen — wie wie aanraakt — de balans tussen effectieve tumoraanval en immuunsuppressie sterk kunnen doen kantelen.
Hoe dit de toekomstige kankerzorg kan vormen
Voor een niet-specialist is de belangrijkste boodschap dat niet alle tumoren met "veel immuuncellen" hetzelfde zijn. Deze studie laat zien dat kleine buurten — vaak maar een paar tientallen cellen — krachtige signalen kunnen dragen over of het immuunsysteem de lokale strijd wint of verliest, en deze signalen voorspellen hoe patiënten het doen zelfs nadat rekening is gehouden met tumorstadium of of ze immunotherapie hebben gekregen. Door een blauwdruk te bieden om deze ruimtelijke patronen met geavanceerde AI te lezen, wijst het werk op volgende-generatie tests die verder gaan dan cellen tellen en kijken naar hoe ze zijn gerangschikt. Dergelijke ruimtelijke biomarkers kunnen artsen helpen beter te bepalen welke patiënten waarschijnlijk baat hebben bij immuuntherapie en welke mogelijk combinatiestrategieën nodig hebben om schadelijke celbuurten te verstoren of nuttige te versterken.
Bronvermelding: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Trefwoorden: niet-kleincellige longkanker, tumormicro-omgeving, grafneurale netwerken, ruimtelijke immunologie, biomarkers voor immunotherapie