Clear Sky Science · ru
Моделирование пространственных взаимодействий опухоль‑иммунитет с помощью графовых нейронных сетей выявляет прогностические клеточные ниши при немелкоклеточном раке лёгкого
Почему важно окружение вокруг опухоли
Рак лёгкого часто описывают через гены и лекарства, но это исследование показывает: расположение клеток в пределах опухоли порой так же важно, как и их тип. Исследователи, изучив миллионы отдельных клеток пациентов с немелкоклеточным раком лёгкого, применили подход искусственного интеллекта, чтобы прочитать «социальную сеть» опухолевых и иммунных клеток. Они обнаружили, что определённые локальные клеточные окрестности сильно связаны с продолжительностью жизни пациентов, что открывает путь к более точным прогнозам и, возможно, к более обоснованному выбору иммунотерапии.
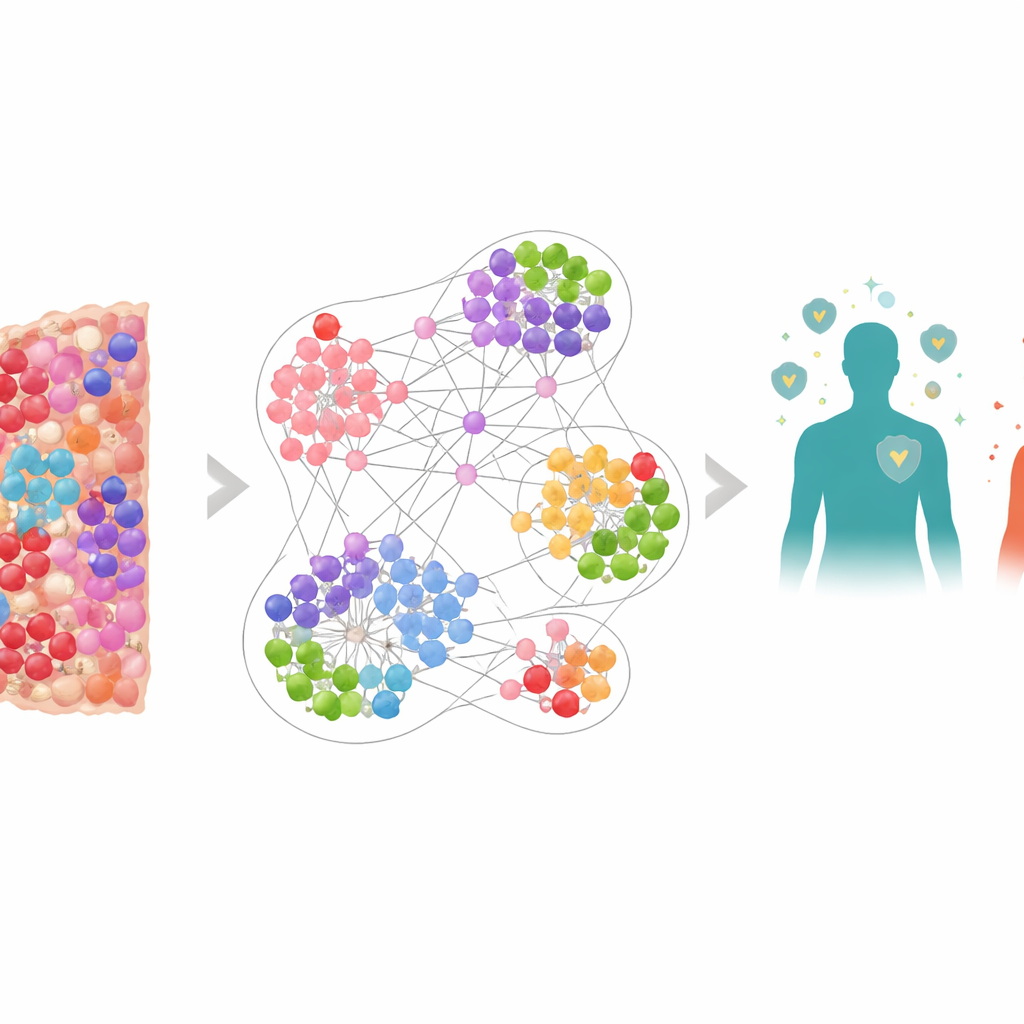
Рассматривать рак как живой город
Вместо того чтобы считать опухоль однородной массой, команда рассматривала её как переполненный город с разными жителями: раковыми клетками, защитными иммунными клетками и подавляющими клетками, которые ослабляют иммунную атаку. С помощью специального метода визуализации, окрашивающего сразу несколько маркеров, они картировали более 6,9 миллиона клеток из биопсий 506 пациентов с раком лёгкого. Были зафиксированы положение и идентичность каждой клетки, включая ключевые элементы: цитотоксические Т-клетки (CD8+), иммунные «тормоза» такие как PD-1 и PD-L1, а также регуляторные Т-клетки, отмеченные FOXP3. Это дало высокодетализированные карты микроокружения опухоли — непосредственной среды, где опухолевые и иммунные клетки постоянно взаимодействуют.
Преобразование карт клеток в сетевую модель
Чтобы понять такую сложность, исследователи построили графовую нейронную сеть — тип ИИ, предназначенный для работы с сетями, а не простыми таблицами чисел. В их модели каждая клетка представлена узлом, а соседние клетки связаны рёбрами, формируя множество пересекающихся «графов окрестностей» вокруг каждой клетки. Сеть обучали распознавать, какие виды локальных окрестностей чаще встречаются у пациентов с более длительной или более короткой выживаемостью. Когда прогнозы на уровне окрестностей усредняли для каждого пациента, модель очень точно предсказывала выживаемость, превосходя простые меры вроде общего числа цитотоксических Т-клеток или моделей, знавших только расположение клеток, но не их экспрессию.
Хорошие и плохие «окрестности» внутри опухоли
Анализируя, чему научилась ИИ, команда выделила разные типы локальных окрестностей с кардинально разным значением для выживаемости. Окрестности, богатые цитотоксическими Т-клетками, особенно если опухолевые клетки также экспрессировали маркеры иммунной активации, обычно ассоциировались с лучшими исходами. Но не все густонаселённые иммунные зоны были полезны. В некоторых окрестностях большое число цитотоксических Т-клеток сочеталось с высокой экспрессией PD-L1 на опухолевых или соседних иммунных клетках — признак сильной иммунной «отключки» и худшей выживаемости. Другие окрестности напоминали иммунные пустыни: доминировали опухолевые клетки и было мало защитников — это также связано с плохим прогнозом. Кластеризуя эти шаблоны, исследование выделило несколько повторяющихся «состояний» опухоли, отражающих баланс между иммунной атакой и уклонением от неё.
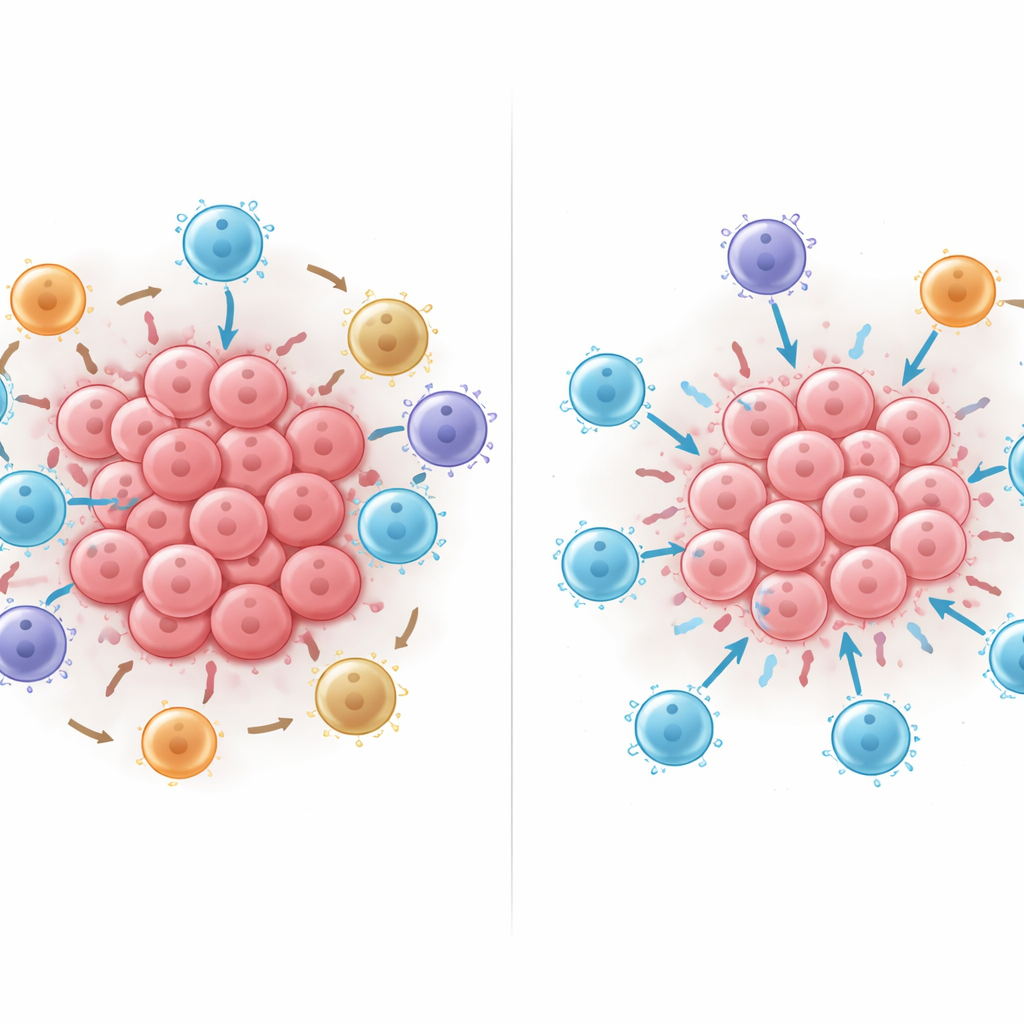
Что происходит, если переставить клетки
Далее исследователи использовали обученную модель ИИ как виртуальную лабораторию: цифровым путём добавляли, удаляли или перемещали клетки внутри окрестностей, чтобы посмотреть, как меняется прогноз выживаемости. Добавление цитотоксических Т-клеток почти всегда улучшало прогноз, но наибольшая польза наблюдалась, когда эти клетки находились в непосредственном контакте с опухолевыми клетками, а не на расстоянии. Перемещение подавляющих PD-L1‑положительных иммунных клеток или FOXP3‑положительных регуляторных Т-клеток в непосредственный контакт с цитотоксическими Т-клетками последовательно снижало предсказание выживаемости, и вред усиливался по мере появления большего числа таких контактов. Эти in-silico эксперименты указывают: физические паттерны контактов — кто с кем соприкасается — могут резко сдвигать баланс между эффективной атакой на опухоль и иммунным подавлением.
Как это может повлиять на будущее лечения рака
Для неспециалиста ключевая мысль такова: не все опухоли с «многими иммунными клетками» равны. Исследование показывает, что крошечные окрестности — часто всего несколько десятков клеток — несут мощные сигналы о том, выигрывает ли иммунная система местную битву или проигрывает, и эти сигналы предсказывают исход пациентов даже с учётом стадии опухоли или получения имимунотерапии. Предоставляя карту для считывания этих пространственных паттернов с помощью продвинутого ИИ, работа указывает на тесты следующего поколения, которые выходят за рамки простого подсчёта клеток и измеряют их организацию. Такие пространственные биомаркеры могут помочь врачам точнее определить, кто из пациентов вероятнее получит пользу от иммунотерапии, а кому потребуются комбинированные стратегии, разрушающие вредные клеточные окрестности или усиливающие полезные.»
Цитирование: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Ключевые слова: немелкоклеточный рак лёгкого, микроокружение опухоли, графовые нейронные сети, пространственная иммунология, биомаркеры иммунотерапии