Clear Sky Science · pl
Modelowanie sieci neuronowych grafowych przestrzennych interakcji nowotwór‑immunologia identyfikuje prognostyczne nisze komórkowe w niedrobnokomórkowym raku płuca
Dlaczego otoczenie guza ma znaczenie
Rak płuca jest często opisywany przez pryzmat genów i leków, ale to badanie pokazuje, że to, które komórki siedzą obok siebie wewnątrz guza, może być równie ważne jak to, jakie to są komórki. Przybliżając się do milionów pojedynczych komórek od pacjentów z niedrobnokomórkowym rakiem płuca, badacze zastosowali podejście sztucznej inteligencji do odczytania „sieci społecznych” komórek nowotworowych i immunologicznych. Odkryli, że pewne lokalne sąsiedztwa komórkowe są silnie powiązane z długością przeżycia pacjentów, co otwiera drogę do precyzyjniejszych prognoz i potencjalnie mądrzejszych wyborów immunoterapii.
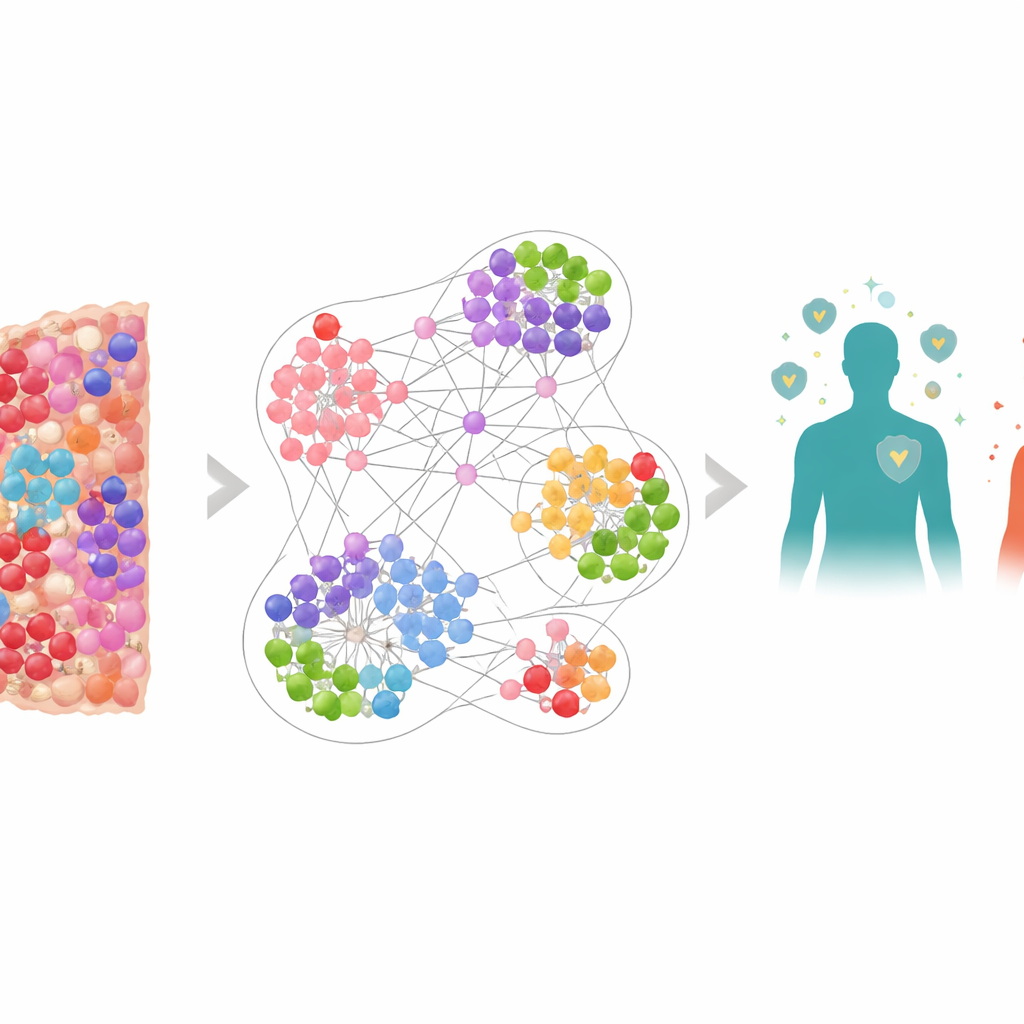
Postrzeganie nowotworu jako żywego miasta
Zamiast traktować guz jako jednorodną masę, zespół potraktował go jak zatłoczone miasto z wieloma różnymi mieszkańcami: komórkami nowotworowymi, obrończymi komórkami układu odpornościowego i komórkami hamującymi, które tłumią atak immunologiczny. Używając specjalnej metody obrazowania, barwiącej jednocześnie wiele markerów, odwzorowali ponad 6,9 miliona komórek z próbek biopsji od 506 pacjentów z rakiem płuca. Zanotowano pozycję i tożsamość każdej komórki, w tym kluczowych graczy, takich jak zabójcze limfocyty T (CD8+), „hamulce” immunologiczne typu PD-1 i PD-L1 oraz regulatorowe limfocyty T oznaczone FOXP3. Powstały szczegółowe mapy mikrośrodowiska guza — bezpośredniego otoczenia, gdzie guzy i komórki odpornościowe nieustannie wchodzą ze sobą w interakcje.
Przekształcanie map komórek w model sieci
Aby zrozumieć taką złożoność, badacze zbudowali grafową sieć neuronową, rodzaj SI zaprojektowany do pracy na sieciach zamiast prostych tabel liczbowych. W ich modelu każda komórka jest węzłem, a sąsiednie komórki łączy się krawędziami, tworząc wiele nakładających się „grafów sąsiedztw” wokół każdej komórki. Sieć była trenowana, by rozpoznać, jakie typy lokalnych sąsiedztw pojawiały się częściej u pacjentów żyjących dłużej w porównaniu z krócej. Gdy przewidywania na poziomie sąsiedztw uśredniono do poziomu pacjenta, model bardzo dokładnie prognozował przeżycie, bijąc prostsze miary, takie jak ogólna liczba zabójczych limfocytów T, czy modele znające jedynie położenie komórek bez informacji o tym, co one wyrażają.
Dobre i złe sąsiedztwa w obrębie guza
Analizując to, czego SI się nauczyła, zespół zidentyfikował odmienne typy lokalnych sąsiedztw o bardzo różnych implikacjach dla przeżycia. Sąsiedztwa bogate w zabójcze limfocyty T, zwłaszcza gdy komórki nowotworowe również wykazywały markery aktywacji immunologicznej, były generalnie skorelowane z lepszymi wynikami. Jednak nie wszystkie skupiska komórek odpornościowych były korzystne. W niektórych obszarach wiele zabójczych limfocytów współistniało z wysokim poziomem PD-L1 na komórkach nowotworowych lub pobliskich komórkach odpornościowych, co sygnalizowało silne „wyłączenie” immunologiczne i gorsze przeżycie. Inne obszary przypominały pustynie immunologiczne, zdominowane przez komórki nowotworowe i z bardzo niewielką liczbą obrońców — one też wiązały się z niekorzystnym rokowaniem. Grupując te wzorce, badanie zdefiniowało kilka powtarzających się „stanów” guza, równoważących atak immunologiczny i ucieczkę przed odpowiedzią odpornościową.
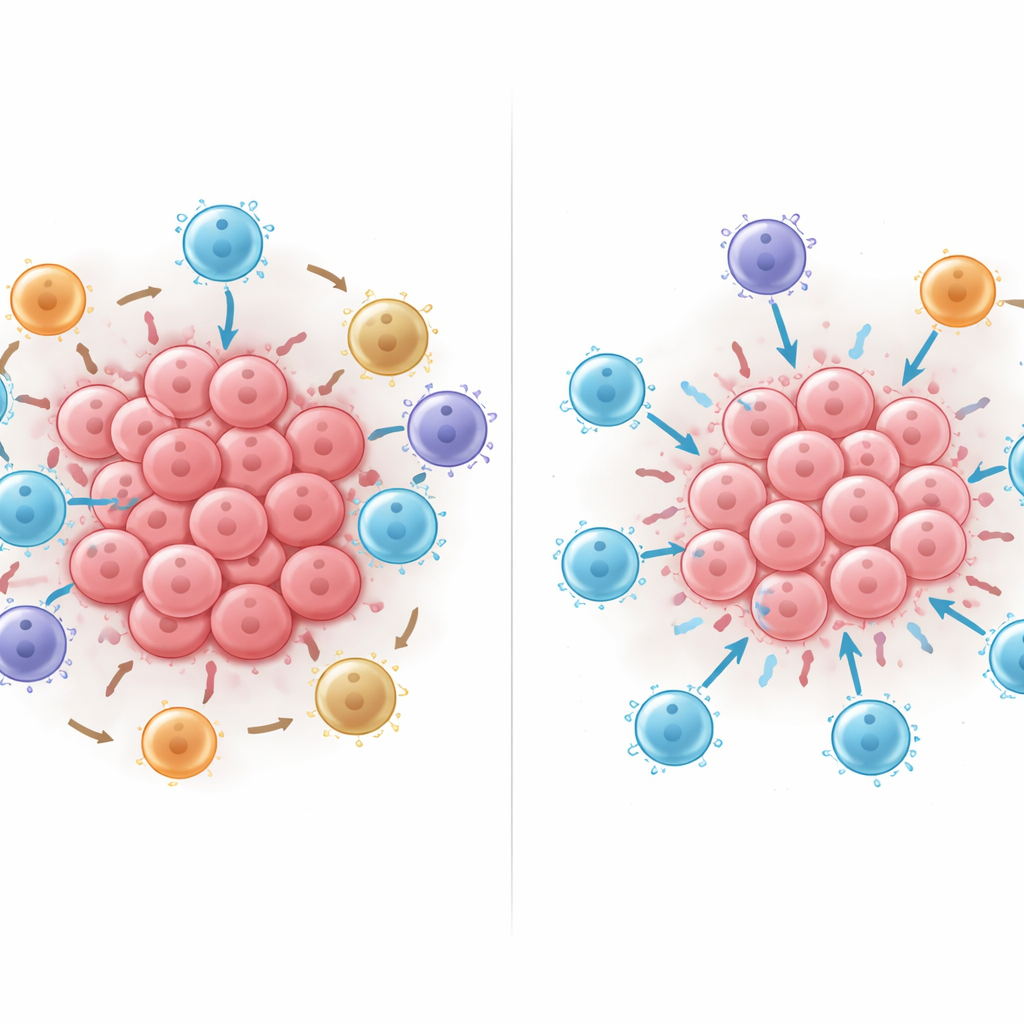
Co się dzieje, gdy przestawisz komórki
Następnie badacze użyli wytrenowanego modelu SI jak wirtualnego laboratorium, cyfrowo dodając, usuwając lub przesuwając komórki w obrębie sąsiedztw, aby zobaczyć, jak zmienia się przewidywane przeżycie. Dodanie zabójczych limfocytów T prawie zawsze pomagało, ale najbardziej pomagało, gdy te komórki były w bezpośrednim kontakcie z komórkami nowotworowymi, a nie trzymane na dystans. Przemieszczanie supresyjnych komórek odpornościowych z PD-L1 lub regulatorowych limfocytów T FOXP3+ w bliski kontakt z zabójczymi limfocytami T konsekwentnie obniżało przewidywanie przeżycia w modelu, a szkoda rosła wraz z liczbą takich kontaktów. Te eksperymenty in silico sugerują, że wzory fizycznych kontaktów — kto dotyka kogo — mogą wyraźnie przechylać równowagę między skutecznym atakiem na guz a immunosupresją.
Jak to może kształtować przyszłą opiekę onkologiczną
Dla laika kluczowy przekaz jest taki: nie wszystkie guzy z „wieloma komórkami odpornościowymi” są takie same. Badanie pokazuje, że maleńkie sąsiedztwa — często złożone z kilkudziesięciu komórek — mogą nieść silne sygnały o tym, czy układ odpornościowy wygrywa czy przegrywa lokalną walkę, i te sygnały prognozują losy pacjentów nawet po uwzględnieniu stadium choroby czy zastosowania immunoterapii. Dostarczając schematu odczytywania tych wzorców przestrzennych za pomocą zaawansowanej SI, praca wskazuje na testy nowej generacji, które wykraczają poza zwykłe liczenie komórek i mierzą sposób ich rozmieszczenia. Takie przestrzenne biomarkery mogłyby pomóc lekarzom lepiej wskazywać pacjentów, którzy najprawdopodobniej skorzystają z terapii immunologicznych, oraz tych, którzy mogą potrzebować strategii skojarzonych, niszczących szkodliwe sąsiedztwa komórkowe lub wzmacniających korzystne.
Cytowanie: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Słowa kluczowe: niedrobnokomórkowy rak płuca, mikrośrodowisko guza, grafowe sieci neuronowe, immunologia przestrzenna, biomarkery immunoterapii