Clear Sky Science · sv
Grafneuronnätsmodellering av rumsliga tumör‑immuninteraktioner identifierar prognostiska cellulära nischer vid icke‑småcellig lungcancer
Varför grannskapet runt en tumör spelar roll
Lungcancer beskrivs ofta utifrån gener och läkemedel, men den här studien visar att var celler sitter i förhållande till varandra i en tumör kan vara lika viktigt som vilka celler de är. Genom att zooma in på miljontals individuella celler från patienter med icke‑småcellig lungcancer använde forskarna en artificiell intelligensmetod för att läsa av tumörens och immunsystemets ”sociala nätverk”. De fann att vissa lokala cellgrannskap är starkt kopplade till patienternas överlevnad, vilket öppnar för mer precisa prognoser och potentiellt klokare val av immunterapi.
Att betrakta cancer som en levande stad
I stället för att behandla tumören som en homogen massa såg teamet den som en tätbefolkad stad med många olika invånare: cancerceller, försvarande immunceller och dämpande celler som dämpar immunsvaret. Med en specialiserad bildteknik som färgar flera markörer samtidigt kartlade de över 6,9 miljoner celler från biopsiprover från 506 lungcancerpatienter. Varje cells position och identitet registrerades, inklusive nyckelspelare som mördande T‑celler (CD8+), immunsystemets ”bromsar” såsom PD‑1 och PD‑L1, samt regulatoriska T‑celler markerade av FOXP3. Detta gav mycket detaljerade kartor över tumörmikromiljön, de omedelbara omgivningarna där tumörer och immunceller ständigt interagerar.
Att förvandla cellkartor till en nätverksmodell
För att förstå en sådan komplexitet byggde forskarna ett grafneuronnätverk, en typ av AI utformad för att arbeta på nätverk snarare än enkla tabeller med siffror. I deras modell är varje cell en nod och angränsande celler kopplas ihop med länkar, vilket bildar många överlappande ”grannskapsgrafer” kring varje cell. Nätverket tränades för att lära sig vilka typer av lokala grannskap som tenderade att förekomma hos patienter som levde längre respektive kortare. När modellens grannskapsnivåprediktioner i genomsnitt fördes upp till patientnivå prognosticerade den överlevnad mycket noggrant och överträffade enklare mått som totalt antal mördande T‑celler eller modeller som endast kände cellernas positioner men inte vad de uttryckte.
Goda och dåliga grannskap inne i tumören
Genom att dissekera vad AI:n hade lärt sig identifierade teamet distinkta typer av lokala grannskap med mycket olika betydelse för överlevnad. Grannskap rika på mördande T‑celler, särskilt när tumörceller också uttryckte markörer för immunaktivering, kopplades generellt till bättre utfall. Men inte alla täta immunområden var fördelaktiga. Vissa grannskap blandade många mördande T‑celler med höga nivåer av PD‑L1 på tumörceller eller närliggande immunceller, vilket signalerade stark immun ”avstängning” och sämre överlevnad. Andra grannskap liknade immunologiska öknar, dominerade av tumörceller med mycket få försvarare, och även dessa var kopplade till dåliga utfall. Genom att klustra dessa mönster definierade studien flera återkommande tumör"tillstånd" som balanserar immunattack mot immunflykt.
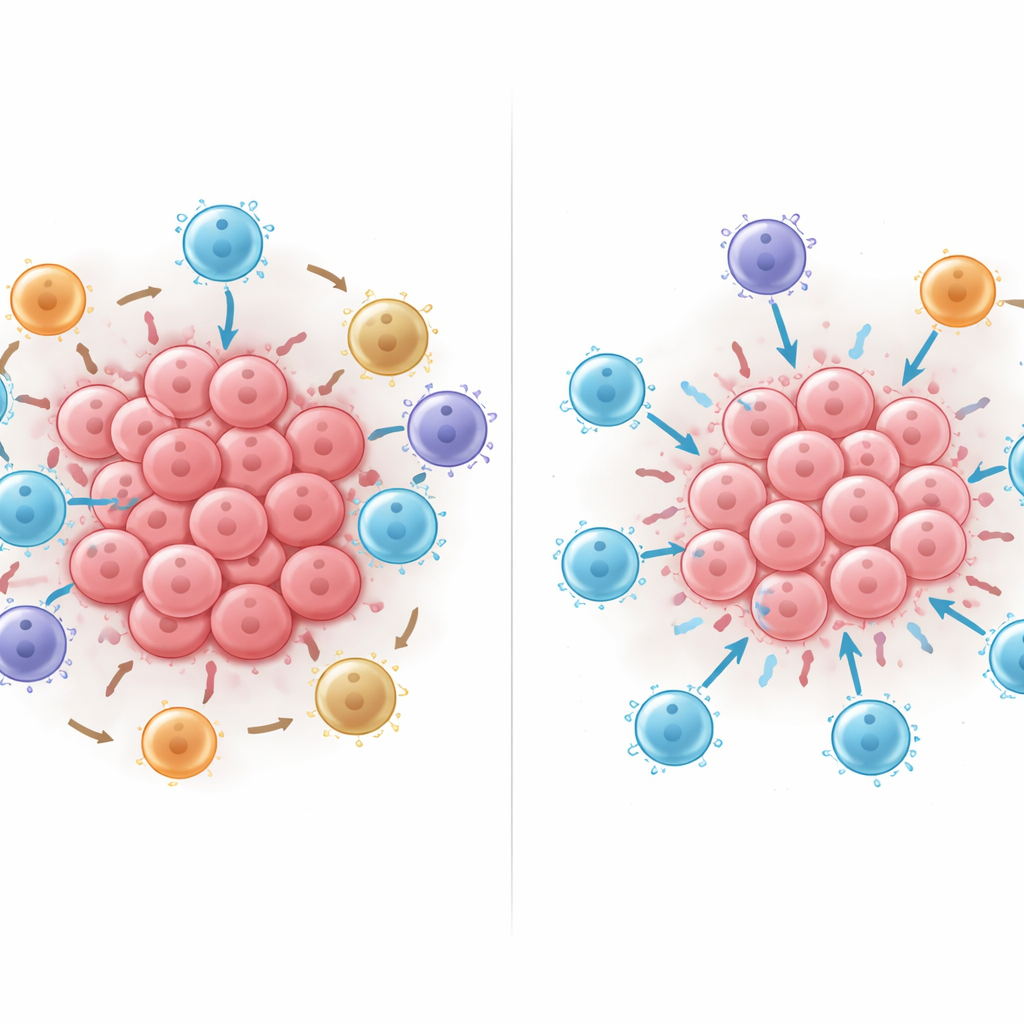
Vad som händer när du omarrangerar cellerna
Forskarna använde sedan den tränade AI‑modellen som ett virtuellt laboratorium och lade digitalt till, tog bort eller flyttade celler inom grannskap för att se hur den predicerade överlevnaden förändrades. Att lägga till mördande T‑celler hjälpte nästan alltid, men hjälpte mest när dessa celler var i direkt kontakt med tumörceller i stället för avstånd. Att flytta dämpande PD‑L1‑positiva immunceller eller FOXP3‑positiva regulatoriska T‑celler i nära kontakt med mördande T‑celler sänkte konsekvent modellens överlevnadsprediktion, och skadan ökade i takt med att fler sådana kontakter skapades. Dessa in silico‑experiment tyder på att fysiska kontaktmönster — vem som rör vid vem — kan kraftigt förskjuta balansen mellan effektiv tumörattack och immunosuppression.
Hur detta kan påverka framtidens cancervård
För en lekmannapublik är huvudbudskapet att inte alla tumörer med ”många immunceller” är likadana. Den här studien visar att små grannskap — ofta bara några dussin celler — kan bära stark information om huruvida immunsystemet vinner eller förlorar den lokala striden, och dessa signaler förutsäger patientutfall även efter att man tagit hänsyn till tumörstadium eller om de fått immunterapi. Genom att erbjuda en plan för att läsa dessa rumsliga mönster med avancerad AI pekar arbetet mot nästa generations tester som går bortom att räkna celler till att mäta hur de är ordnade. Sådana rumsliga biomarkörer skulle kunna hjälpa läkare att bättre identifiera vilka patienter sannolikt får nytta av immunbaserade behandlingar och vilka som kan behöva kombinationsstrategier som stör skadliga cellgrannskap eller stärker gynnsamma.
Citering: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Nyckelord: icke‑småcellig lungcancer, tumörmikromiljö, grafneuronnätverk, rumslig immunologi, biomarkörer för immunterapi