Clear Sky Science · ar
نمذجة الشبكات العصبية البيانية للتفاعلات المكانية بين الورم والمناعة تكشف عن محميات خلوية تكوينية للتنبؤ في سرطان الرئة غير صغير الخلايا
لماذا يهم الحي المحيط بالورم
عادة ما يُوصَف سرطان الرئة من حيث الجينات والأدوية، لكن هذه الدراسة تُظهر أن موقع الخلايا بجانب بعضها داخل الورم قد يكون بنفس أهمية نوع هذه الخلايا. من خلال تكبير صور ملايين الخلايا الفردية من مرضى سرطان الرئة غير صغير الخلايا، استخدم الباحثون نهجاً ذكياً اصطناعياً لقراءة "شبكة العلاقات" بين خلايا الورم والمناعة. وجدوا أن أحياء خلوية محلية معينة مرتبطة ارتباطاً قوياً بزمن بقاء المرضى على قيد الحياة، ما يفتح طريقاً لتنبؤات أدق وربما خيارات علاج مناعي أكثر ذكاءً.
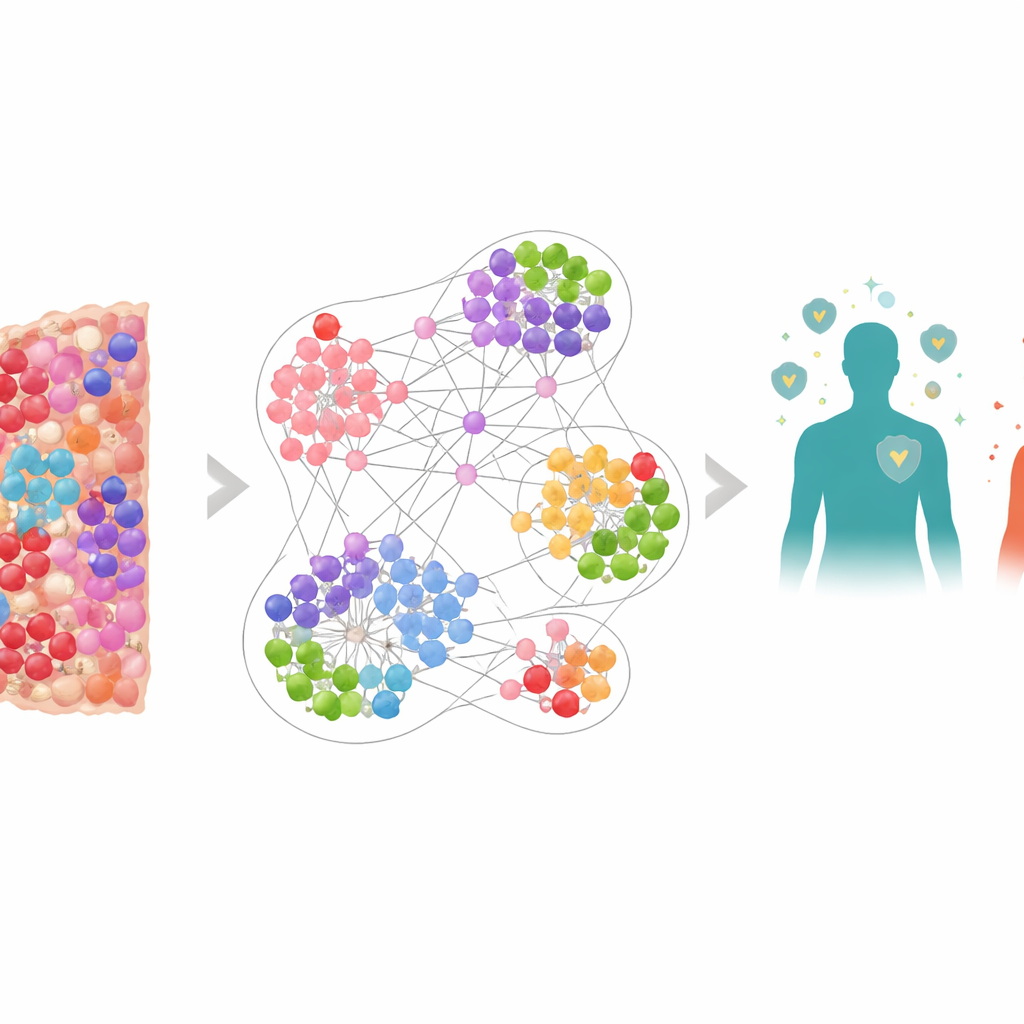
النظر إلى السرطان كمدينة حية
بدلاً من التعامل مع الورم ككتلة متجانسة، نظر الفريق إليه كمدينة مكتظة تتألف من العديد من السكان المختلفين: خلايا سرطانية، خلايا مناعية دفاعية، وخلايا مثبطة تخفف الهجوم المناعي. باستخدام طريقة تصوير خاصة تصبغ عدة مؤشرات في آن واحد، خرّطوا أكثر من 6.9 مليون خلية من عينات خزعات لـ506 مرضى بسرطان الرئة. سُجل موقع وهوية كل خلية، بما في ذلك لاعبين أساسيين مثل الخلايا التائية القاتلة (CD8+) و"مكابح" المناعة مثل PD-1 وPD-L1، والخلايا التائية المنظمة المميزة بـFOXP3. أنتج هذا خرائط مفصلة للغاية للبيئة الدقيقة للورم، المحيط الفوري حيث تتفاعل الأورام والخلايا المناعية باستمرار.
تحويل خرائط الخلايا إلى نموذج شبكي
لفهم هذه التعقيدات، بنى الباحثون شبكة عصبية بيانية، نوع من الذكاء الاصطناعي مصمم للعمل على الشبكات بدل الجداول البسيطة من الأرقام. في نموذجهم، كل خلية تمثل عقدة والخلايا المجاورة مرتبطة بروابط، مكونة العديد من "رسوم أحياء" متداخلة حول كل خلية. درّبوا الشبكة لتتعلم أي أنواع الأحياء المحلية كانت أكثر شيوعاً لدى المرضى الذين عاشوا لفترات أطول مقابل الأقصر. عندما جُمعت توقعات النموذج على مستوى الأحياء إلى مستوى المريض، تنبأت بالبقاء بدقة عالية، متفوقة على مقاييس أبسط مثل عدد الخلايا التائية القاتلة إجمالاً أو نماذج تعرف فقط مواقع الخلايا دون ما تعبر عنه.
الأحياء الجيدة والسيئة داخل الورم
من خلال تفكيك ما تعلمه الذكاء الاصطناعي، حدد الفريق أنواعاً مميزة من الأحياء المحلية ذات دلالات مختلفة جداً للبقاء. كانت الأحياء الغنية بالخلايا التائية القاتلة، خصوصاً عندما عبرت الخلايا الورمية أيضاً عن مؤشرات تنشيط مناعي، مرتبطة عموماً بنتائج أفضل. لكن ليست كل المناطق المليئة بالمناعة مفيدة. بعض الأحياء جمعت بين كثير من الخلايا التائية القاتلة ومستويات عالية من PD-L1 على الخلايا الورمية أو الخلايا المناعية القريبة، مما يشير إلى إغلاق مناعي قوي وبقاء أسوأ. كانت أحياء أخرى أقرب إلى صحارى مناعية، يهيمن عليها الخلايا الورمية مع قلة المدافعين، وهذه أيضاً ارتبطت بنتائج سيئة. من خلال تجميع هذه الأنماط، عرّفت الدراسة عدة "حالات" ورمية متكررة توازن بين الهجوم المناعي وفرار المناعة.
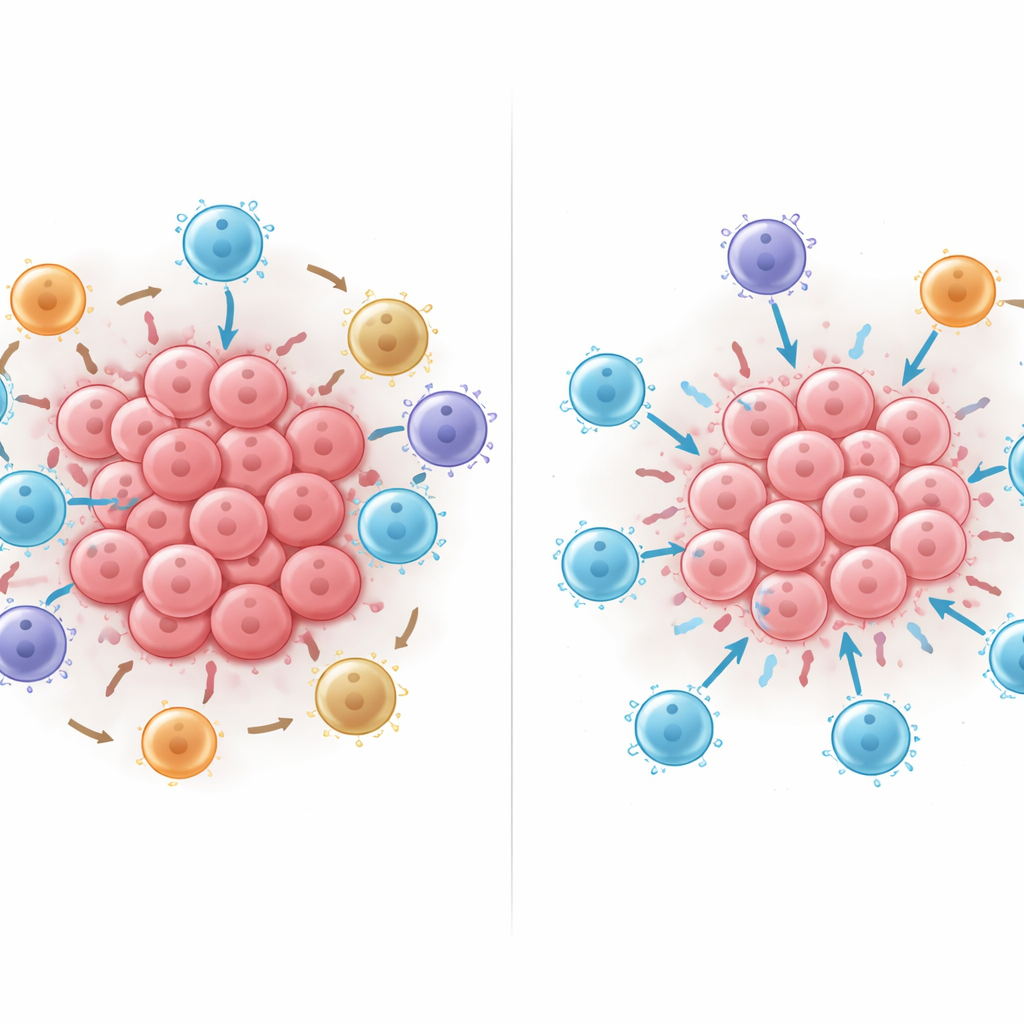
ماذا يحدث عندما تعيد ترتيب الخلايا
استخدم الباحثون بعد ذلك نموذج الذكاء الاصطناعي المدرب كمعمل افتراضي، بإضافة أو إزالة أو تحريك الخلايا رقمياً داخل الأحياء لرؤية كيف يتغير التنبؤ بالبقاء. إضافة الخلايا التائية القاتلة كانت تساعد تقريباً دائماً، لكنها أفادت أكثر عندما كانت هذه الخلايا على اتصال مباشر بالخلايا الورمية بدلاً من أن تُترك بعيداً. نقل الخلايا المناعية المثبطة الحاملة لـPD-L1 أو الخلايا التائية المنظمة الإيجابية لـFOXP3 إلى اتصال وثيق مع الخلايا التائية القاتلة قلّل باستمرار من توقع البقاء لدى النموذج، وتزايد الضرر مع زيادة مثل هذه الاتصالات. تشير هذه التجارب الحاسوبية إلى أن أنماط التلامس الفيزيائي — من يلامس من — يمكن أن تميل الميزان بشدة نحو هجوم ورمي فعال أو كبت مناعي.
كيف قد يشكل هذا رعاية السرطان في المستقبل
بالنسبة للقارئ العام، الرسالة الأساسية أن ليس كل الأورام التي تحتوي على "كثير من الخلايا المناعية" متشابهة. تُظهر هذه الدراسة أن الأحياء الميكروسكوبية — غالباً مجرد عشرات الخلايا — يمكن أن تحمل إشارات قوية عمّا إذا كان الجهاز المناعي يحقق النصر أو يخسر المعركة المحلية، وتنبؤات هذه الإشارات تظل قائمة حتى بعد احتساب مرحلة الورم أو ما إذا كان المريض قد تلقى علاجاً مناعياً. من خلال تقديم مخطط لقراءة هذه الأنماط المكانية بالذكاء الاصطناعي المتقدم، يشير العمل إلى اختبارات من الجيل التالي تتجاوز عدّ الخلايا إلى قياس كيف تُرتّب. يمكن أن تساعد مثل هذه العلامات المكانية الأطباء على تحديد أي المرضى من المرجح أن يستفيدوا من العلاجات المناعية وأيهم قد يحتاج إلى استراتيجيات مركبة تفكك الأحياء الخلوية الضارة أو تعزز الأحياء المفيدة.
الاستشهاد: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
الكلمات المفتاحية: سرطان الرئة غير صغير الخلايا, البيئة الدقيقة للورم, الشبكات العصبية البيانية, علم المناعة المكاني, مؤشرات حيوية للعلاج المناعي