Clear Sky Science · es
Modelado con redes neuronales gráficas de las interacciones espaciales tumor‑inmunes identifica nichos celulares pronósticos en el cáncer de pulmón no microcítico
Por qué importa el vecindario alrededor de un tumor
El cáncer de pulmón suele describirse en términos de genes y fármacos, pero este estudio muestra que la posición relativa de las células dentro de un tumor puede ser tan importante como el tipo de célula. Al examinar millones de células individuales de pacientes con cáncer de pulmón no microcítico, los investigadores emplearon un enfoque de inteligencia artificial para leer la “red social” de células tumorales e inmunes. Encontraron que ciertos vecindarios celulares locales se asocian de forma clara con la supervivencia de los pacientes, lo que abre la vía a predicciones más precisas y, potencialmente, a opciones de inmunoterapia más acertadas.
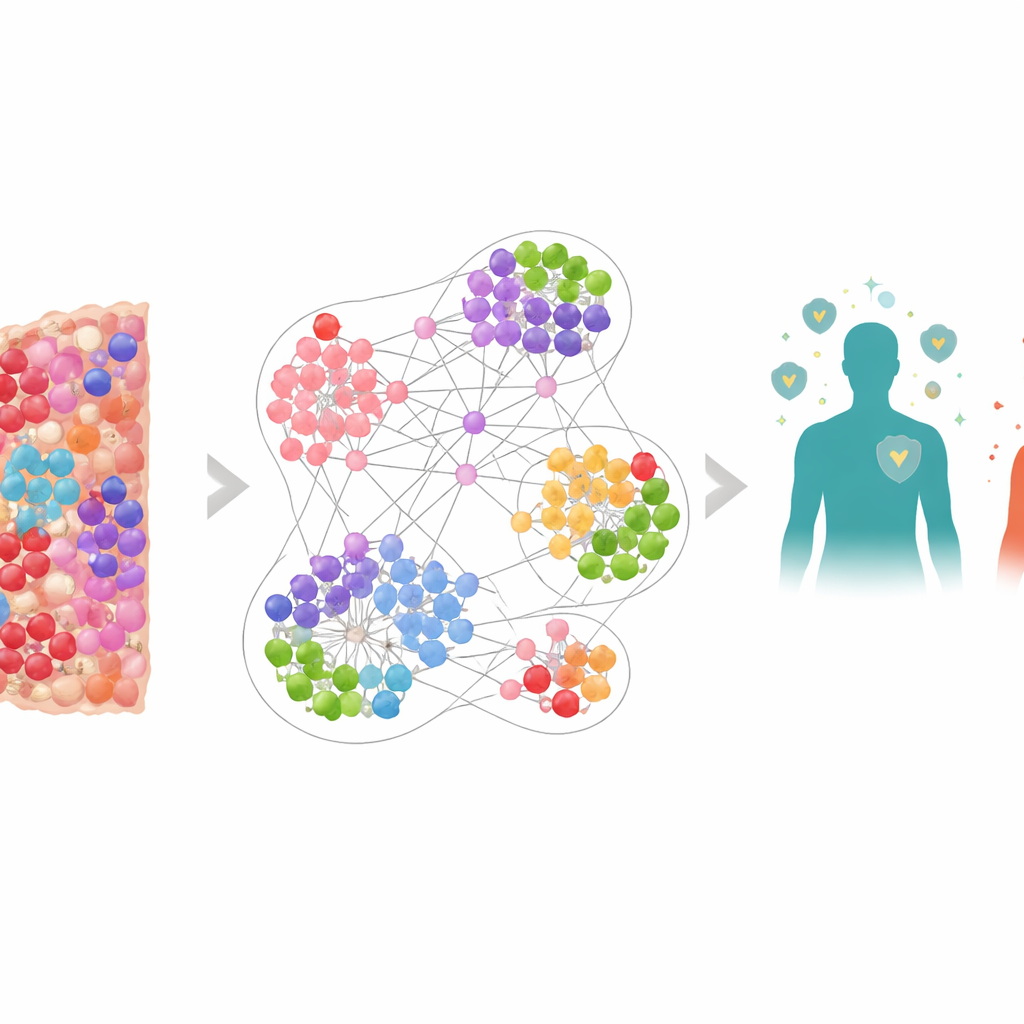
Ver el cáncer como una ciudad viva
En lugar de tratar el tumor como una masa uniforme, el equipo lo concibió como una ciudad abarrotada compuesta por distintos residentes: células cancerosas, células inmunes defensoras y células supresoras que frenan el ataque inmunitario. Usando un método de imagenación que tiñe múltiples marcadores a la vez, cartografiaron más de 6,9 millones de células procedentes de biopsias de 506 pacientes con cáncer de pulmón. Se registró la posición y la identidad de cada célula, incluidos actores clave como los linfocitos T citotóxicos (CD8+), los “frenos” inmunitarios como PD-1 y PD-L1, y las células T reguladoras marcadas por FOXP3. Esto produjo mapas muy detallados del microambiente tumoral, el entorno inmediato donde tumores y células inmunes interactúan constantemente.
Convertir mapas celulares en un modelo de red
Para comprender tal complejidad, los investigadores construyeron una red neuronal gráfica, un tipo de IA diseñada para trabajar sobre redes en lugar de tablas simples de números. En su modelo, cada célula es un nodo y las células vecinas están conectadas por enlaces, formando muchos “grafos de vecindario” superpuestos alrededor de cada célula. La red se entrenó para aprender qué tipos de vecindarios locales tendían a aparecer en pacientes con mayor o menor supervivencia. Cuando las predicciones a nivel de vecindario del modelo se promediaron a nivel de paciente, la predicción de supervivencia fue muy precisa, superando medidas más simples como el recuento total de linfocitos T citotóxicos o modelos que solo conocían la localización de las células pero no lo que expresaban.
Vecindarios buenos y malos dentro del tumor
Al analizar lo que la IA había aprendido, el equipo identificó tipos distintos de vecindarios locales con implicaciones muy diferentes para la supervivencia. Los vecindarios ricos en linfocitos T citotóxicos, especialmente cuando las células tumorales también expresaban marcadores de activación inmune, se asociaron generalmente con mejores resultados. Pero no todas las zonas con muchas células inmunes fueron beneficiosas. Algunos vecindarios mezclaban numerosos linfocitos T citotóxicos con altos niveles de PD-L1 en células tumorales o inmunes cercanas, lo que señalaba una fuerte «desactivación» inmune y peor supervivencia. Otros espacios eran más bien desiertos inmunes, dominados por células tumorales con muy pocos defensores, y estos también se relacionaron con malos resultados. Al agrupar estos patrones, el estudio definió varios “estados” tumorales recurrentes que equilibran el ataque inmunitario frente a la evasión inmune.
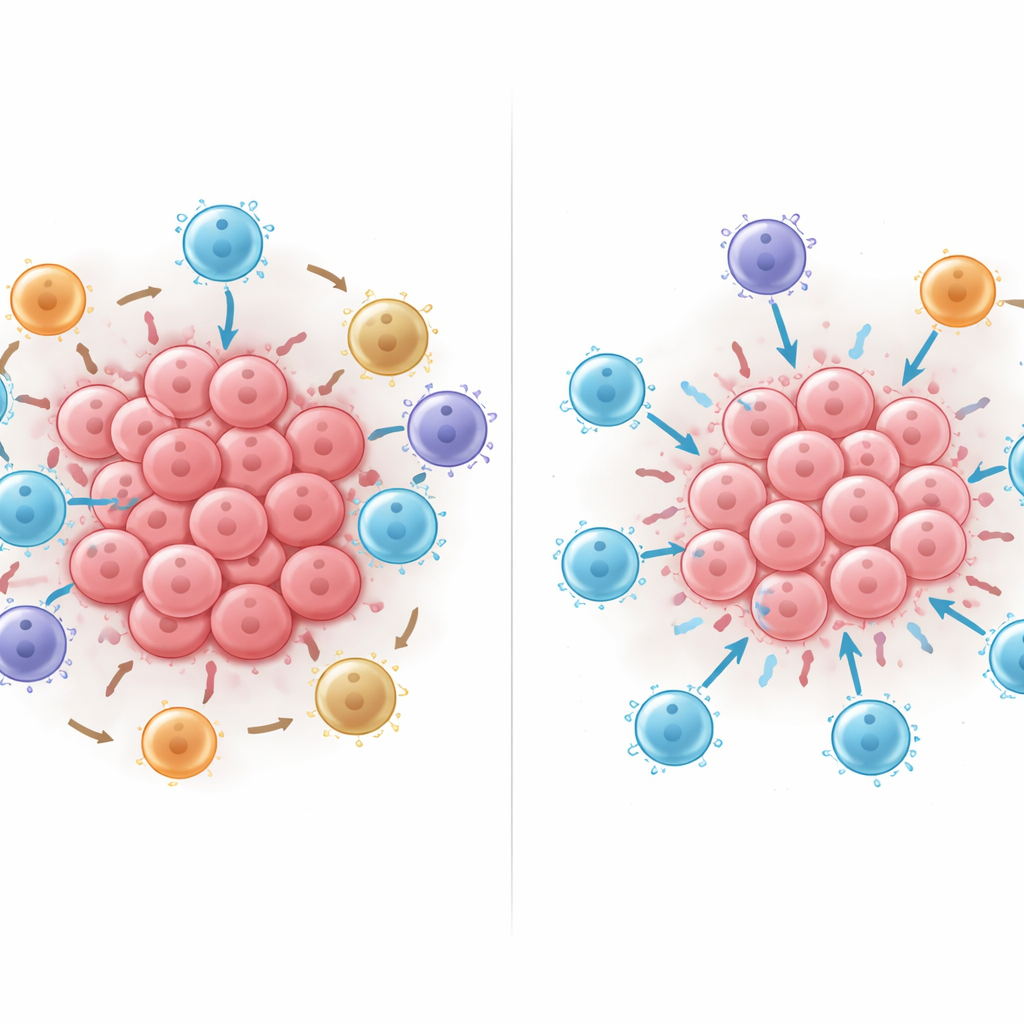
Qué ocurre cuando reorganizas las células
Los investigadores usaron entonces el modelo de IA entrenado como un laboratorio virtual, añadiendo, eliminando o moviendo células digitalmente dentro de los vecindarios para observar cómo cambiaba la supervivencia predicha. Añadir linfocitos T citotóxicos casi siempre mejoró la predicción, pero lo hizo en mayor medida cuando esas células estaban en contacto directo con las tumorales en lugar de permanecer a distancia. Mover células inmunes supresoras positivas para PD-L1 o células T reguladoras positivas para FOXP3 a contacto estrecho con linfocitos T citotóxicos redujo de forma consistente la predicción de supervivencia del modelo, y el efecto dañino aumentaba conforme se creaban más de esos contactos. Estos experimentos in silico sugieren que los patrones de contacto físico —quién toca a quién— pueden inclinar drásticamente el equilibrio entre un ataque tumoral efectivo y la supresión inmune.
Cómo podría influir esto en la atención oncológica futura
Para un público general, el mensaje clave es que no todos los tumores con “muchas células inmunes” son iguales. Este estudio muestra que pequeños vecindarios —a menudo apenas unas decenas de células— pueden contener señales potentes sobre si el sistema inmune está ganando o perdiendo la batalla local, y estas señales predicen la evolución de los pacientes incluso tras ajustar por estadio tumoral o por si recibieron inmunoterapia. Al ofrecer un plano para leer estos patrones espaciales con IA avanzada, el trabajo apunta hacia pruebas de nueva generación que vayan más allá de contar células y midan cómo están dispuestas. Tales biomarcadores espaciales podrían ayudar a los médicos a identificar mejor qué pacientes es probable que se beneficien de tratamientos basados en el sistema inmune y cuáles podrían necesitar estrategias combinadas que rompan vecindarios celulares dañinos o refuercen los beneficiosos.
Cita: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Palabras clave: cáncer de pulmón no microcítico, microambiente tumoral, redes neuronales gráficas, inmunología espacial, biomarcadores de inmunoterapia