Clear Sky Science · he
מודל רשת עצבית גרפית של אינטראקציות מרחביות בין גידול למערכת החיסון מזהה נישות תאיות פרוגנוסטיות בסרטן ריאה שאינו תאי זיר
למה השכונה סביב הגידול משנה
סרטן הריאה מתואר לעתים קרובות במונחים של גנים ותרופות, אך המחקר הזה מראה שלמיקום התאים זה לצד זה בתוך הגידול יכולה להיות חשיבות זהה לסוגיות של אותם תאים. על ידי התמקדות במיליוני תאים בודדים של מטופלים עם סרטן ריאה שאינו תאי זיר, החוקרים השתמשו בגישה של בינה מלאכותית כדי לקרוא את “הרשת החברתית” של תאי הגידול והתאים החיסוניים. הם מצאו כי ישנם אזורים מקומיים מסוימים של תאים שמקושרים באופן חזק לאורך חיי המטופלים, מה שמציע נתיב לניבויים מדויקים יותר ואולי לבחירות חכמות יותר של אימונותרפיה.
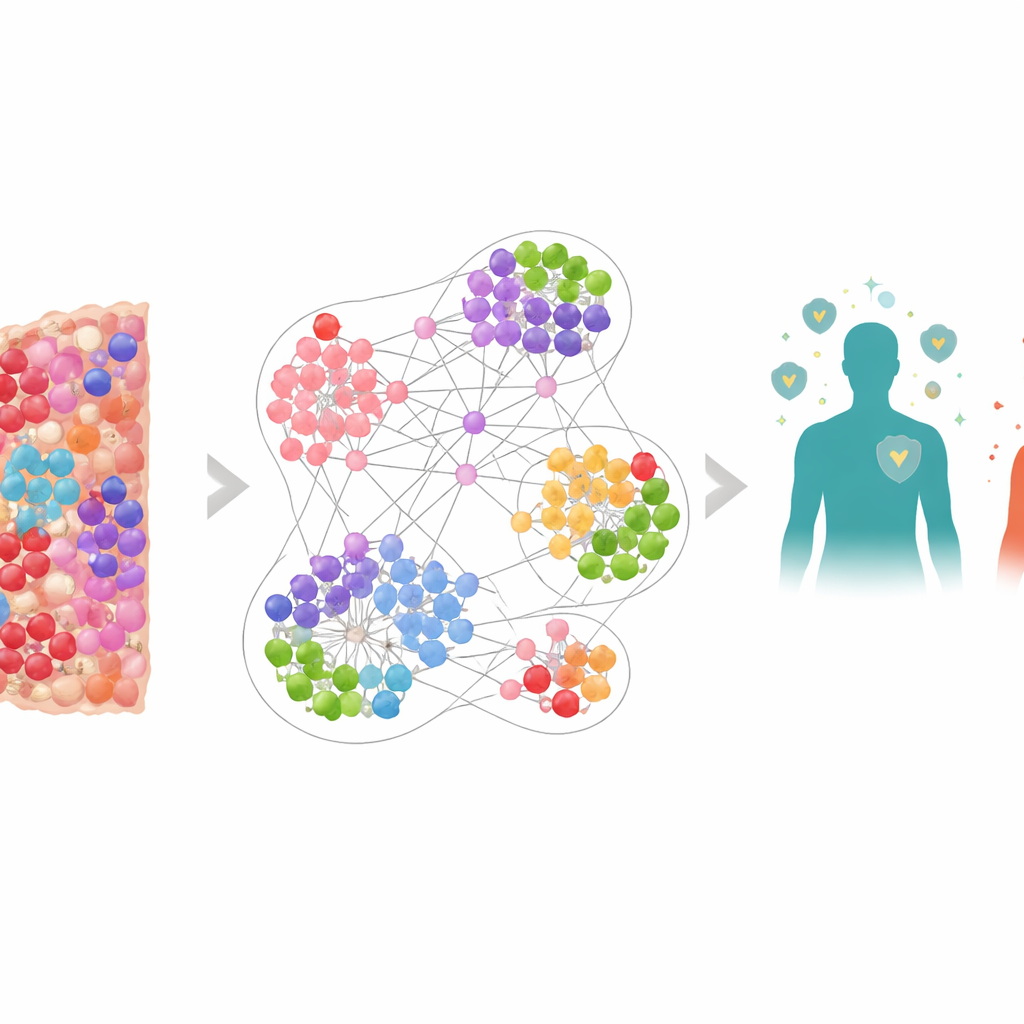
להסתכל על הסרטן כמו עיר חיה
במקום להתייחס לגידול כמסה אחידה, הצוות ראה אותו כעיר צפופה המורכבת מתושבים שונים: תאי סרטן, תאי חיסון מגינים ותאים מדכאים שמעכבים את המתקפה החיסונית. באמצעות שיטת הדמיה מיוחדת שמסמנת מספר סמנים בו‑זמנית, הם מיפו מעל 6.9 מיליון תאים מדגימות ביופסיה של 506 חולים בסרטן ריאה. מיקום וזיהוי כל תא נרשמו, כולל שחקנים מרכזיים כמו תאי T קטלניים (CD8+), “בלמים” חיסוניים כגון PD-1 ו‑PD-L1, ותאי T רגולטוריים המסומנים ב‑FOXP3. זה הניב מפות מפורטות מאוד של המיקרו‑סביבה של הגידול — הסביבה המיידית שבה תאי הגידול והתאים החיסוניים באינטראקציה מתמדת.
להפוך מפות תאים למודל רשת
כדי לפענח את המורכבות הזו, החוקרים בנו רשת עצבית גרפית, סוג של בינה מלאכותית שמיועדת לעבוד על רשתות במקום על טבלאות מספרים פשוטות. במודל שלהם כל תא הוא צומת ותאים שכנים מקושרים בקישורים, מה שיוצר סביב כל תא הרבה "גרפי שכונות" החופפים זה את זה. המערכת אומנה לזהות אילו סוגי שכונות מקומיות נטו להופיע בחולים שחיו זמן רב יותר לעומת קצרים יותר. כאשר תחזיות ברמת השכונה נערכו לממוצע ברמת המטופל, המודל חזא השרידות בדיוק רב, והיה טוב יותר ממידות פשוטות כמו כמות תאי ה‑T הקטלניים הכוללת או ממודלים שידעו רק היכן התאים נמצאים מבלי לדעת מה הם מבטאים.
שכונות טובות ורעות בתוך הגידול
על ידי ניתוח מה שלמדה ה‑AI, הצוות זיהה סוגים מובחנים של שכונות מקומיות עם השלכות שונות מאוד על השרידות. שכונות עשירות בתאי T קטלניים, במיוחד כאשר תאי הגידול גם הביעו סמנים של הפעלה חיסונית, היו בדרך כלל מקושרות לתוצאות טובות יותר. אך לא כל אזורי הצפיפות החיסונית היו מועילים. חלק מהשכונות ערבבו תאי T רבים עם רמות גבוהות של PD-L1 על תאי הגידול או תאים חיסוניים סמוכים, המצביע על כיבוי חיסוני חזק ותוצאות גרועות יותר. שכונות אחרות היו יותר כמו מדבריות חיסוניות, נשלטות על ידי תאי הגידול עם מעט מגינים — גם הן קשורות לתוחלת חיים נמוכה. על ידי אשכול של דפוסים אלה, המחקר הגדיר מספר "מצבי" גידול חוזרים שמאזנים בין מתקפה חיסונית לבריחת חיסון.
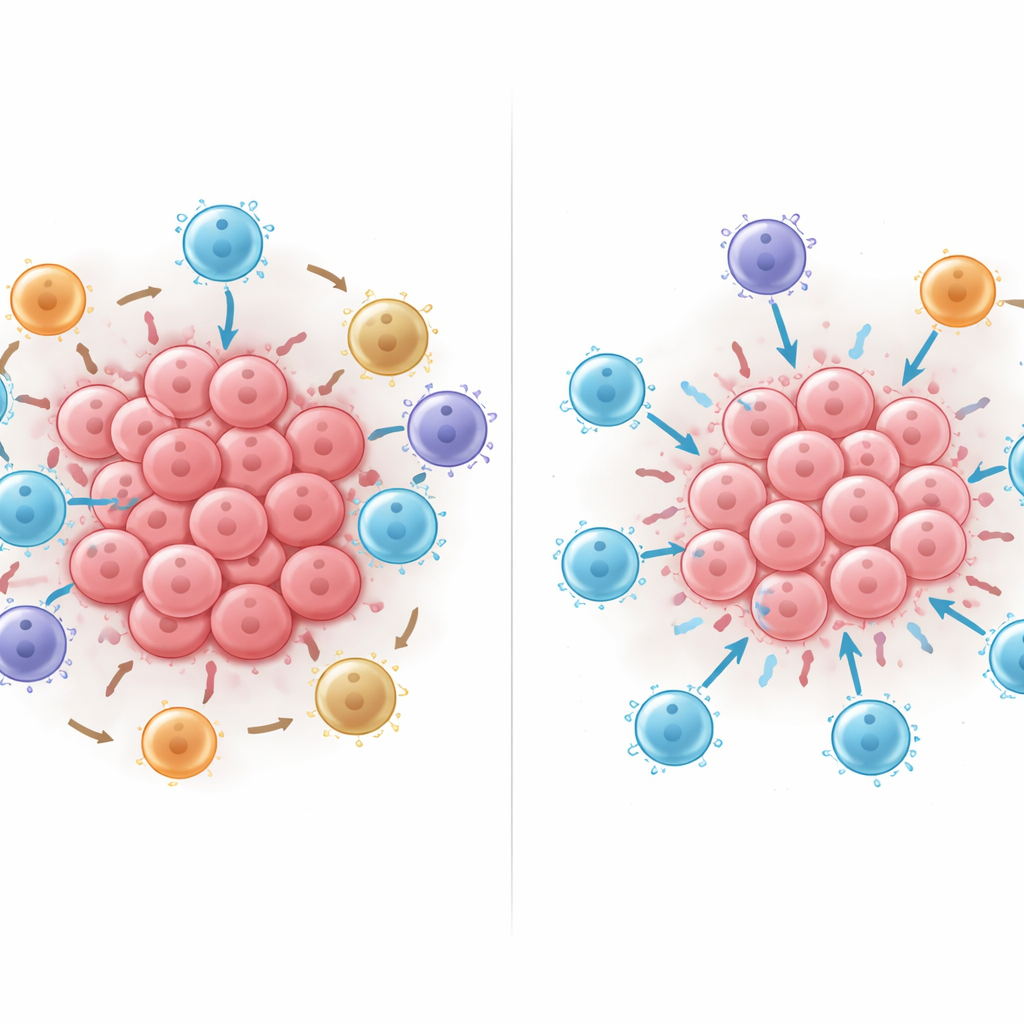
מה קורה כשמורידים ומעבירים את התאים
החוקרים השתמשו אז במודל המאומן כמו מעבדה וירטואלית, והוסיפו דיגיטלית, הסירו או הזיזו תאים בתוך שכונות כדי לראות כיצד הניבוי של השרידות משתנה. הוספת תאי T קטלניים כמעט תמיד שיפרה את התחזית, אך היא הועילה במיוחד כשהתאים היו במגע ישיר עם תאי הגידול ולא מרוחקים. הזזת תאים מדכאים הנושאים PD-L1 או תאי T רגולטוריים FOXP3‑חיוביים למגע קרוב עם תאי T קטלניים הורידה בעקביות את תחזית השרידות של המודל, והנזק גדל ככל שנוצרו קשרים כאלה יותר. ניסויים אלו במרחב הדיגיטלי מצביעים על כך שדפוסי מגע פיזיים — מי נוגע במי — יכולים להטות באופן חמור את המאוזן בין התקפה יעילה על הגידול לדיכוי חיסוני.
כיצד זה עשוי לעצב טיפול עתידי בסרטן
למי שאינו מומחה, המסר המרכזי הוא שלא כל גידול "עם הרבה תאים חיסוניים" זהה. המחקר מראה ששכונות זעירות — לעתים רק כמה עשרות תאים — יכולות לשאת רמזים חזקים לגבי האם המערכת החיסונית מנצחת או מפסידה בקרב המקומי, ורמזים אלה חוזים כיצד המטופלים מסתדרים אפילו לאחר התחשבות בשלב הגידול או בשאלה האם קיבלו אימונותרפיה. על ידי מתן תבנית לקריאת דפוסים מרחביים אלה באמצעות AI מתקדם, העבודה מצביעה לעבר בדיקות בדור הבא שעוברות מעבר לספירת תאים וחושבות כיצד הם מסודרים. ביומרקרים מרחביים כאלה עשויים לעזור לרופאים לזהות טוב יותר אילו מטופלים צפויים להפיק תועלת מטיפולים מבוססי חיסון ואילו עשויים להזדקק לאסטרטגיות משולבות שמפרקות שכונות מזיקות או מחזקות שכונות מועילות.
ציטוט: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
מילות מפתח: סרטן ריאה שאינו תאי זיר, מיקרו‑סביבה של הגידול, רשתות עצביות גרפיות, אימונולוגיה מרחבית, ביומרקרים לאימונותרפיה