Clear Sky Science · it
Modellizzazione con reti neurali a grafo delle interazioni spaziali tumore‑immunitarie identifica nicchie cellulari prognostiche nel carcinoma polmonare non a piccole cellule
Perché il vicinato intorno a un tumore conta
Il cancro polmonare è spesso descritto in termini di geni e farmaci, ma questo studio mostra che anche la disposizione delle cellule l’una accanto all’altra all’interno di un tumore può essere importante quanto la loro identità. Osservando da vicino milioni di singole cellule provenienti da pazienti con carcinoma polmonare non a piccole cellule, i ricercatori hanno usato un approccio di intelligenza artificiale per leggere la “rete sociale” di cellule tumorali e immunitarie. Hanno scoperto che alcuni quartieri cellulari locali sono fortemente correlati con la durata della sopravvivenza dei pazienti, offrendo una strada per previsioni più precise e, potenzialmente, per scelte più mirate di immunoterapia.
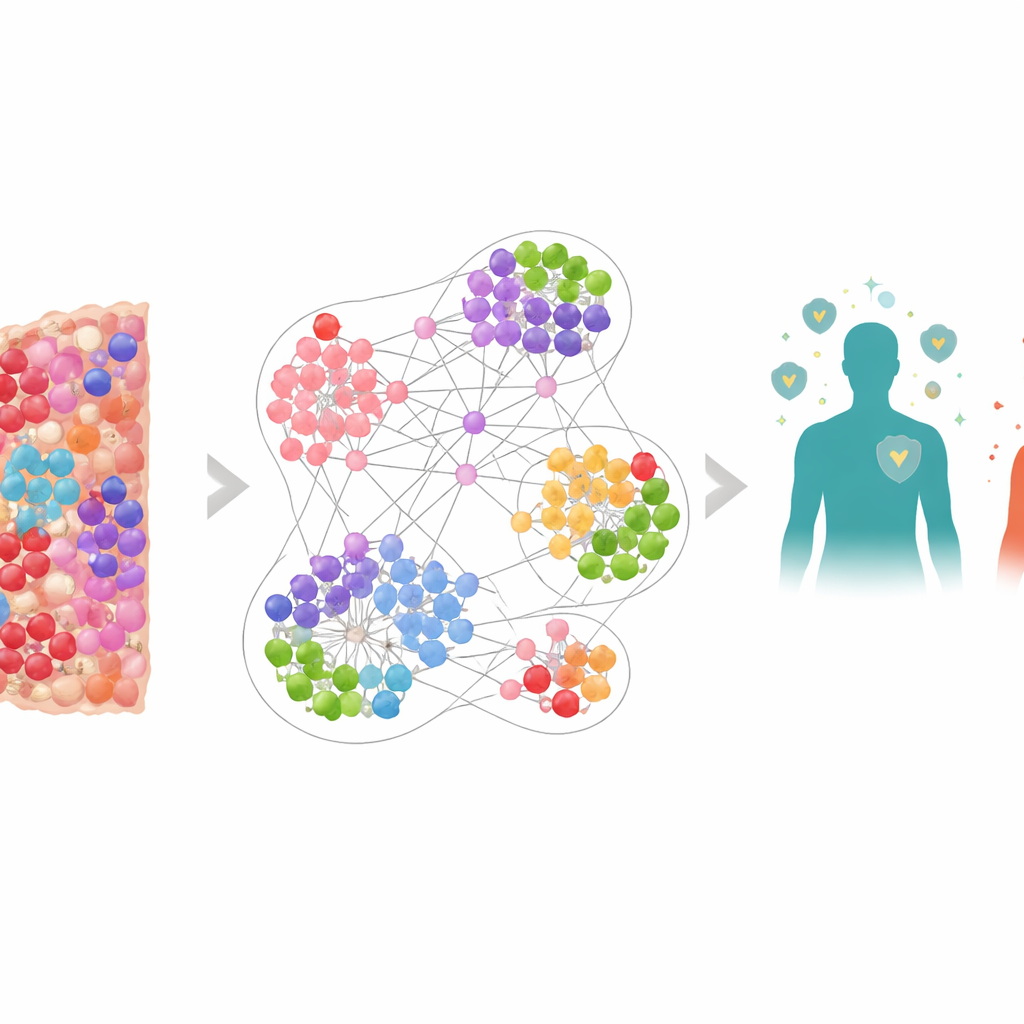
Guardare il cancro come una città viva
Invece di considerare il tumore come una massa uniforme, il gruppo l’ha visto come una città affollata composta da molti residenti diversi: cellule tumorali, cellule immunitarie difensive e cellule soppressive che smorzano l’attacco immunitario. Utilizzando un metodo di imaging speciale che colora più marker contemporaneamente, hanno mappato oltre 6,9 milioni di cellule provenienti da campioni bioptici di 506 pazienti con cancro al polmone. Sono state registrate la posizione e l’identità di ciascuna cellula, compresi attori chiave come le cellule T citotossiche (CD8+), i “freni” immunitari come PD‑1 e PD‑L1, e le cellule T regolatorie marcate da FOXP3. Ne sono nate mappe molto dettagliate del microambiente tumorale, l’ambiente immediato dove tumori e cellule immunitarie interagiscono costantemente.
Trasformare le mappe cellulari in un modello a grafo
Per dare senso a una tale complessità, i ricercatori hanno costruito una rete neurale a grafo, un tipo di IA progettata per lavorare su reti anziché su semplici tabelle di numeri. Nel loro modello, ogni cellula è un nodo e le cellule vicine sono connesse da link, formando molti “grafi di vicinato” sovrapposti intorno a ciascuna cellula. La rete è stata addestrata a riconoscere quali tipi di vicinato locale tendevano a comparire nei pazienti con sopravvivenze più lunghe rispetto a quelle più brevi. Quando le previsioni a livello di vicinato del modello sono state aggregate a livello di paziente, la previsione di sopravvivenza è risultata molto accurata, superando misure più semplici come il numero complessivo di cellule T citotossiche o modelli che conoscevano solo la posizione delle cellule ma non ciò che esprimevano.
Quartieri buoni e cattivi all’interno del tumore
Analizzando ciò che l’IA aveva appreso, il gruppo ha identificato tipi distinti di vicinati locali con implicazioni molto diverse per la sopravvivenza. I vicinati ricchi di cellule T citotossiche, specialmente quando anche le cellule tumorali esprimevano marker di attivazione immunitaria, erano generalmente associati a esiti migliori. Ma non tutte le aree affollate di cellule immunitarie erano benefiche. Alcuni vicinati mescolavano molte cellule T citotossiche con alti livelli di PD‑L1 su cellule tumorali o su cellule immunitarie vicine, segnalando una forte “spegnimento” immunitario e peggiori prospettive di sopravvivenza. Altri vicinati erano più simili a deserti immunitari, dominati da cellule tumorali con pochissimi difensori, e anche questi risultavano associati a esiti sfavorevoli. Clusterizzando questi modelli, lo studio ha definito diversi “stati” tumorali ricorrenti che bilanciano attacco immunitario e fuga immunitaria.
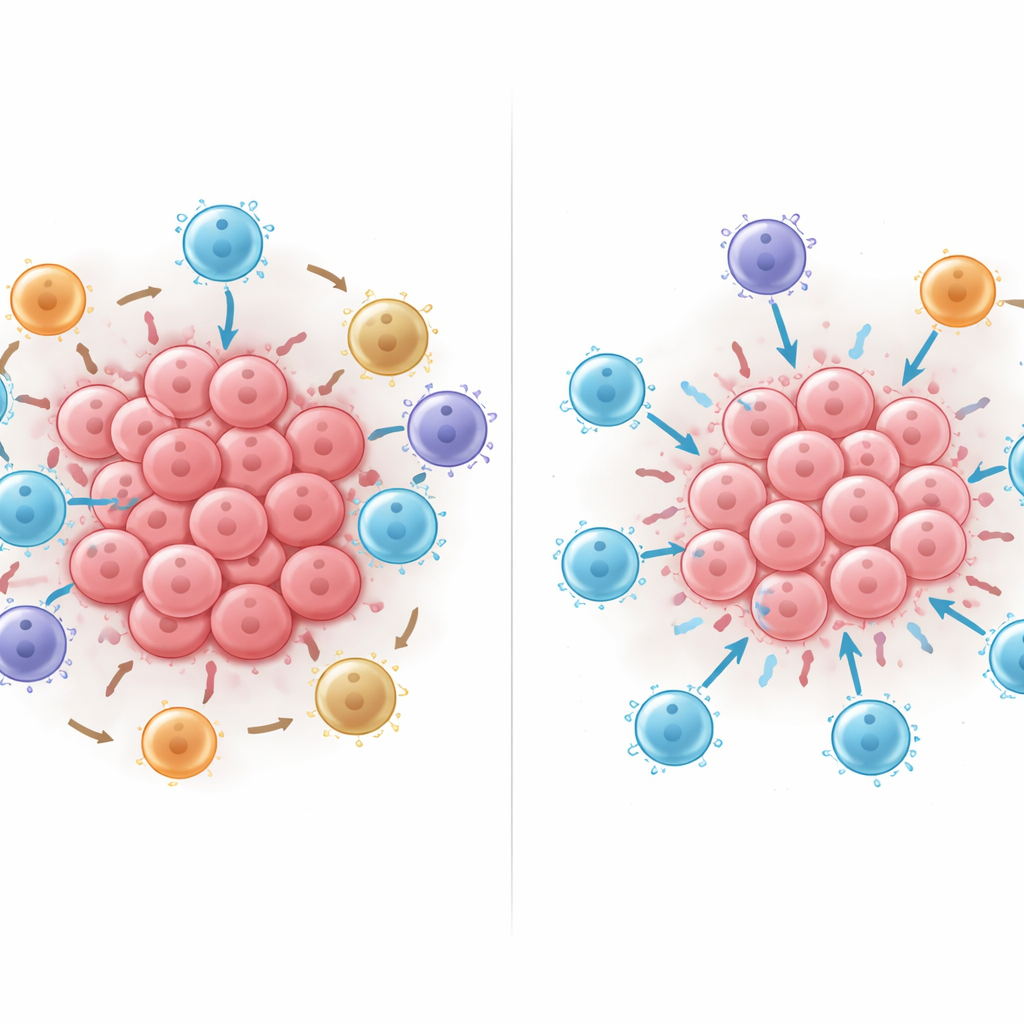
Cosa succede quando si riorganizzano le cellule
I ricercatori hanno poi usato il modello IA addestrato come un laboratorio virtuale, aggiungendo, rimuovendo o spostando digitalmente cellule all’interno dei vicinati per osservare come cambiava la sopravvivenza prevista. Aggiungere cellule T citotossiche quasi sempre aiutava, ma il beneficio era massimo quando queste cellule erano in contatto diretto con le cellule tumorali anziché tenute a distanza. Spostare cellule immunitarie soppressive PD‑L1‑positive o cellule T regolatorie FOXP3‑positive in stretto contatto con le cellule T citotossiche riduceva sistematicamente la previsione di sopravvivenza del modello, e il danno aumentava all’aumentare dei contatti di questo tipo. Questi esperimenti in silico suggeriscono che i pattern di contatto fisico — chi tocca chi — possono spostare nettamente l’equilibrio tra un attacco tumorale efficace e la soppressione immunitaria.
Come questo potrebbe influenzare la cura del cancro in futuro
Per un lettore non specialista, il messaggio chiave è che non tutti i tumori con “molte cellule immunitarie” sono uguali. Questo studio dimostra che minuscoli vicinati — spesso poche dozzine di cellule — possono contenere segnali potenti su se il sistema immunitario stia vincendo o perdendo la battaglia locale, e questi segnali predicono l’andamento dei pazienti anche tenendo conto dello stadio tumorale o del fatto che abbiano ricevuto immunoterapia. Fornendo una mappa per leggere questi pattern spaziali con IA avanzata, il lavoro indica la direzione per test di nuova generazione che vadano oltre il semplice conteggio cellulare e misurino come le cellule sono disposte. Tali biomarcatori spaziali potrebbero aiutare i medici a identificare meglio quali pazienti trarranno beneficio dai trattamenti immunitari e quali potrebbero necessitare di strategie combinate per interrompere i vicinati cellulari dannosi o potenziare quelli utili.
Citazione: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Parole chiave: carcinoma polmonare non a piccole cellule, microambiente tumorale, reti neurali a grafo, immunologia spaziale, biomarcatori per immunoterapia