Clear Sky Science · de
Graph-Neuronales-Netzwerk-Modellieren räumlicher Tumor-Immun-Wechselwirkungen identifiziert prognostische zelluläre Nischen beim nicht‑kleinzelligen Lungenkrebs
Warum die Nachbarschaft um einen Tumor wichtig ist
Lungenkrebs wird oft über Gene und Medikamente beschrieben, doch diese Studie zeigt, dass die räumliche Anordnung von Zellen nebeneinander in einem Tumor genauso wichtig sein kann wie ihre Identität. Indem sie Millionen einzelner Zellen von Patientinnen und Patienten mit nicht‑kleinzelligem Lungenkrebs heranzoomen, nutzten die Forschenden einen KI‑Ansatz, um das „soziale Netzwerk“ von Tumor‑ und Immunzellen zu entschlüsseln. Sie fanden heraus, dass bestimmte lokale Zell‑Nachbarschaften stark mit der Überlebenszeit der Patienten verknüpft sind, was genauere Vorhersagen und möglicherweise intelligentere Entscheidungen bei der Immuntherapie ermöglicht.
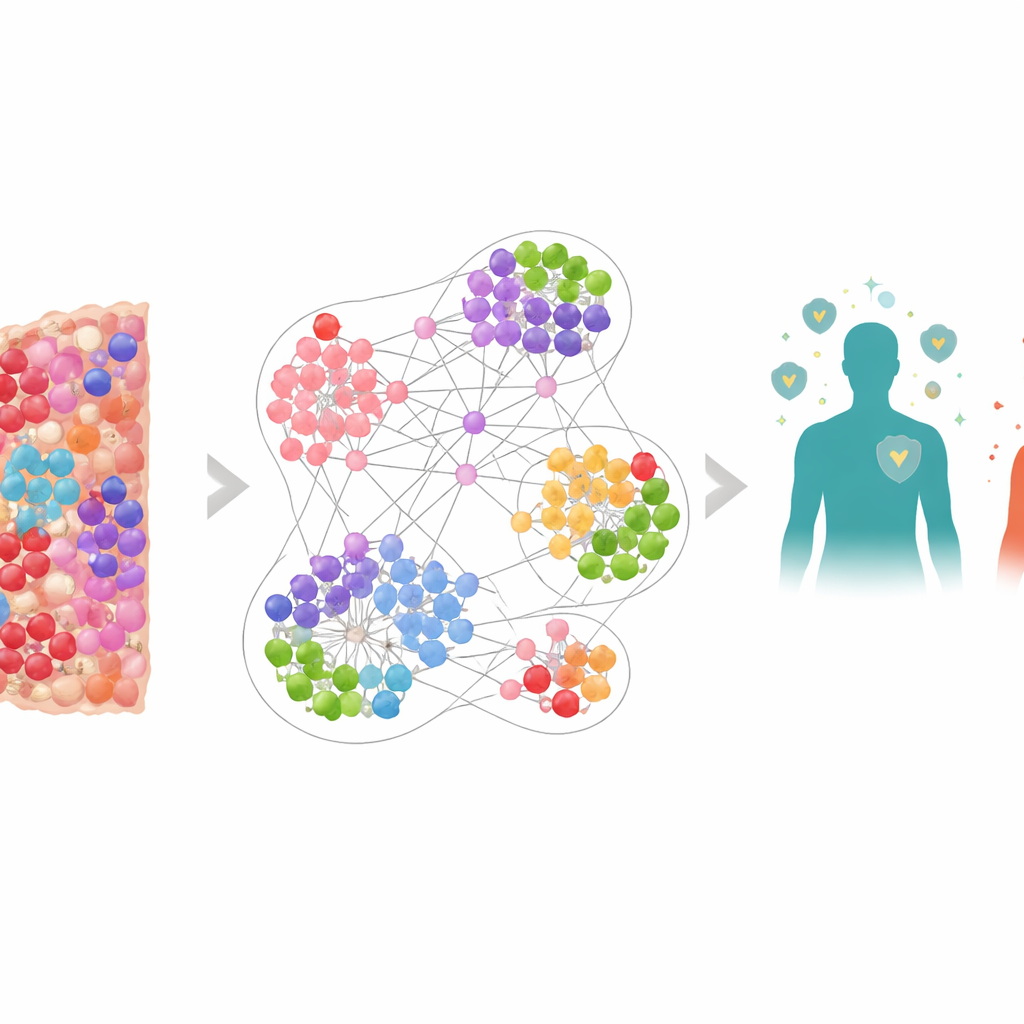
Krebs als lebendige Stadt betrachten
Anstatt einen Tumor als einheitliche Masse zu sehen, betrachtete das Team ihn als eine überfüllte Stadt mit vielen verschiedenen Einwohnern: Krebszellen, verteidigende Immunzellen und dämpfende Zellen, die den Immunangriff abschwächen. Mithilfe einer speziellen Bildgebung, die mehrere Marker gleichzeitig anfärbt, kartierten sie über 6,9 Millionen Zellen aus Biopsien von 506 Lungenkrebspatienten. Position und Identität jeder Zelle wurden erfasst, einschließlich wichtiger Akteure wie Killer‑T‑Zellen (CD8+), Immun‑„Bremsen“ wie PD‑1 und PD‑L1 sowie regulatorischer T‑Zellen, markiert durch FOXP3. So entstanden hochdetaillierte Karten der Tumormikroumgebung, also der direkten Umgebung, in der Tumor- und Immunzellen ständig interagieren.
Zellkarten in ein Netzwerkmodell verwandeln
Um diese Komplexität verständlich zu machen, bauten die Forschenden ein graph‑neuronales Netzwerk, eine Form der KI, die für Netzwerke statt einfache Zahlentabellen entwickelt wurde. In ihrem Modell ist jede Zelle ein Knoten und benachbarte Zellen sind durch Verbindungen gekoppelt, wodurch sich viele überlappende „Nachbarschaftsgraphen“ um jede Zelle bilden. Das Netzwerk wurde trainiert zu erkennen, welche Arten von lokalen Nachbarschaften bei Patientinnen und Patienten mit längerer beziehungsweise kürzerer Lebenszeit häufiger vorkommen. Wenn die vorhersagen auf Nachbarschaftsebene zu Patientenwerten gemittelt wurden, sagte das Modell das Überleben sehr genau voraus und übertraf einfachere Maße wie die Gesamtzahl an Killer‑T‑Zellen oder Modelle, die nur wussten, wo Zellen waren, aber nicht, welche Marker sie exprimierten.
Gute und schlechte Nachbarschaften im Tumor
Durch die Analyse dessen, was die KI gelernt hatte, identifizierte das Team verschiedene Typen lokaler Nachbarschaften mit sehr unterschiedlichen Folgen für das Überleben. Nachbarschaften, die reich an Killer‑T‑Zellen waren, insbesondere wenn Tumorzellen auch Marker für Immunaktivierung zeigten, standen allgemein für bessere Prognosen. Aber nicht alle immundichten Bereiche waren vorteilhaft. Manche Mischungen aus vielen Killer‑T‑Zellen mit hohen PD‑L1‑Werten auf Tumor‑ oder benachbarten Immunzellen signalisierten eine starke Immunabschaltung und schlechteres Überleben. Andere Regionen glichen immunen Wüsten, dominiert von Tumorzellen mit sehr wenigen Verteidigern, und auch diese waren mit schlechten Ergebnissen verbunden. Durch Clusterbildung dieser Muster definierte die Studie mehrere wiederkehrende Tumor‑„Zustände“, die das Gleichgewicht zwischen Immunangriff und Immunflucht widerspiegeln.
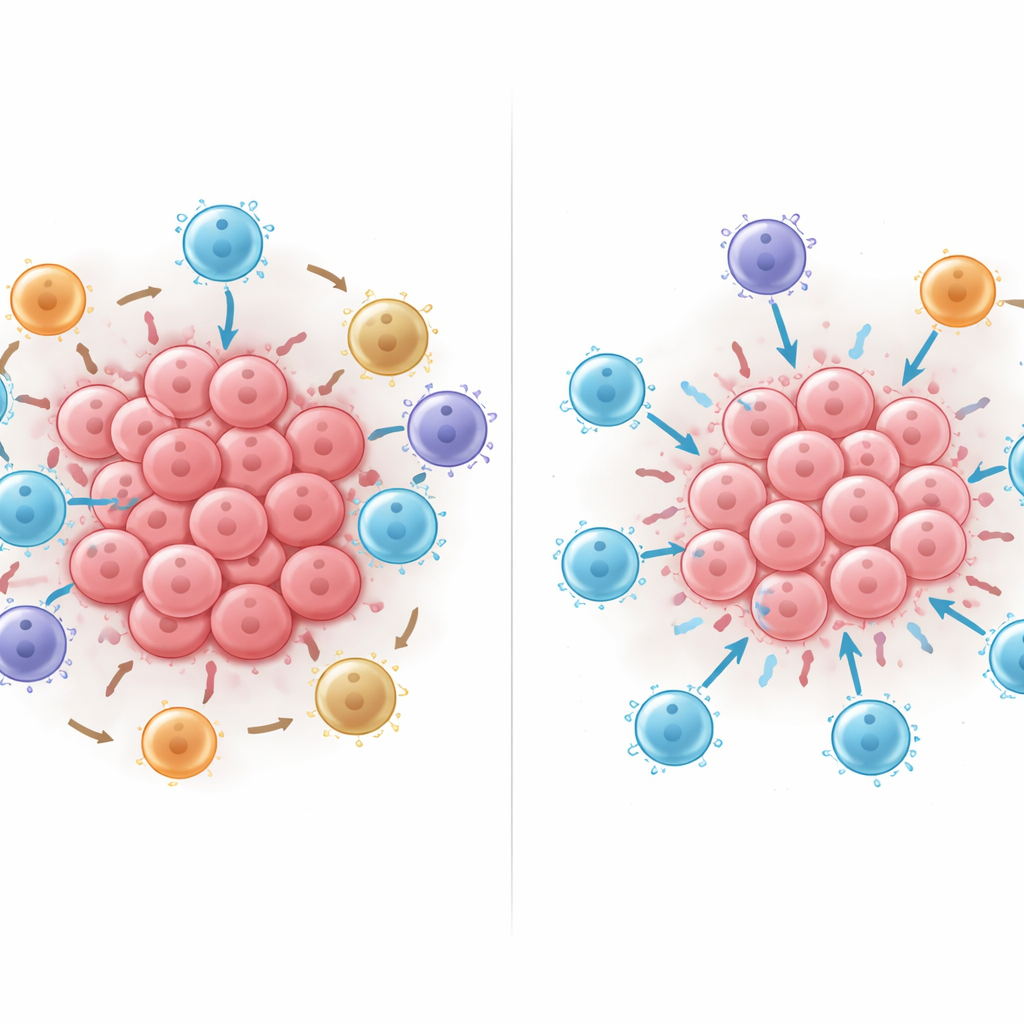
Was passiert, wenn man die Zellen umordnet
Die Forschenden nutzten das trainierte KI‑Modell anschließend wie ein virtuelles Labor, indem sie innerhalb von Nachbarschaften digital Zellen hinzufügten, entfernten oder verschoben, um zu sehen, wie sich die vorhergesagte Überlebensprognose änderte. Das Hinzufügen von Killer‑T‑Zellen half fast immer, am stärksten jedoch, wenn diese Zellen in direktem Kontakt mit Tumorzellen standen, statt auf Distanz gehalten zu werden. Das Verschieben unterdrückender PD‑L1‑positiver Immunzellen oder FOXP3‑positiver regulatorischer T‑Zellen in engen Kontakt mit Killer‑T‑Zellen verringerte konsistent die Überlebensvorhersage des Modells, und der Schaden nahm zu, je mehr solche Kontakte entstanden. Diese In‑silico‑Experimente deuten darauf hin, dass physische Kontaktmuster — wer wen berührt — das Gleichgewicht zwischen effektivem Tumorangriff und Immunsuppression stark beeinflussen können.
Wie das die künftige Krebsversorgung beeinflussen könnte
Für Laien ist die Kernbotschaft: Nicht alle Tumoren mit „vielen Immunzellen“ sind gleich. Diese Studie zeigt, dass winzige Nachbarschaften — oft nur einige Dutzend Zellen — kraftvolle Signale darüber tragen können, ob das Immunsystem die lokale Auseinandersetzung gewinnt oder verliert, und diese Signale sagen das Patientenoutcome voraus, selbst wenn Tumorstadium oder der Erhalt einer Immuntherapie berücksichtigt werden. Indem sie eine Blaupause liefern, wie diese räumlichen Muster mit fortgeschrittener KI gelesen werden können, weist die Arbeit auf nächste‑Generation‑Tests hin, die über das Zählen von Zellen hinausgehen und deren Anordnung messen. Solche räumlichen Biomarker könnten Ärzten helfen, besser zu erkennen, welche Patienten wahrscheinlich von immunbasierten Therapien profitieren und welche Kombinationen erforderlich sein könnten, um schädliche Zellnachbarschaften zu stören oder förderliche zu stärken.
Zitation: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Schlüsselwörter: nicht‑kleinzelliger Lungenkrebs, Tumormikroumgebung, graph neuronale Netze, räumliche Immunologie, Biomarker für Immuntherapie