Clear Sky Science · fr
Modélisation par réseaux de neurones graphiques des interactions tumorales‑immunes spatiales identifie des niches cellulaires pronostiques dans le cancer du poumon non à petites cellules
Pourquoi le voisinage autour d’une tumeur compte
Le cancer du poumon est souvent décrit en termes de gènes et de médicaments, mais cette étude montre que la manière dont les cellules sont disposées les unes par rapport aux autres à l’intérieur d’une tumeur peut être tout aussi importante que leur identité. En zoomant sur des millions de cellules individuelles provenant de patients atteints de cancer du poumon non à petites cellules, les chercheurs ont utilisé une approche d’intelligence artificielle pour lire le « réseau social » des cellules tumorales et immunitaires. Ils ont constaté que certains micro‑voisinages cellulaires sont fortement associés à la durée de survie des patients, ouvrant la voie à des prédictions plus précises et, potentiellement, à des choix d’immunothérapie plus pertinents.
Regarder le cancer comme une ville vivante
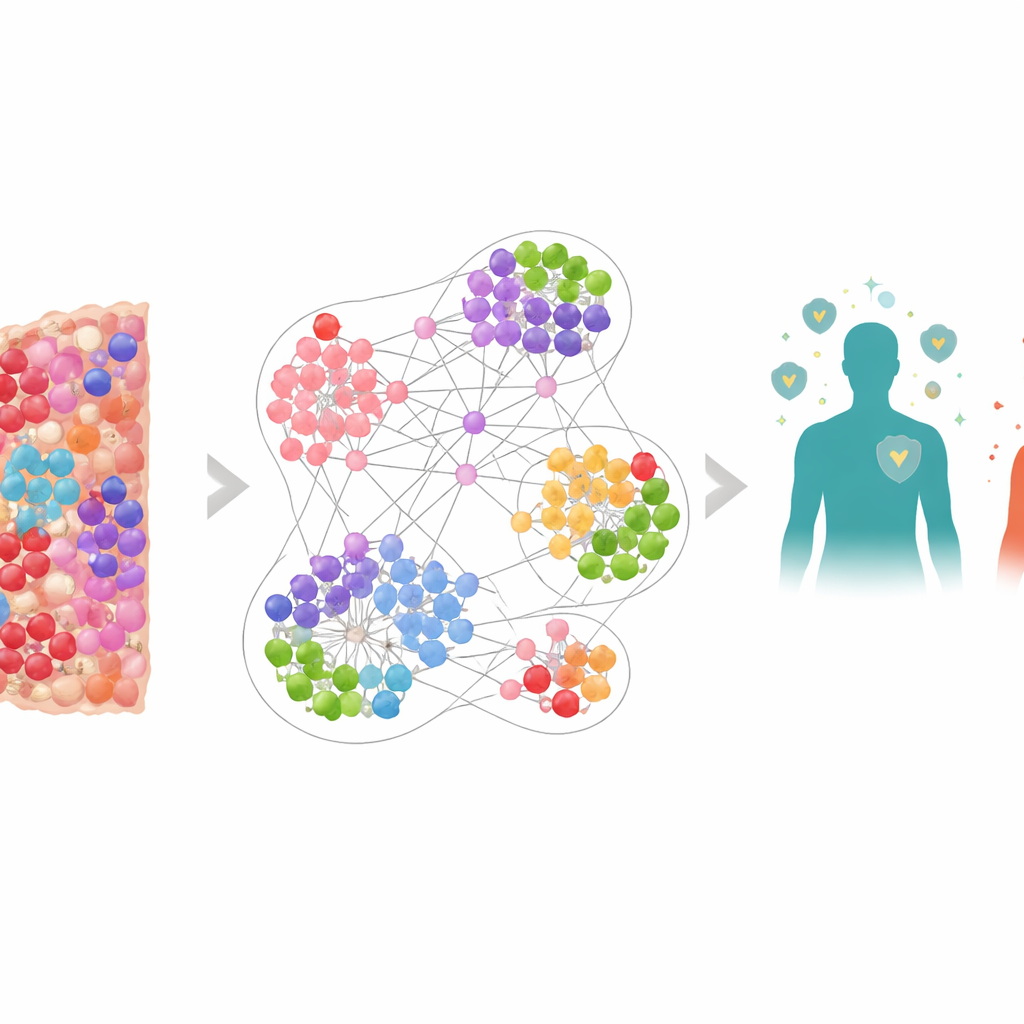
Plutôt que de considérer la tumeur comme une masse homogène, l’équipe l’a envisagée comme une ville dense composée de nombreux habitants différents : cellules cancéreuses, cellules immunitaires défensives et cellules suppresseuses qui atténuent l’attaque immunitaire. Grâce à une méthode d’imagerie spéciale marquant simultanément plusieurs marqueurs, ils ont cartographié plus de 6,9 millions de cellules issues de prélèvements biopsiques de 506 patients atteints de cancer du poumon. La position et l’identité de chaque cellule ont été enregistrées, incluant des acteurs clés comme les lymphocytes T cytotoxiques (CD8+), des « freins » immunitaires tels que PD‑1 et PD‑L1, et les cellules T régulatrices marquées par FOXP3. Cela a produit des cartes très détaillées du microenvironnement tumoral, l’environnement immédiat où tumeurs et cellules immunitaires interagissent en permanence.
Transformer les cartes cellulaires en modèle de réseau
Pour interpréter une telle complexité, les chercheurs ont construit un réseau de neurones graphique, un type d’IA conçu pour travailler sur des réseaux plutôt que sur de simples tableaux de nombres. Dans leur modèle, chaque cellule est un nœud et les cellules voisines sont reliées par des liens, formant de nombreux « graphes de voisinage » chevauchants autour de chaque cellule. Le réseau a été entraîné à reconnaître quels types de voisinages locaux avaient tendance à apparaître chez les patients ayant une plus longue survie versus une survie plus courte. Lorsque les prédictions au niveau des voisinages ont été moyennées au niveau du patient, le modèle a prédit la survie très précisément, surpassant des mesures plus simples comme le nombre total de lymphocytes T cytotoxiques ou des modèles ne connaissant que la position des cellules sans leurs marqueurs d’expression.
Bons et mauvais quartiers à l’intérieur de la tumeur
En disséquant ce que l’IA avait appris, l’équipe a identifié des types distincts de voisinages locaux avec des implications très différentes pour la survie. Les voisinages riches en lymphocytes T cytotoxiques, en particulier lorsque les cellules tumorales exprimaient aussi des marqueurs d’activation immunitaire, étaient généralement associés à de meilleurs résultats. Mais toutes les zones peuplées d’immunitaires n’étaient pas bénéfiques. Certains voisinages combinaient de nombreux lymphocytes T cytotoxiques avec des niveaux élevés de PD‑L1 sur les cellules tumorales ou les cellules immunitaires avoisinantes, signe d’une forte « mise en veille » immunitaire et d’une survie plus mauvaise. D’autres voisinages ressemblaient davantage à des déserts immunitaires, dominés par des cellules tumorales avec très peu de défenseurs, et ceux‑ci étaient également liés à de mauvais pronostics. En regroupant ces configurations, l’étude a défini plusieurs « états » tumoraux récurrents qui reflètent l’équilibre entre attaque immunitaire et évasion immunitaire.
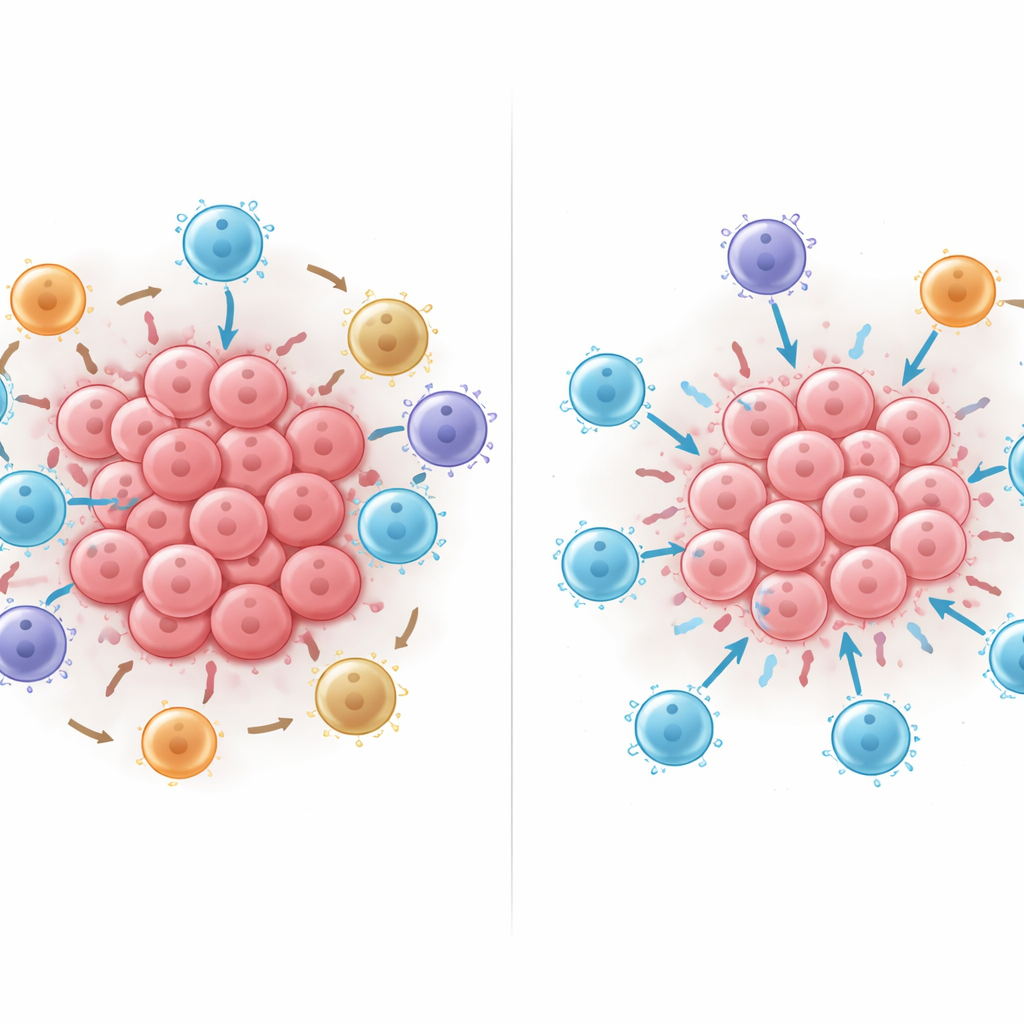
Que se passe‑t‑il lorsqu’on réorganise les cellules
Les chercheurs ont ensuite utilisé le modèle d’IA entraîné comme un laboratoire virtuel, ajoutant, retirant ou déplaçant numériquement des cellules au sein des voisinages pour observer comment la survie prédite évoluait. L’ajout de lymphocytes T cytotoxiques aidait presque toujours, mais c’était le plus bénéfique lorsque ces cellules étaient en contact direct avec les cellules tumorales plutôt qu’à distance. Le fait de rapprocher des cellules immunitaires suppressives positives pour PD‑L1 ou des cellules T régulatrices FOXP3‑positives des lymphocytes T cytotoxiques réduisait systématiquement la prédiction de survie du modèle, et le dommage augmentait au fur et à mesure que ces contacts se multipliaient. Ces expériences in silico suggèrent que les schémas de contact physique — qui touche qui — peuvent faire basculer nettement l’équilibre entre une attaque tumorale efficace et la suppression immunitaire.
Comment cela pourrait orienter les soins du cancer à l’avenir
Pour un non‑spécialiste, le message clé est que toutes les tumeurs contenant « beaucoup de cellules immunitaires » ne se valent pas. Cette étude montre que de petits voisinages — souvent seulement quelques dizaines de cellules — peuvent porter des signaux puissants sur la victoire ou la défaite locale du système immunitaire, et ces signaux prédisent l’issue des patients même en tenant compte du stade tumoral ou de la réception d’une immunothérapie. En fournissant une feuille de route pour lire ces motifs spatiaux avec une IA avancée, le travail ouvre la voie à des tests de nouvelle génération qui dépassent le simple comptage de cellules pour mesurer leur organisation. De tels biomarqueurs spatiaux pourraient aider les médecins à mieux identifier quels patients sont susceptibles de bénéficier des traitements à base d’immunothérapie et lesquels pourraient nécessiter des stratégies combinatoires visant à perturber les voisinages cellulaires nuisibles ou à renforcer les voisinages protecteurs.
Citation: Hoebel, K.V., Lindsay, J.R., Altreuter, J. et al. Graph neural network modeling of spatial tumor-immune interactions identifies prognostic cellular niches in non‑small cell lung cancer. npj Precis. Onc. 10, 158 (2026). https://doi.org/10.1038/s41698-026-01314-3
Mots-clés: cancer du poumon non à petites cellules, microenvironnement tumoral, réseaux de neurones graphiques, immunologie spatiale, biomarqueurs d’immunothérapie