Clear Sky Science · tr
Şeker taşınması için iki aşamalı bir mekanizma
Hücreler Doğru Şekeri Nasıl Seçer
Vücudunuzdaki her hücre, özellikle beyin ve tümör gibi hızla büyüyen dokular, enerji için sürekli bir şeker kaynağına bağımlıdır. Bu şeker yağlı hücre zarını geçmek zorundadır ve bunu taşıyıcı adı verilen özelleşmiş “kapılar” aracılığıyla yapar. Bu makale, benzer birçok şekerin bulunduğu durumda bir taşıyıcının hangilerini geçirip hangilerini engelleyeceğini nasıl belirlediğine dair görünüşte basit ama tıbbi sonuçları büyük olan bir soruyu inceliyor. Cevap, şeker ile proteinin ilk temasında değil, zarın derinliklerinde gerçekleşen ince bir iki aşamalı dansta yatıyor. 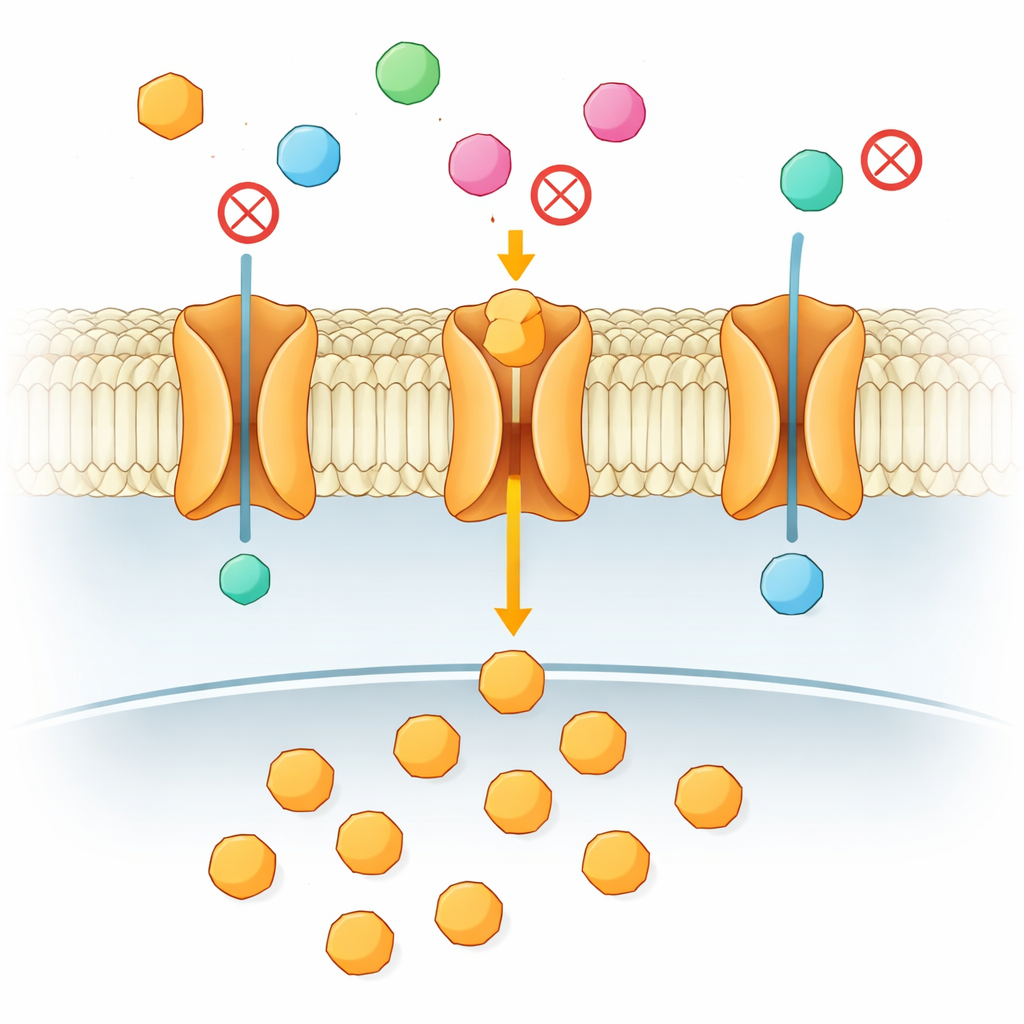
Benzer Şekerlerin Neden Çok Farklı Davrandığı
İnsanlarda, şekerin gerçekten bağlandığı bölgede şaşırtıcı derecede benzer görünen 14 yakın ilişkili glukoz taşıyıcısı vardır. Yine de farklı şekerleri farklı hızlarda taşırlar ve diyabetten kanserlere kadar çeşitli durumlarla ilişkilidirler. Bu bilmecenin çözümü için yazarlar, insan taşıyıcılarının bakteriyel bir kuzeni olan XylE adlı bir proteine yöneldiler. XylE, ksilozu taşır ama glukozu neredeyse aynı güçte bağlar; oysa glukoz geçemez ve kapıyı tıkar. Bu garip davranış, XylE’yi gerçekten taşınan bir şekeri sistemi tıkayan bir şekerden ayıranın ne olduğunu sormak için ideal bir model yapıyor.
Manyetik Rezonansla Şekerleri Dinlemek
Araştırma ekibi, doyurma transfer farkı (STD) NMR olarak bilinen bir manyetik rezonans yöntemini şeker–taşıyıcı karşılaşmaları için bir tür “steteskop” olarak kullandı. Saflaştırılmış taşıyıcıları, doğal ortamı taklit eden küçük yapay zarlar olan lipozomlara yeniden yerleştirdiler. STD NMR’de, proteinin yakınında yeterince uzun süre kalan sadece şeker molekülleri algılanabilir bir sinyal alır. Şaşırtıcı bulgu, XylE’nin doğal yükü olan ksiloz ile güçlü sinyaller ürettiği, fakat her iki şeker de bağlansa bile glukozla neredeyse hiç sinyal alınmadığıydı. Araştırmacılar XylE’yi genetik olarak kilitleyip artık şekil değiştiremeyecek ve taşımacılık yapamayacak hale getirdiklerinde, ksiloz sinyali neredeyse tamamen kayboldu. Tersine, XylE’yi glukozu taşıyabilme yeteneği kazandıracak şekilde tasarladıklarında güçlü glukoz sinyalleri belirdi. Başka bir deyişle, bu deneyde zarın diğer tarafına gerçekten ulaşan şeker–taşıyıcı çiftleri ışık veriyor.
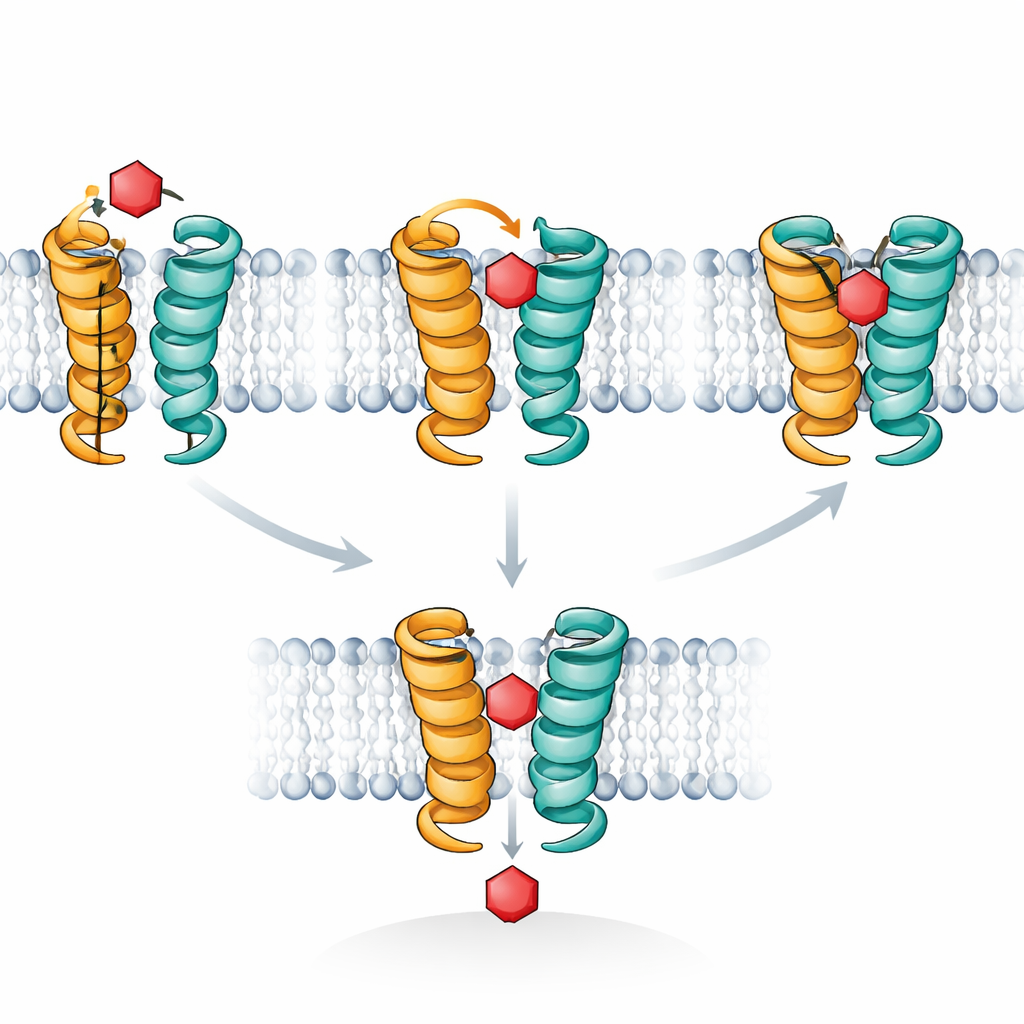
Yolculukta Gizli Bir Ara Adım
Bilgisayar simülasyonları bu gözlemleri açıklayan moleküler bir film sundu. XylE, insan glukoz taşıyıcıları gibi, hücrenin dışına ve içine sırasıyla açılan şekiller arasında döner; arada şekerin her iki taraftan da izole edildiği "oksüle" (occluded) bir ara durum vardır. Yazarlar, dış kapı gibi iş gören kısa bir heliks segmenti olan TM7b'ye odaklandılar. Simülasyonları, ksiloz doğru pozisyonda oturduğunda TM7b'nin tamamen kapanabileceğini ve şekerin sıkıca sarıldığı derin oksüle durumu stabilize ettiğini gösterdi. Buna karşılık glukoz sallanma eğiliminde olup TM7b'yi bu kapanmayı tamamlamaya sürekli olarak yönlendiremez; o, yolu bitirmeden engelleyen daha sığ, dışa-oksüle bir pozda sıkışmış kalır. STD NMR sinyalleri tam olarak şekerlerin tamamen oksüle, yüksek temaslı konfigürasyonda ne kadar uzun süre kaldığındaki farkı izliyor.
Sıtma Taşıyıcısı ve Bir Fruktoz Uzmanından Dersler
Bu ilkenin XylE ile sınırlı olup olmadığını görmek için araştırmacılar, hem glukozu hem fruktozu taşıyabilen sıtma paraziti taşıyıcısı PfHT1'e ve bağırsaktaki fruktoz uzmanı olan memeli GLUT5'e baktılar. STD NMR, kristal yapılar, kriyo-elektron mikroskopya ve ilave simülasyonlar kullanarak bu taşıyıcıların da oksüle adımı sırasında şekerleri koordine etmek için TM7b'ye güvendiğini buldular. TM7b'deki tek bir asparagin amino asidi merkezi bir rol oynuyor; kapı kapanırken şeker halkasındaki kilit hidroksil gruplarıyla temas kuruyor. PfHT1'de yüksek çözünürlüklü bir kriyo-EM görüntüsü, şekerin yalnızca kısmen koordine edildiği "yarı yol" içe-oksüle bir pozu yakaladı; daha önce belirlenmiş bir kristal yapı ise tam oksüle pozu yakalamıştı. İkisini karşılaştırmak, şekerin yalnızca yaklaşık iki milyarıncı metre kadar kaydığını ama geçiş durumuna benzeyen oksüle formda çok daha sıkı bağlanmayı sağlayan ek temas ağını kazandığını gösterdi.
Taşıyıcılar Küçük Enzimler Gibidir
Tüm kanıtları birleştirerek yazarlar, şeker taşıyıcılarının özgüllüğünün ilk bağlanma adımıyla değil geçici bir geçiş durumuna ne kadar iyi uyduklarıyla yönetildiği sonucuna varıyorlar; yani taşıyıcılar küçük enzimler gibi çalışıyor. Taşıyıcılar, şeker olmadan bile dışa ve içe-oksüle şekillere kendiliğinden geçiş yapar. Uyumlu bir şeker önce bu önceden var olan pozlardan birini "seçer" (konformasyonel seçim), sonra kapının tam oksüle duruma sıkılaşmasını tetikleyerek proteinin diğer tarafa çevrilip şekeri salmasına karar verdirir (indüklenmiş uyum). Uyumsuz şekerler yine bağlanabilir, bazen güçlü şekilde, ama bu son sıkılaşma adımını tetikleyemezler; bu nedenle yük yerine inhibitör gibi davranırlar. Oksüle durumun gerçek karar noktası olduğunu kabul etmek, taşıyıcıları geçişe benzeyen bir poztan donduracak ilaçlar tasarlamak için yeni yollar öneriyor; bu da kanser hücrelerini veya parazitleri şekere erişimlerini engelleyerek adeta aç bırakma potansiyeline sahip olabilir.
Atıf: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Anahtar kelimeler: glukoz taşıyıcıları, şeker taşınması, zar proteinleri, STD NMR, geçiş durumu özgüllüğü