Clear Sky Science · nl
Een twee-stappenmechanisme voor suikerverplaatsing
Hoe cellen de juiste suiker kiezen
Elke cel in je lichaam is afhankelijk van een constante aanvoer van suiker voor energie, vooral de hersenen en snelgroeiende weefsels zoals tumoren. Die suiker moet een vette celmembraan oversteken, en doet dat via gespecialiseerde "poorten" die transporters worden genoemd. Dit artikel onderzoekt een bedrieglijk eenvoudige vraag met grote medische implicaties: wanneer veel vergelijkbare suikers aanwezig zijn, hoe beslist een transporter welke suikers door mogen en welke worden tegengehouden? Het antwoord blijkt niet te liggen in het eerste contact tussen suiker en eiwit, maar in een subtiele twee-stappen-dans diep in het membraan. 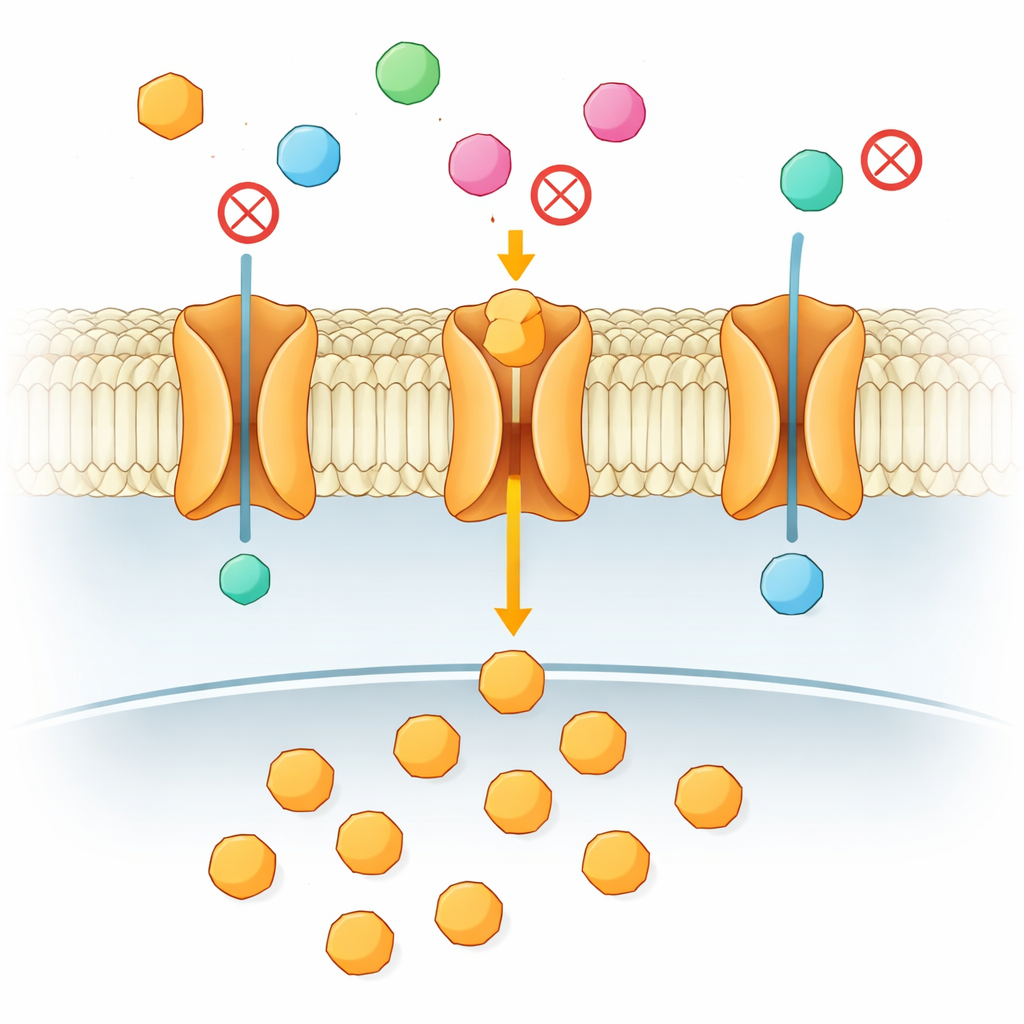
Waarom vergelijkbare suikers zich zo verschillend gedragen
Bij mensen zijn er 14 nauw verwante glucosetransporters die er opvallend hetzelfde uitzien op de plek waar de suiker daadwerkelijk bindt. Toch verplaatsen ze verschillende suikers met verschillende snelheden en zijn ze gelinkt aan aandoeningen variërend van diabetes tot kanker. Om deze puzzel te ontwarren, richtten de auteurs zich op een bacteriële verwant van menselijke transporters, een eiwit dat XylE heet. XylE vervoert de suiker xylose maar bindt glucose met bijna dezelfde sterkte, hoewel glucose niet kan passeren en in plaats daarvan de poort verstopt. Dat vreemde gedrag maakt XylE tot een ideaal model om te vragen wat een getransporteerde suiker werkelijk onderscheidt van een die het systeem alleen maar blokkeert.
Suikers beluisteren met magnetische resonantie
Het team gebruikte een magnetische resonantiemethode bekend als saturation transfer difference (STD) NMR als een soort "stethoscoop" voor suiker–transporterontmoetingen. Ze reconstrueerden gezuiverde transporters in kleine kunstmatige membranen, liposomen genoemd, die de natuurlijke omgeving nabootsen. In STD NMR nemen alleen suikermoleculen die lang genoeg in de buurt van het eiwit blijven een detecteerbaar signaal op. De verrassende bevinding was dat XylE sterke signalen produceerde met xylose, zijn natuurlijke lading, maar bijna geen met glucose, hoewel beide suikers binden. Toen de onderzoekers XylE genetisch vastzetten zodat het zijn vorm niet meer kon veranderen en niet meer kon transporteren, verdween het xylose-signaal vrijwel helemaal. Omgekeerd, toen ze XylE zo ontwierpen dat het glucose kon verplaatsen, verschenen er sterke glucose-signalen. Met andere woorden: alleen suiker–transporterparen die daadwerkelijk de reis door het membraan voltooien lichten op in dit experiment. 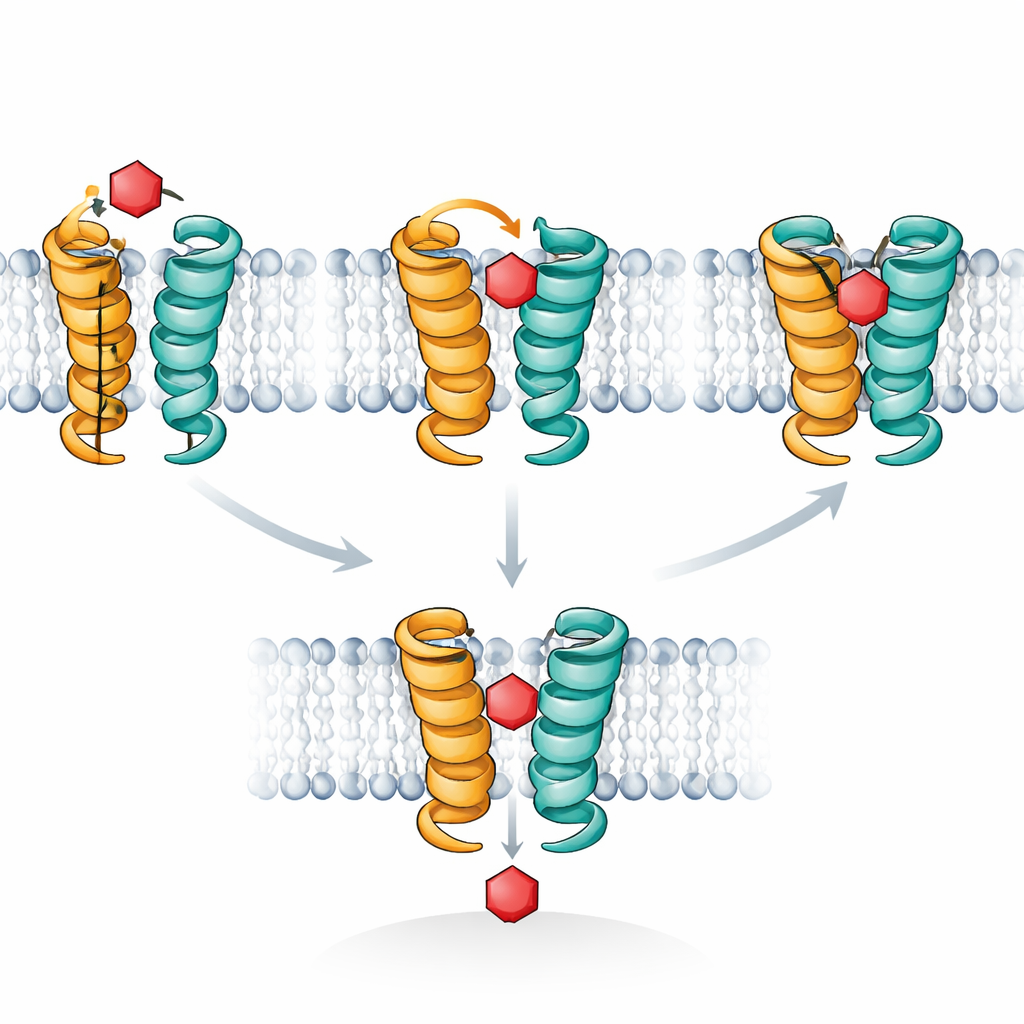
Een verborgen tussentap in de reis
Computersimulaties leverden een moleculaire film om deze observaties te verklaren. XylE, net als menselijke glucosetransporters, werkt door te cykelen tussen vormen die afwisselend naar buiten en naar binnen openen, met een tussenliggende "geoccludeerde" toestand waarin de suiker van beide zijden afgesloten is. De auteurs concentreerden zich op een kort helixsegment, TM7b genoemd, dat fungeert als een buitendeur. Hun simulaties toonden dat wanneer xylose in precies de juiste pose zit, TM7b volledig kan dichtklappen en zo de diep geoccludeerde toestand stabiliseert waarin de suiker stevig wordt omarmd. Glucose daarentegen heeft de neiging te wiebelen en drijft TM7b nooit consequent tot volledige sluiting; het blijft vastzitten in een ondiepere, naar buiten geoccludeerde pose die het pad blokkeert zonder het transport te voltooien. De STD NMR-signalen volgen precies dit verschil in hoe lang suikers verblijven in de volledig geoccludeerde, hoog-contactconfiguratie.
Lessen van een malaria-transporter en een fructose-specialist
Om te onderzoeken of dit principe verder reikt dan XylE, richtten de onderzoekers zich op PfHT1, een suikertransporter van de malariaparasiet die zowel glucose als fructose kan verplaatsen, en op het zoogdierenzym GLUT5, een fructosespecialist in de darm. Met behulp van STD NMR, kristalstructuren, cryo-elektronmicroscopie en verdere simulaties ontdekten ze dat ook deze transporters TM7b gebruiken om suikers te coördineren tijdens de geoccludeerde stap. Een enkele asparaginezuur-aminozuur in TM7b speelt een centrale rol en maakt contact met belangrijke hydroxylgroepen op de suikerring terwijl de poort sluit. In PfHT1 legde een hoge-resolutie cryo-EM-snapshot een "halverwege" naar binnen geoccludeerde pose vast waarbij de suiker slechts gedeeltelijk wordt gecoördineerd; een eerder bepaalde kristalstructuur ving de volledig geoccludeerde pose. Vergelijking van de twee toonde dat de suiker slechts ongeveer twee miljardsten van een meter verschuift, maar daarbij een netwerk van extra contacten opbouwt dat de overgangstoestand-achtige geoccludeerde vorm veel strakker gebonden maakt.
Transporters als mini-enzymen
Als men al het bewijs samenneemt, stellen de auteurs voor dat suikerporters werken als enzymen, waarbij specificiteit niet wordt bepaald door de eerste bindingsstap maar door hoe goed een suiker past in een vluchtige overgangstoestand. Transporters flikkeren spontaan in naar buiten- en naar binnen-geoccludeerde vormen, zelfs zonder suiker. Een compatibele suiker "kiest" eerst een van deze vooraf bestaande poses (conformationele selectie), en triggert vervolgens een laatste aanscherping van de poort naar een volledig geoccludeerde toestand (induced fit) die het eiwit verplicht om om te klappen en de suiker aan de andere kant vrij te geven. Incompatibele suikers kunnen nog steeds binden, soms sterk, maar slagen er niet in deze laatste aanscherping teweeg te brengen, zodat ze als remmers optreden in plaats van als lading. Het erkennen dat de geoccludeerde toestand het echte beslismoment is, suggereert nieuwe manieren om medicijnen te ontwerpen die transporters vastzetten in een overgangsachtige pose, mogelijk door kankercellen of parasieten uit te hongeren door hun suikerlevering te blokkeren.
Bronvermelding: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Trefwoorden: glucosetransporters, suikerverplaatsing, membraaneiwitten, STD NMR, specificiteit van de overgangstoestand