Clear Sky Science · sv
En tvåstegsmekanism för sockertranslokation
Hur celler väljer rätt socker
Varje cell i din kropp är beroende av en stadig tillförsel av socker för energi, särskilt hjärnan och snabbt växande vävnader som tumörer. Det sockret måste passera ett fettliknande cellmembran och det görs via specialiserade ”portar” kallade transportörer. Denna artikel undersöker en bedrägligt enkel fråga med stora medicinska konsekvenser: när många snarlika sockerarter finns närvarande, hur avgör en transportör vilka som släpps igenom och vilka som stoppas? Svaret visar sig inte ligga i det första sammanstötningen mellan socker och protein, utan i en subtil tvåstegsdans långt inne i membranet. 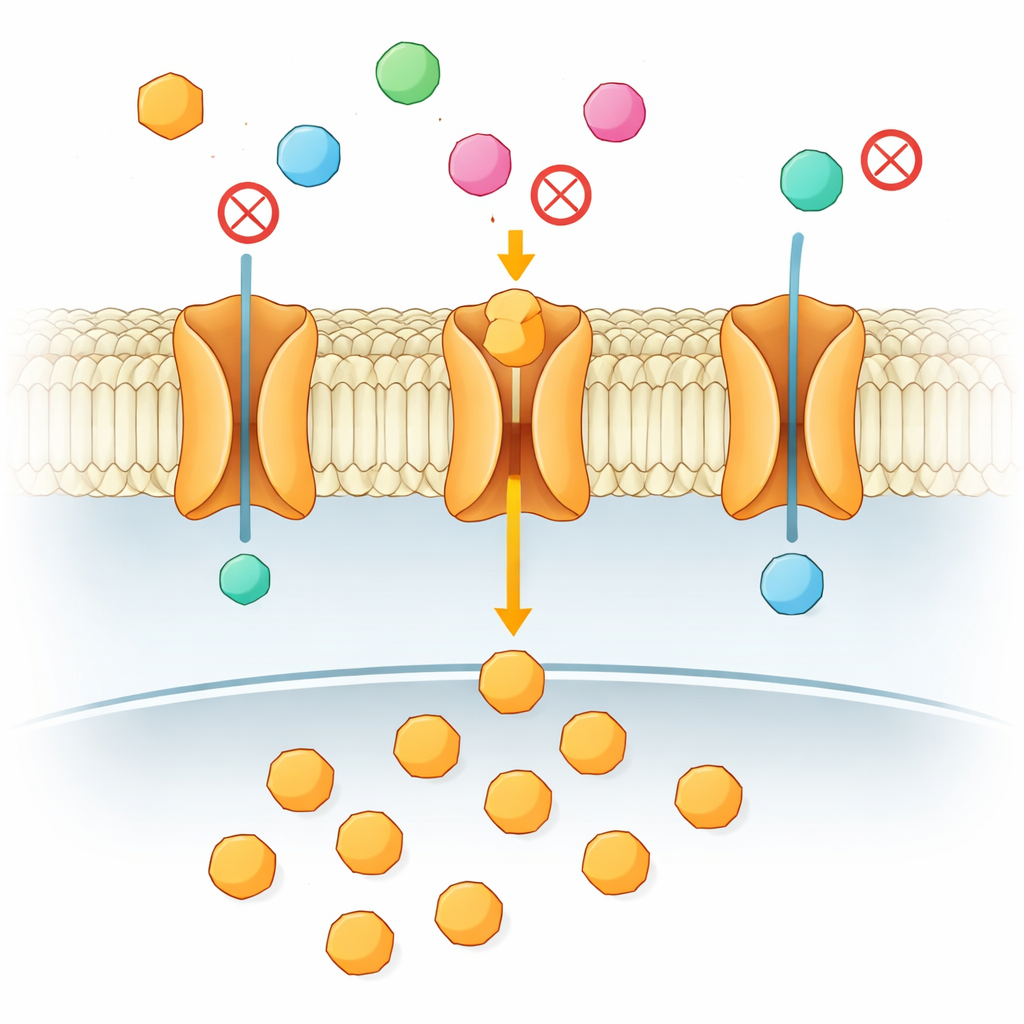
Varför likartade socker beter sig så olika
Hos människor finns det 14 närbesläktade glukostransportörer som ser slående lika ut där sockret faktiskt binder. Ändå flyttar de olika sockerarter med olika hastigheter och är kopplade till tillstånd som sträcker sig från diabetes till cancer. För att lösa upp detta pussel vände sig författarna till en bakteriell kusin till de mänskliga transportörerna, ett protein kallat XylE. XylE för xylose men binder glukos med nästan samma styrka, även om glukos inte kan passera och istället blockerar porten. Det udda beteendet gör XylE till en idealisk modell för att fråga vad som verkligen skiljer ett transporterat socker från ett som bara fastnar i systemet.
Lyssna på socker med magnetisk resonans
Forskargruppen använde en magnetresonansmetod känd som saturation transfer difference (STD) NMR som ett slags ”stetoskop” för möten mellan socker och transportör. De rekonstituerade renade transportörer i små konstgjorda membraner kallade liposomer, för att efterlikna den naturliga miljön. I STD NMR plockar endast sockermolekyler som dröjer nära proteinet tillräckligt länge upp en detekterbar signal. Den överraskande upptäckten var att XylE gav starka signaler med xylose, sitt naturliga last, men nästan inga med glukos, trots att båda sockren binder. När forskarna genetiskt låste XylE så att det inte längre kunde ändra form och transportera, försvann xylose-signalen i stort sett. Omvänt, när de konstruerade XylE för att få förmåga att flytta glukos, uppträdde starka glukossinaler. Med andra ord är det endast socker–transportör-par som faktiskt fullföljer resan över membranet som lyser upp i detta experiment. 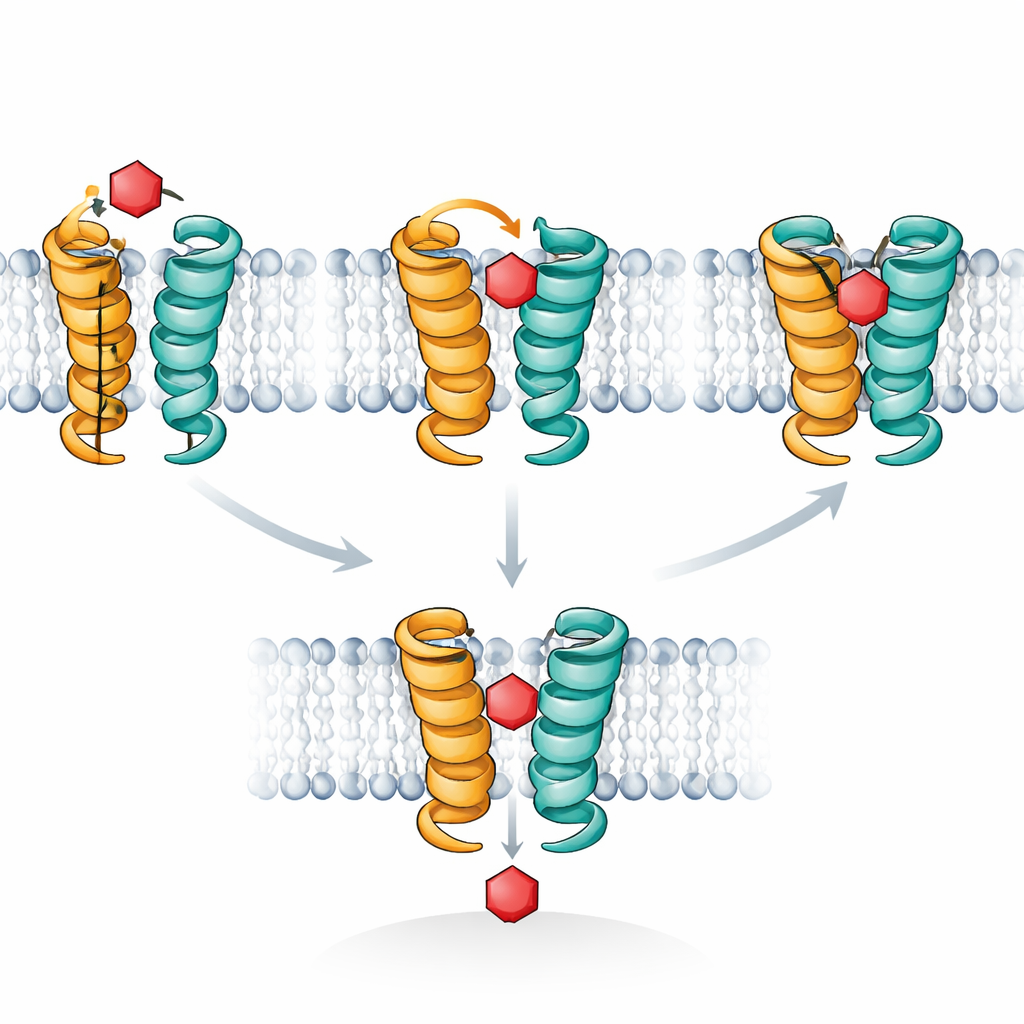
Ett dolt intermediärt steg i resan
Datorsimuleringar gav en molekylär film som förklarar dessa observationer. XylE, liksom mänskliga glukostransportörer, fungerar genom att cykla genom former som växelvis öppnar mot utsidan och insidan av cellen, med ett mellanting – ett "occluderat" tillstånd där sockret är avskärmat från båda sidor. Författarna fokuserade på ett kort helixsegment, kallat TM7b, som fungerar som en yttre grind. Deras simuleringar visade att när xylose sitter i precis rätt läge kan TM7b slå igen helt och stabilisera det djupt occluderade tillståndet där sockret är tätt omfamnat. Glukos tenderar däremot att vobbla och driver aldrig konsekvent TM7b till fullständig stängning; det förblir fast i en grundare, utåt-occluderad position som blockerar vägen utan att slutföra transporten. STD NMR-signalerna följer exakt denna skillnad i hur länge socker stannar i den fullt occluderade, högt kontaktintensiva konfigurationen.
Lärdomar från en malariatransportör och en fruktosspecialist
För att se om denna princip gäller bortom XylE vände sig forskarna till PfHT1, en sockertransportör från malariaparasiten som kan flytta både glukos och fruktos, och till den däggdjursbaserade GLUT5, en fruktosspecialist i tarmen. Genom att använda STD NMR, kristallstrukturer, kryo-elektronmikroskopi och ytterligare simuleringar fann de att även dessa transportörer förlitar sig på TM7b för att koordinera sockren under det occluderade steget. En enda asparagin‑aminosyra i TM7b spelar en central roll, genom att kontakta viktiga hydroxylgrupper på sockerringen när grinden stängs. I PfHT1 fångade en högupplöst kryo‑EM-snapshot en "halvvägs" inåt‑occluderad position där sockret bara delvis är koordinerat; en tidigare bestämd kristallstruktur fångade den fullt occluderade positionen. Jämförelsen av de två visade att sockret flyttar sig med bara ungefär två miljarderdels meter, men plockar ändå upp ett nätverk av ytterligare kontakter som gör övergångs‑liknande occluderat tillstånd mycket mer tätt bundet.
Transportörer som små enzymer
Sammanvägt föreslår författarna att sockerportare fungerar mycket som enzymer, där specificiteten styrs inte av det första bindningssteget utan av hur väl ett socker passar ett flyktigt övergångstillstånd. Transportörer fladdrar spontant in i utåt‑ och inåt‑occluderade former även utan socker. Ett kompatibelt socker ”väljer” först en av dessa förhands‑existerande poser (konformationell selektion) och utlöser sedan en slutlig åtstramning av grinden in i ett fullt occluderat tillstånd (inducerad passform) som binder proteinet till att vända sig och släppa sockret på andra sidan. Icke‑kompatibla sockerarter kan fortfarande binda, ibland starkt, men misslyckas med att driva det sista åtstramningssteget, så de fungerar som hämmare snarare än last. Att känna igen att det occluderade tillståndet är den verkliga beslutspunkten öppnar för nya sätt att designa läkemedel som fryser transportörer i en övergångs‑liknande pose och potentiellt svälter ut cancerceller eller parasiter genom att blockera deras sockertillförsel.
Citering: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Nyckelord: glukostransportörer, sockertranslokation, membranproteiner, STD NMR, övergångstillståndsspecificitet