Clear Sky Science · pl
Dwustopniowy mechanizm translokacji cukru
Jak komórki wybierają właściwy cukier
Każda komórka w organizmie potrzebuje stałego dopływu cukru jako źródła energii, zwłaszcza mózg oraz szybko rosnące tkanki, jak guzy. Ten cukier musi przejść przez lipofilową błonę komórkową, a robi to przez wyspecjalizowane „furtki” zwane transporterami. Artykuł bada pozornie proste pytanie o dużych implikacjach medycznych: gdy obecnych jest wiele podobnych cukrów, jak transporter decyduje, które przepuści, a które zablokuje? Okazuje się, że odpowiedź nie kryje się w pierwszym kontakcie cukru z białkiem, lecz w subtelnym, dwustopniowym tańcu głęboko w obrębie błony.
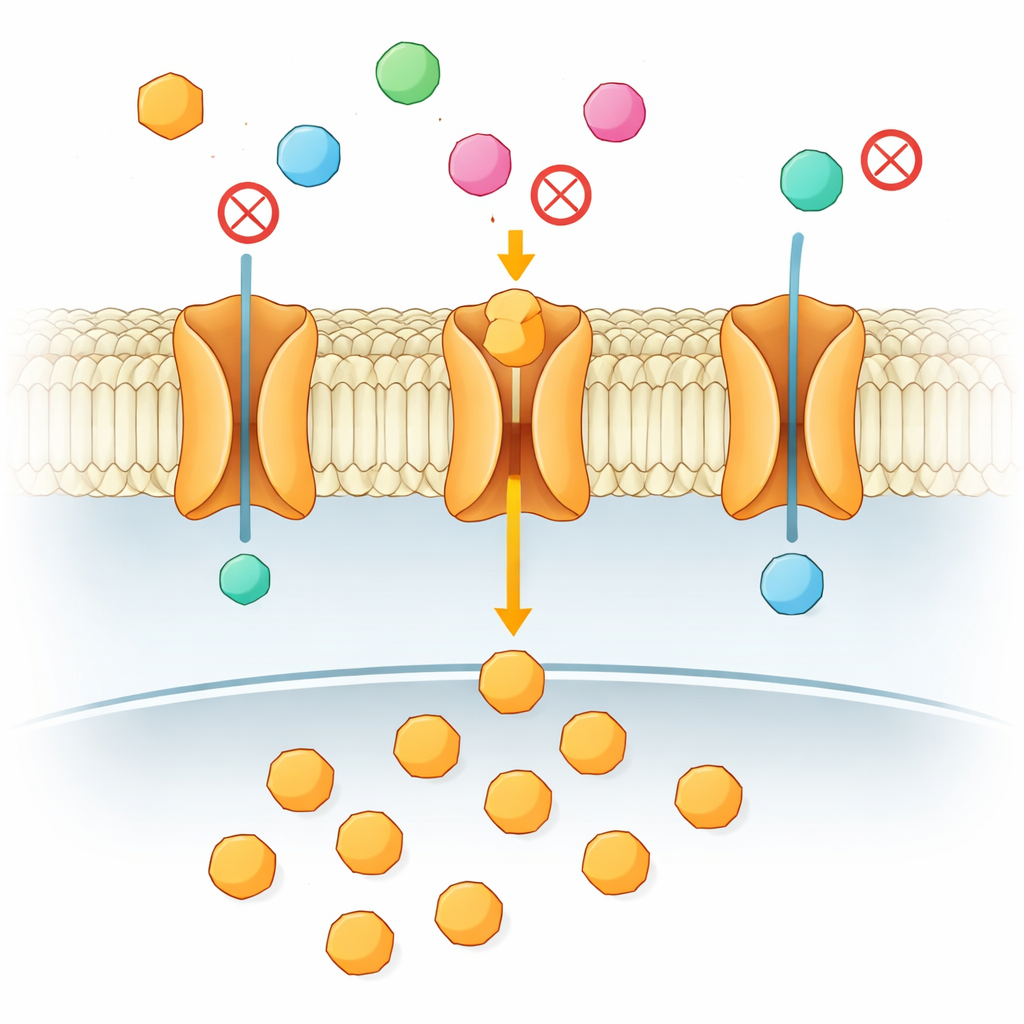
Dlaczego podobne cukry zachowują się tak różnie
U ludzi występuje 14 blisko spokrewnionych transporterów glukozy, które wyglądają niemal identycznie w miejscu wiązania cukru. Mimo to transportują różne cukry z różną szybkością i są powiązane z chorobami od cukrzycy po raka. Aby rozwiązać tę zagadkę, autorzy zwrócili się do bakteryjnego odpowiednika ludzkich transporterów — białka o nazwie XylE. XylE przenosi cukier ksylozę, ale wiąże glukozę z prawie takim samym powinowactwem, mimo że glukoza nie przechodzi przez transporter i zamiast tego zatyka furtkę. To nietypowe zachowanie czyni XylE idealnym modelem do sprawdzenia, co naprawdę odróżnia cukier transportowany od tego, który jedynie zakleszcza system.
Nasłuchiwanie cukrów za pomocą rezonansu magnetycznego
Zespół zastosował metodę rezonansu magnetycznego zwaną STD NMR (saturation transfer difference) jako rodzaj „stetoskopu” do badania spotkań cukier–transporter. Odtworzyli oczyszczone transportery w maleńkich sztucznych błonach zwanych liposomami, naśladując naturalne środowisko. W STD NMR sygnał odbierają tylko te molekuły cukru, które zatrzymują się blisko białka wystarczająco długo, by przejąć wykrywalny sygnał. Zaskakujące odkrycie było takie, że XylE dawał silne sygnały z ksylozą, swoim naturalnym ładunkiem, ale prawie żadne z glukozą, mimo że oba cukry wiążą się z białkiem. Gdy badacze genetycznie zablokowali XylE, tak by nie mógł zmieniać konformacji i transportować, sygnał ksylozy praktycznie zniknął. Odwrotnie, gdy zmodyfikowali XylE tak, że zyskał zdolność przenoszenia glukozy, pojawiły się silne sygnały glukozy. Innymi słowy, w tym eksperymencie świecą tylko pary cukier–transporter, które faktycznie kończą podróż przez błonę.
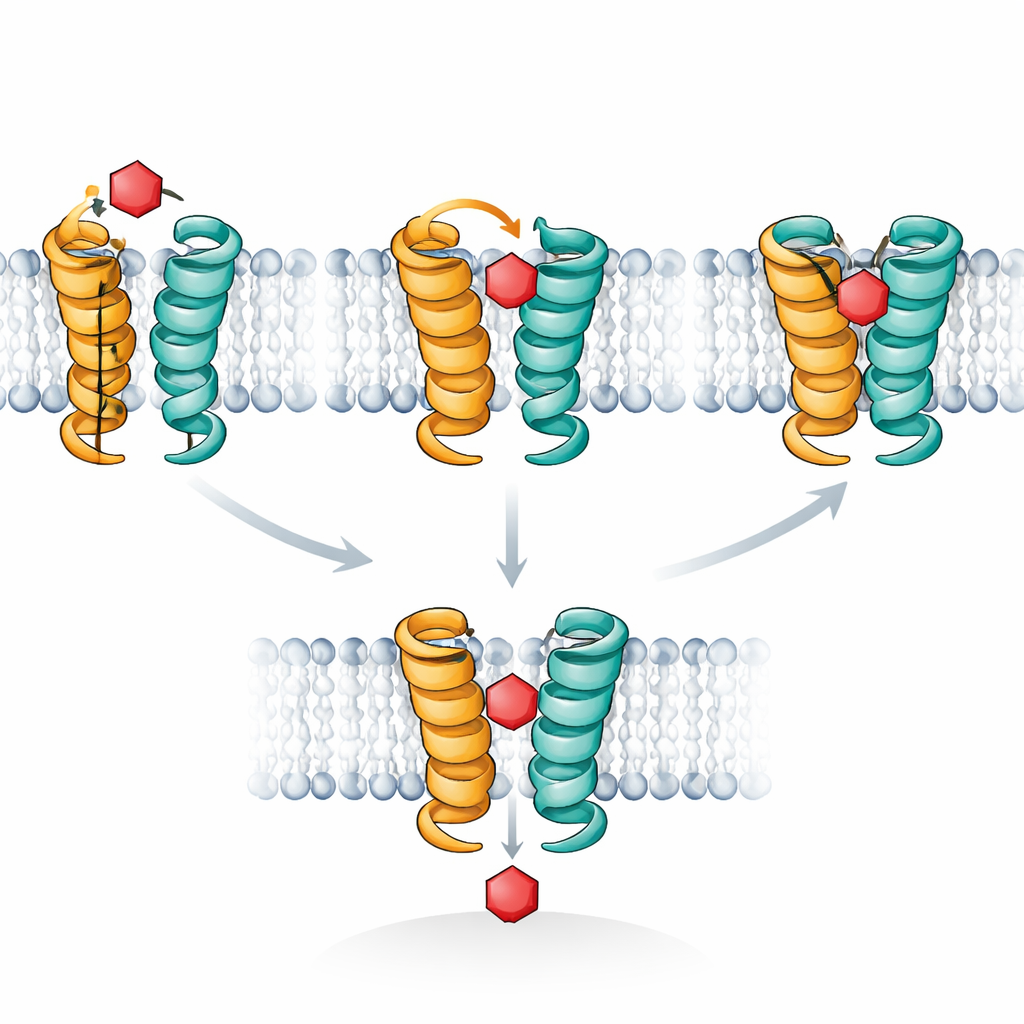
Ukryty etap pośredni w podróży
Symulacje komputerowe dostarczyły molekularnego filmu wyjaśniającego te obserwacje. XylE, podobnie jak ludzkie transportery glukozy, działa poprzez cykliczne zmiany kształtu, które na przemian otwierają się na zewnątrz i do wnętrza komórki, z pośrednim stanem „okludowanym”, w którym cukier jest odcięty od obu stron. Autorzy skupili się na krótkim segmencie helikalnym zwanym TM7b, który pełni rolę zewnętrznej bramy. Ich symulacje wykazały, że gdy ksyloza zajmuje odpowiednią pozycję, TM7b może zamknąć się całkowicie, stabilizując głęboko okludowany stan, w którym cukier jest silnie objęty. Glukoza natomiast ma tendencję do chybotania i nigdy konsekwentnie nie wymusza pełnego zamknięcia TM7b; pozostaje utkniona w płytszej, zewnętrznie-okludowanej pozycji, która zatyka przepustkę bez dokończenia transportu. Sygnały STD NMR odzwierciedlają dokładnie tę różnicę w czasie, jaki cukry spędzają w całkowicie okludowanej, obejmującej konfiguracji o wysokim kontakcie.
Wnioski z transportera malarii i specjalisty od fruktozy
Aby sprawdzić, czy zasada ta obowiązuje poza XylE, badacze zwrócili się do PfHT1, transportera cukrów z pasożyta malarii, który potrafi przenosić zarówno glukozę, jak i fruktozę, oraz do mlecznego GLUT5, specjalisty od fruktozy w jelicie. Korzystając ze STD NMR, struktur krystalicznych, kriomikroskopii elektronowej i dalszych symulacji, stwierdzili, że te transportery również polegają na TM7b do koordynacji cukrów podczas kroku okludowanego. Jedny aminokwas, asparagina, w TM7b odgrywa kluczową rolę, kontaktując się z istotnymi grupami hydroksylowymi na pierścieniu cukru w trakcie zamykania bramy. W PfHT1 migawka o wysokiej rozdzielczości z kriomikroskopii uchwyciła „połowiczną” wewnętrznie-okludowaną pozę, w której cukier jest tylko częściowo skoordynowany; wcześniej określona struktura krystaliczna zarejestrowała w pełni okludowaną pozę. Porównanie obu pokazało, że przesunięcie cukru wynosiło zaledwie około dwóch miliardowych metra, a mimo to powstała sieć dodatkowych kontaktów, które sprawiają, że forma okludowana przypominająca stan przejściowy jest znacznie mocniej związana.
Transportery jako maleńkie enzymy
Składając wszystkie dowody, autorzy proponują, że portery cukrów działają podobnie jak enzymy — specyficzność nie wynika z pierwszego etapu wiązania, lecz z tego, jak dobrze cukier pasuje do przelotnego stanu przejściowego. Transportery spontanicznie migoczą do zewnętrznie i wewnętrznie okludowanych kształtów nawet bez cukru. Kompatybilny cukier najpierw „wybiera” jedną z tych istniejących wcześniej póz (selekcja konformacyjna), a następnie wywołuje ostateczne dociśnięcie bramy do w pełni okludowanego stanu (indukowane dopasowanie), co zobowiązuje białko do odwrócenia i uwolnienia cukru po drugiej stronie. Niekompatybilne cukry nadal mogą wiązać się, czasem silnie, ale nie są w stanie wywołać tego ostatniego dociśnięcia, więc działają jako inhibitory zamiast ładunku. Uznanie, że stan okludowany jest rzeczywistym punktem decyzyjnym, sugeruje nowe sposoby projektowania leków, które zamrażają transportery w pozie przypominającej przejściową, potencjalnie pozbawiając komórki raka lub pasożyty źródła cukru przez zablokowanie ich dopływu.
Cytowanie: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Słowa kluczowe: transportery glukozy, translokacja cukrów, białka błonowe, STD NMR, specyficzność stanu przejściowego