Clear Sky Science · fr
Un mécanisme en deux étapes pour la translocation des sucres
Comment les cellules choisissent le bon sucre
Toute cellule de votre corps dépend d’un apport régulier en sucre pour l’énergie, en particulier le cerveau et les tissus à croissance rapide comme les tumeurs. Ce sucre doit traverser une membrane cellulaire lipidique, et il le fait via des « portes » spécialisées appelées transporteurs. Cet article explore une question apparemment simple mais aux importantes implications médicales : lorsque plusieurs sucres similaires sont présents, comment un transporteur décide-t-il lesquels laisser passer et lesquels bloquer ? La réponse ne réside pas dans le premier contact entre le sucre et la protéine, mais dans une subtile danse en deux étapes profondément située dans la membrane. 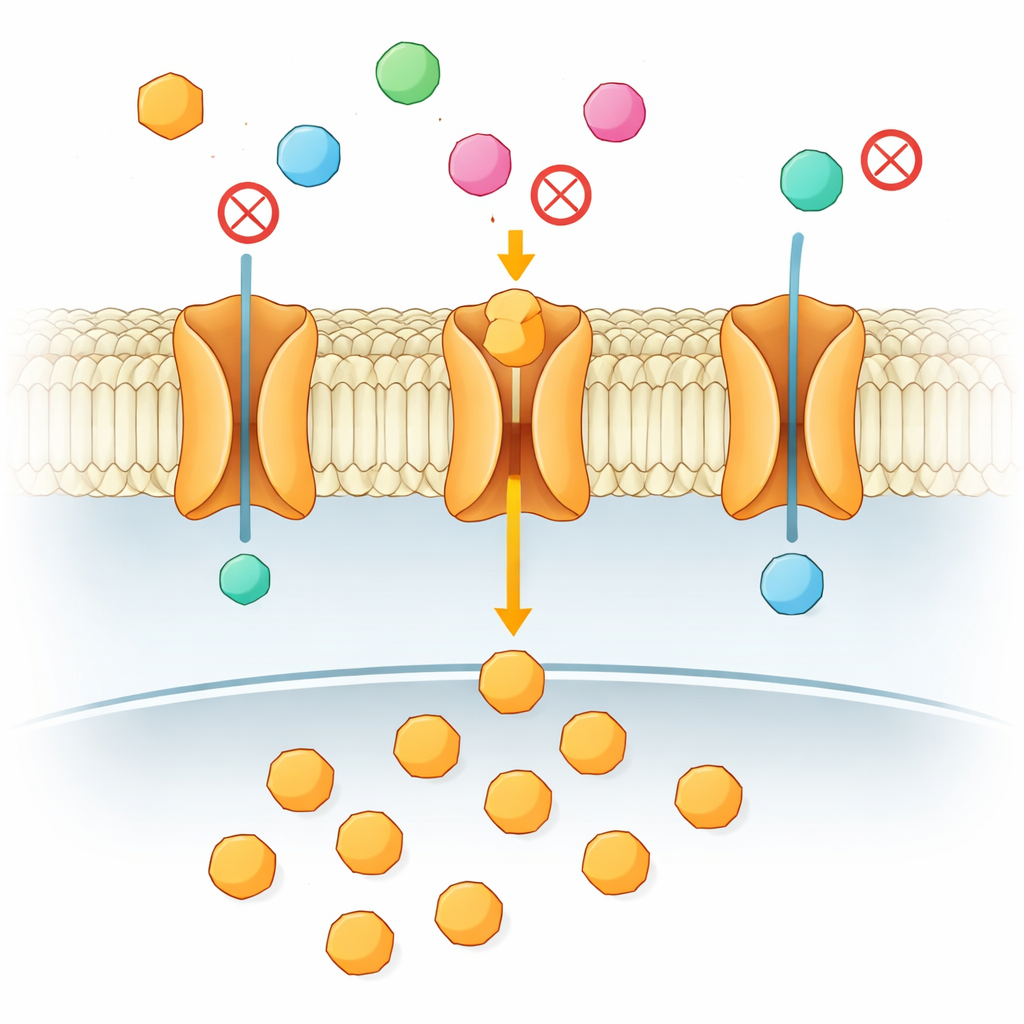
Pourquoi des sucres similaires se comportent si différemment
Chez l’homme, il existe 14 transporteurs de glucose étroitement liés qui se ressemblent étonnamment là où le sucre se lie réellement. Pourtant, ils déplacent des sucres différents à des vitesses différentes et sont associés à des pathologies allant du diabète au cancer. Pour démêler ce puzzle, les auteurs se sont tournés vers un cousin bactérien des transporteurs humains, une protéine appelée XylE. XylE transporte le sucre xylose mais lie le glucose avec une affinité presque identique, bien que le glucose ne puisse pas traverser et finisse par boucher la porte. Ce comportement étrange fait de XylE un modèle idéal pour interroger ce qui distingue réellement un sucre transporté d’un sucre qui enrayé le système.
Écouter les sucres avec la résonance magnétique
L’équipe a utilisé une méthode de résonance magnétique connue sous le nom de STD NMR (saturation transfer difference) comme une sorte de « stéthoscope » pour les rencontres sucre–transporteur. Ils ont reconstitué des transporteurs purifiés dans de minuscules membranes artificielles appelées liposomes, mimant l’environnement naturel. En STD NMR, seules les molécules de sucre qui restent suffisamment longtemps à proximité de la protéine reçoivent un signal détectable. La découverte surprenante fut que XylE produisait des signaux forts avec le xylose, son « cargo » naturel, mais quasiment aucun avec le glucose, bien que les deux sucres se lient. Lorsque les chercheurs ont verrouillé génétiquement XylE pour qu’il ne puisse plus changer de conformation et transporter, le signal du xylose a pratiquement disparu. Inversement, lorsqu’ils ont modifié XylE pour lui donner la capacité de déplacer le glucose, de forts signaux de glucose sont apparus. En d’autres termes, seuls les couples sucre–transporteur qui accomplissent effectivement le trajet à travers la membrane s’allument dans cette expérience. 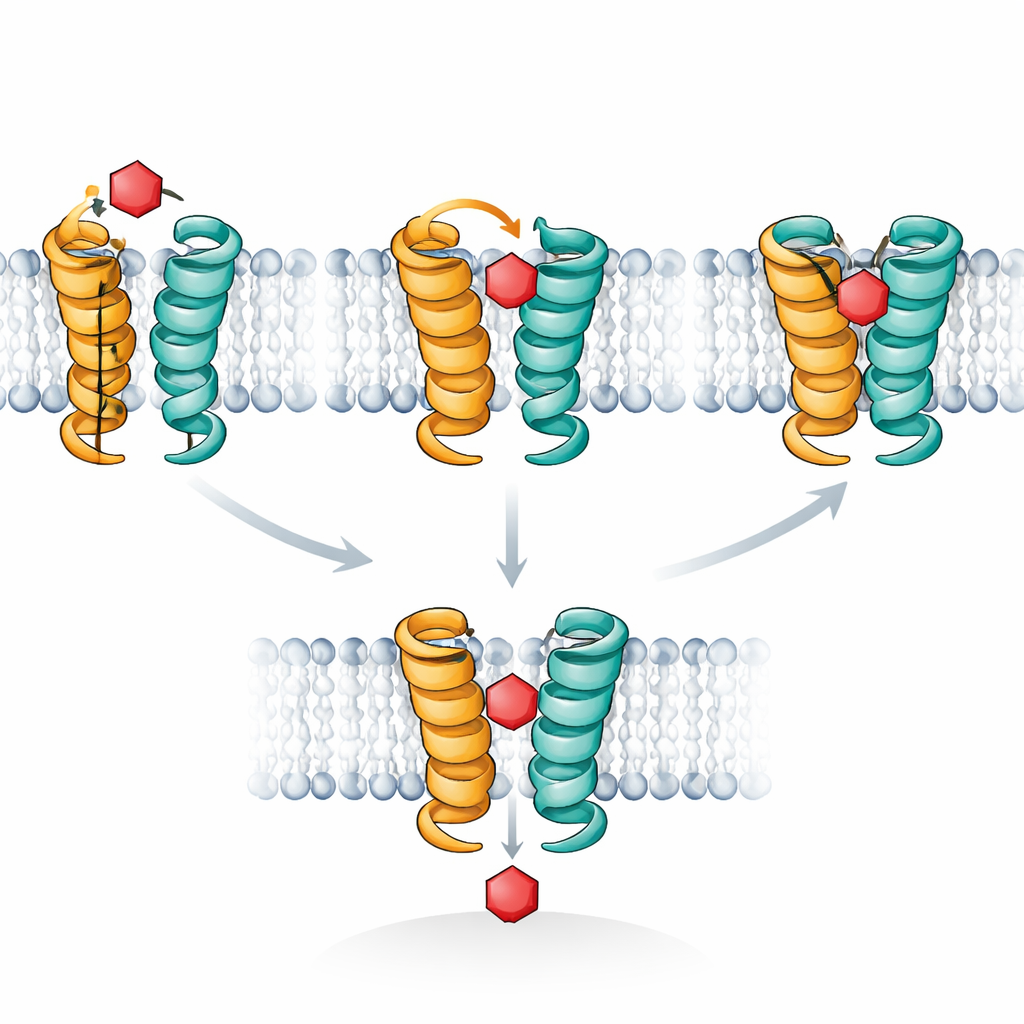
Une étape intermédiaire cachée dans le trajet
Des simulations informatiques ont fourni un film moléculaire pour expliquer ces observations. XylE, comme les transporteurs de glucose humains, fonctionne en alternant des conformations qui s’ouvrent alternativement vers l’extérieur et l’intérieur de la cellule, avec un état intermédiaire « occlus » où le sucre est isolé des deux côtés. Les auteurs se sont concentrés sur un court segment hélicoïdal, nommé TM7b, qui agit comme une porte externe. Leurs simulations ont montré que lorsque le xylose adopte la bonne position, TM7b peut se refermer complètement, stabilisant l’état profondément occlus où le sucre est fermement embrassé. Le glucose, en revanche, a tendance à osciller et ne pousse jamais de manière cohérente TM7b à achever cette fermeture ; il reste coincé dans une posture occlusive plus superficielle vers l’extérieur qui bloque le passage sans finir le transport. Les signaux STD NMR reflètent précisément cette différence de durée de séjour des sucres dans la configuration entièrement occluse et à haut contact.
Enseignements tirés d’un transporteur du paludisme et d’un spécialiste du fructose
Pour vérifier si ce principe s’applique au-delà de XylE, les chercheurs se sont intéressés à PfHT1, un transporteur de sucres du parasite du paludisme capable de déplacer à la fois glucose et fructose, et à GLUT5, un spécialiste du fructose chez les mammifères présent dans l’intestin. En combinant STD NMR, structures cristallographiques, cryo‑microscopie électronique et simulations complémentaires, ils ont constaté que ces transporteurs s’appuient aussi sur TM7b pour coordonner les sucres pendant l’étape occluse. Un seul acide aminé, une asparagine dans TM7b, joue un rôle central en contactant des groupes hydroxyle clés sur le cycle du sucre à mesure que la porte se referme. Dans PfHT1, un cliché cryo‑EM à haute résolution a capturé une posture « à mi‑chemin » inward‑occluded où le sucre est seulement partiellement coordonné ; une structure cristallographique déterminée antérieurement a saisi la posture entièrement occluse. La comparaison des deux montre un déplacement du sucre d’à peine deux milliardièmes de mètre, mais l’acquisition d’un réseau de contacts supplémentaires qui rendent la forme occluse, proche d’un état de transition, beaucoup plus fortement liée.
Les transporteurs comme de minuscules enzymes
En rassemblant toutes les preuves, les auteurs proposent que les transporteurs de sucres fonctionnent à l’instar d’enzymes, la spécificité étant gouvernée non pas par la première étape de liaison mais par l’aptitude d’un sucre à convenir à un état de transition éphémère. Les transporteurs basculent spontanément entre des conformations outward‑ et inward‑occluded même en l’absence de sucre. Un sucre compatible « choisit » d’abord l’une de ces postures préexistantes (sélection conformationnelle), puis déclenche un dernier resserrement de la porte vers un état entièrement occlus (adaptation induite) qui engage la protéine à basculer et relâcher le sucre de l’autre côté. Les sucres incompatibles peuvent encore se lier, parfois fortement, mais échouent à provoquer ce dernier resserrement, agissant ainsi comme des inhibiteurs plutôt que comme du cargo. Reconnaître que l’état occlus est le véritable point de décision ouvre de nouvelles voies pour concevoir des médicaments qui figent les transporteurs dans une posture de type transition, privant potentiellement les cellules cancéreuses ou les parasites de leur approvisionnement en sucre.
Citation: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Mots-clés: transporteurs de glucose, translocation des sucres, protéines membranaires, STD NMR, spécificité de l’état de transition