Clear Sky Science · he
מנגנון דו-שלבי להעברת סוכרים
כיצד תאים בוחרים את הסוכר הנכון
כל תא בגופך זקוק למימן קבוע של סוכר לאנרגיה, במיוחד המוח והרקמות הגדלות במהירות כמו גידולים. הסוכר הזה חייב לחצות ממברנת שומן של התא, והוא עושה זאת דרך "שערים" מיוחדים שנקראים משאבות (טרנספורטרים). מאמר זה בוחן שאלה לכאורה פשוטה עם השלכות רפואיות רחבות: כאשר קיימים מספר סוכרים דומים, כיצד המשאבה מחליטה אילו להכניס ואילו לחסום? התשובה אינה טמונה במגע הראשוני בין הסוכר לחלבון, אלא בריקוד דקיק דו-שלבי שמתרחש עמוק בתוך הממברנה. 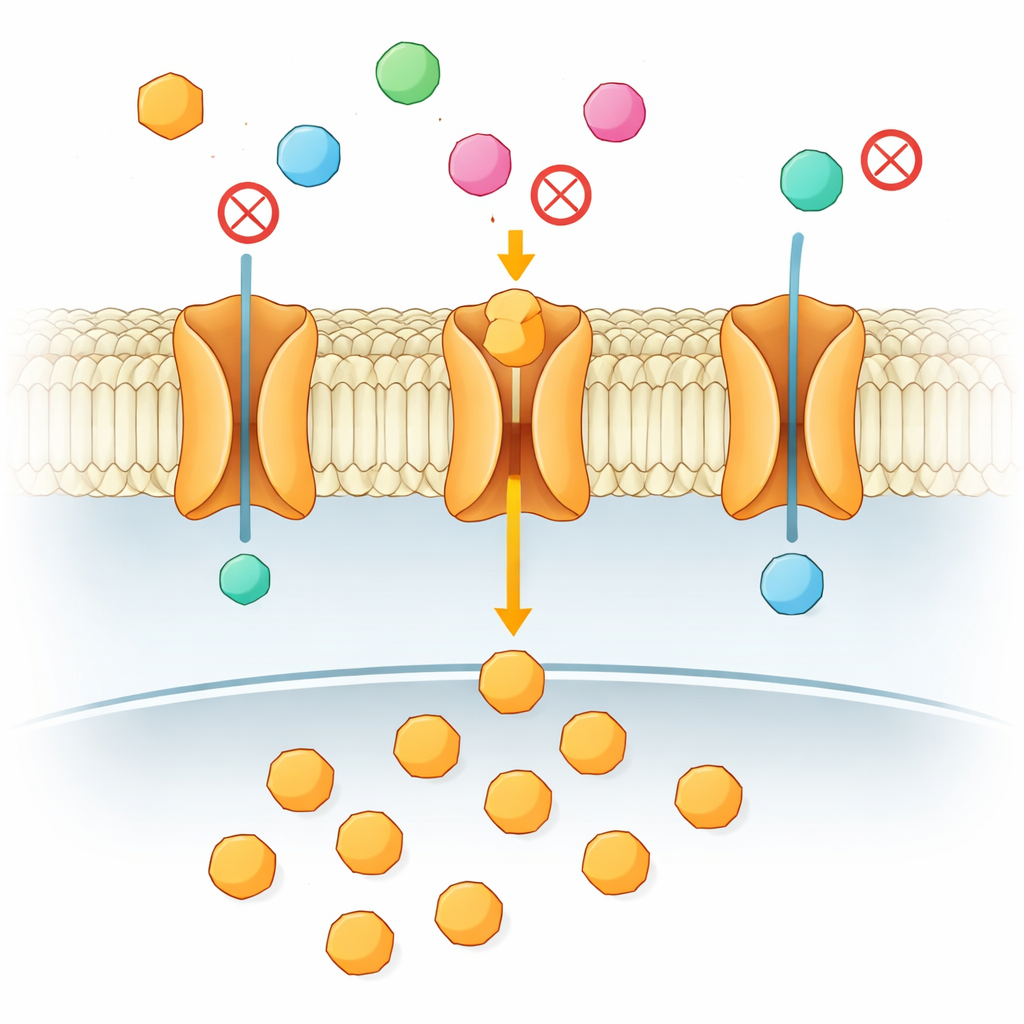
מדוע סוכרים דומים מתנהגים כל כך אחרת
בבני אדם יש 14 משאבות גלוקוז קרובות זו לזו שמראות דמיון מרשים באזור שבו הסוכר נקשר בפועל. אך הן מעבירות סוכרים שונים במהירויות שונות וקושרות למחלות הנעות מסוכרת עד סרטן. כדי לפענח את החידה פנו החוקרים לקרוב חיידקי של המשאבות האנושיות, חלבון בשם XylE. XylE מעביר את הסוכר קסילוז אך קושר גלוקוז בעוצמת קשר כמעט זהה, אף על פי שגלוקוז אינו יכול לעבור ובמקום זאת סותם את השער. ההתנהגות המוזרה הזו הופכת את XylE למודל אידיאלי לשאלה מה באמת מבחין בין סוכר שמועבר לבין זה שמסתם את המערכת.
להקשיב לסוכרים בעזרת תהודה מגנטית
הקבוצה השתמשה בשיטת תהודה מגנטית הנקראת Saturation Transfer Difference (STD) NMR כמעין "סטטוסקופ" לפגישות בין סוכר למשאבה. הם השיבו את המשאבות הטהורות בממברנות מלאכותיות זעירות הנקראות ליפוזומים, המדמות את הסביבה הטבעית. ב-STD NMR רק מולקולות סוכר שנמצאות קרוב לחלבון זמן מספיק ממושך קולטים אות שניתן לזהות. הממצא המפתיע היה ש-XylE ייצר אותות חזקים עם קסילוז, המטען הטבעי שלו, אך כמעט ואין אותות עם גלוקוז, אף על פי ששני הסוכרים נקשרים. כאשר החוקרים נעלו גנטית את XylE כך שלא יוכל לשנות צורה ולהעביר, אות הקסילוז כמעט נעלם. להפך, כאשר הנדסו את XylE כדי לקבל יכולת להזיז גלוקוז, הופיעו אותות גלוקוז חזקים. במילים אחרות, רק זוגות סוכר–משאבה שמממשים בפועל את המסע דרך הממברנה מאירים בניסוי זה. 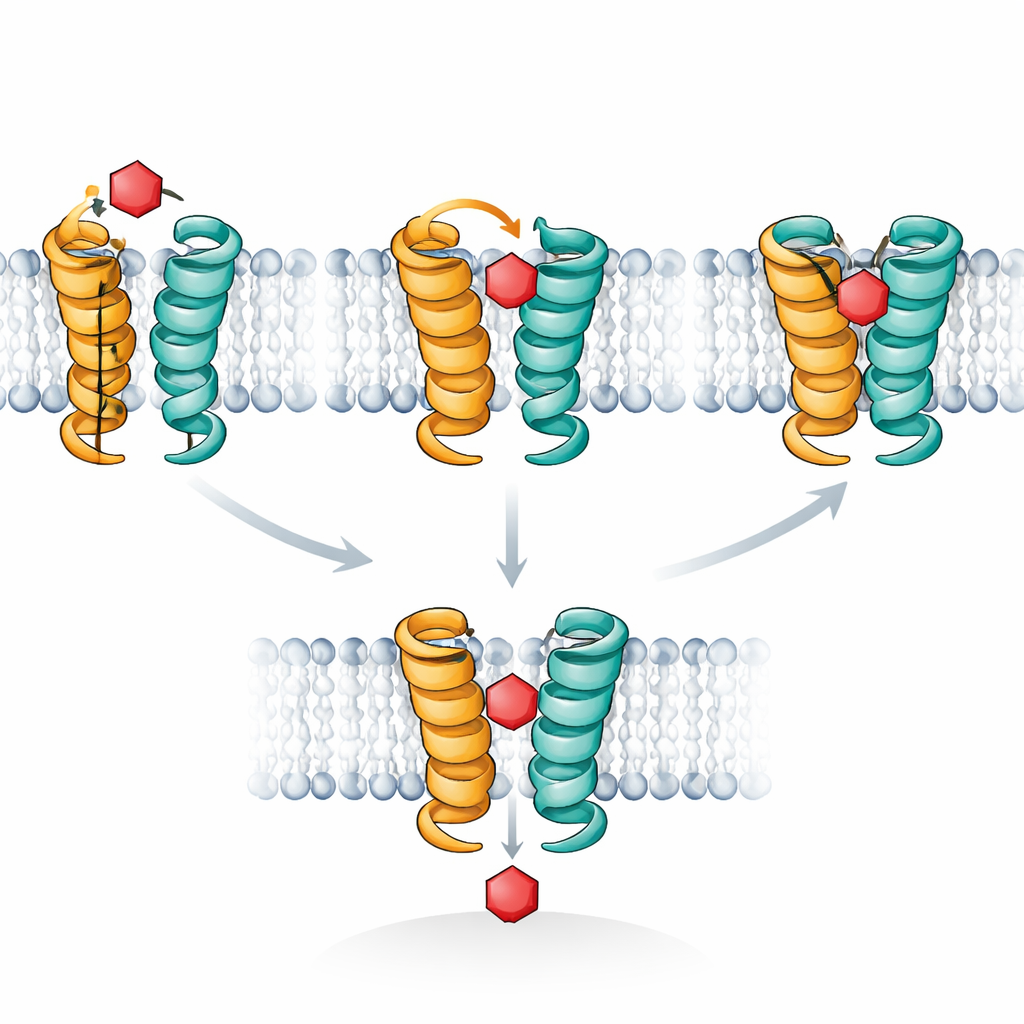
שלב ביניים נסתר במסע
סימולציות ממוחשבות סיפקו סרט מולקולרי שמסביר את התצפיות הללו. XylE, כמו משאבות גלוקוז אנושיות, פועלת באמצעות מחזור של צורות שפותחות לסירוגין כלפי חוץ וכלפי פנים של התא, עם מצב תווך "חסום" שבו הסוכר מבודד משני הצדדים. המחברים התמקדו במקטע ספירלי קצר, הנקרא TM7b, שמתפקד כשער חיצוני. הסימולציות הראו שכאשר קסילוז מצוי בפוזה מדויקת, TM7b יכול להיסגר לחלוטין, לייצב את המצב החסום העמוק שבו הסוכר מאובטח בחיבוק הדוק. גלוקוז, לעומת זאת, נוטה להתנדנד ולא מצליח בעקביות לדחוף את TM7b להשלים את הסגירה; הוא נשאר תקוע בתנוחה חיצונית-חסומה רדודה יותר שחוסמת את המסלול מבלי להשלים את ההעברה. אותות ה-STD NMR עוקבים בדיוק אחרי ההבדל במשך כמה זמן הסוכרים שוהים בקונפיגורציה החסומה המלאה עם קשרים מרובים.
תובנות ממשאבת מלריה ומומחה פרוקטוז
כדי לבדוק האם עיקרון זה תקף מעבר ל-XylE, החוקרים פנו ל-PfHT1, משאבת סוכר של טפיל המלריה שיכולה להעביר גם גלוקוז וגם פרוקטוז, ול-GLUT5 של היונקים, מומחה לפרוקטוז במעיים. בעזרת STD NMR, מבנים גבישיים, מיקרוסקופיית קריואלקטרון וסימולציות נוספות, הם מצאו שגם משאבות אלה מסתמכות על TM7b לתאום הסוכרים במהלך שלב החסימה. חומצת אמינו אספרגין יחידה ב-TM7b ממלאת תפקיד מרכזי, ונוגעת בקבוצות הידרוקסיל מפתחיות על טבעת הסוכר כאשר השער נסגר. ב-PfHT1, תמונת cryo-EM ברזולוציה גבוהה תפסה תנוחת "חצי־דרך" פנימית-חסומה שבה הסוכר מתואם רק חלקית; מבנה גבישי שנקבע בעבר תפס את התנוחה החסומה המלאה. השוואת השתיים הראתה תזוזת סוכר של כחצי־שני מיליארדית המטר בלבד, ובכל זאת רכישת רשת של מגעים נוספים שהופכת את הצורה החסומה בדומה למצב מעבר לקשירה חזקה הרבה יותר.
משאבות כמיניאטורות של אנזימים
בהשוואת כל הקווים, המחברים מציעים שמשאבות סוכר פועלות בדומה לאנזימים, כשהספציפיות נשלטת לא על ידי שלב הקישור הראשוני אלא על ידי מידת התאמת הסוכר למצב מעבר חולף. המשאבות מהבהבות ספונטנית לצורות חיצוניות-וחסומות פנימיות גם ללא סוכר. סוכר תואם בוחר תחילה אחת מהתנוחות הקיימות מראש האלה (בחירת קונפורמציה), ואז מעורר הידוק סופי של השער לתוך מצב חסום מלא (התאמה מגרה) שמחוייב את החלבון להתהפך ולשחרר את הסוכר בצד השני. סוכרים שאינם תואמים עדיין יכולים להיקשר, לעתים בעוצמה, אך אינם מצליחים להניע את שלב ההידוק האחרון, ולכן הם פועלים כמעכבים במקום כמטען. ההכרה בכך שמצב החסימה הוא הנקודה ההכרעתית האמיתית מציעה דרכים חדשות לעיצוב תרופות שמקפיאות משאבות בתנוחה דמויית־מעבר, ובכך עשויות להרעיב תאים סרטניים או טפילים על ידי חסימת אספקת הסוכר שלהם.
ציטוט: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
מילות מפתח: מפטרי גלוקוז, העברת סוכרים, חלבוני ממברנה, STD NMR, ספציפיות של מצב מעבר