Clear Sky Science · it
Un meccanismo in due fasi per la traslocazione degli zuccheri
Come le cellule scelgono lo zucchero giusto
Ogni cellula del tuo corpo dipende da un flusso costante di zucchero per ottenere energia, in particolare il cervello e i tessuti in rapida crescita come i tumori. Quello zucchero deve attraversare una membrana cellulare lipidica, e lo fa tramite “porte” specializzate chiamate trasportatori. Questo articolo esplora una domanda apparentemente semplice ma dalle grandi implicazioni mediche: quando sono presenti molti zuccheri simili, come fa un trasportatore a decidere quali far passare e quali bloccare? La risposta non risiede nel primo contatto tra zucchero e proteina, ma in una sottile danza in due fasi che avviene in profondità nella membrana. 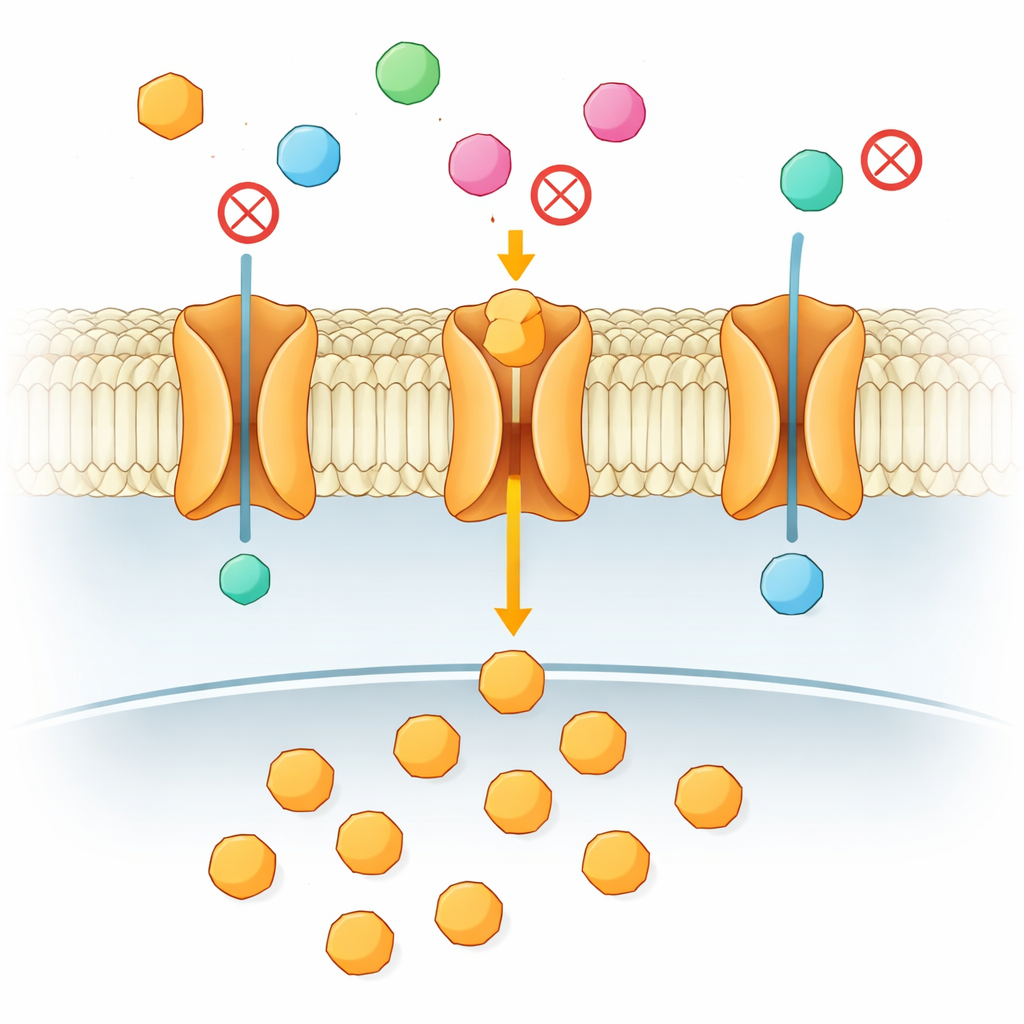
Perché zuccheri simili si comportano in modo così diverso
Nell’uomo esistono 14 trasportatori del glucosio strettamente correlati che appaiono sorprendentemente simili nel sito dove lo zucchero si lega. Eppure spostano zuccheri diversi a velocità diverse e sono collegati a patologie che vanno dal diabete al cancro. Per districare questo enigma, gli autori si sono rivolti a un cugino batterico dei trasportatori umani, una proteina chiamata XylE. XylE trasporta lo zucchero xiloso ma lega il glucosio con quasi la stessa affinità, nonostante il glucosio non possa attraversare e anzi incastri la porta. Questo comportamento curioso rende XylE un modello ideale per chiedersi cosa distingua realmente uno zucchero trasportato da uno che semplicemente blocca il sistema.
Ascoltare gli zuccheri con la risonanza magnetica
Il gruppo ha usato un metodo di risonanza magnetica noto come saturation transfer difference (STD) NMR come una sorta di “stetoscopio” per gli incontri zucchero–trasportatore. Hanno ricostituito trasportatori purificati in piccole membrane artificiali chiamate liposomi, imitando l’ambiente naturale. Nell’STD NMR, solo le molecole di zucchero che rimangono a lungo vicino alla proteina acquisiscono un segnale rilevabile. La scoperta sorprendente è stata che XylE produceva segnali forti con la xilosa, il suo carico naturale, ma quasi nulli con il glucosio, nonostante entrambi gli zuccheri si leghino. Quando i ricercatori hanno bloccato geneticamente XylE in modo che non potesse più cambiare forma e trasportare, il segnale della xilosa è praticamente scomparso. Viceversa, quando hanno ingegnerizzato XylE perché potesse muovere il glucosio, sono comparsi forti segnali di glucosio. In altre parole, solo le coppie zucchero–trasportatore che completano realmente il viaggio attraverso la membrana si illuminano in questo esperimento. 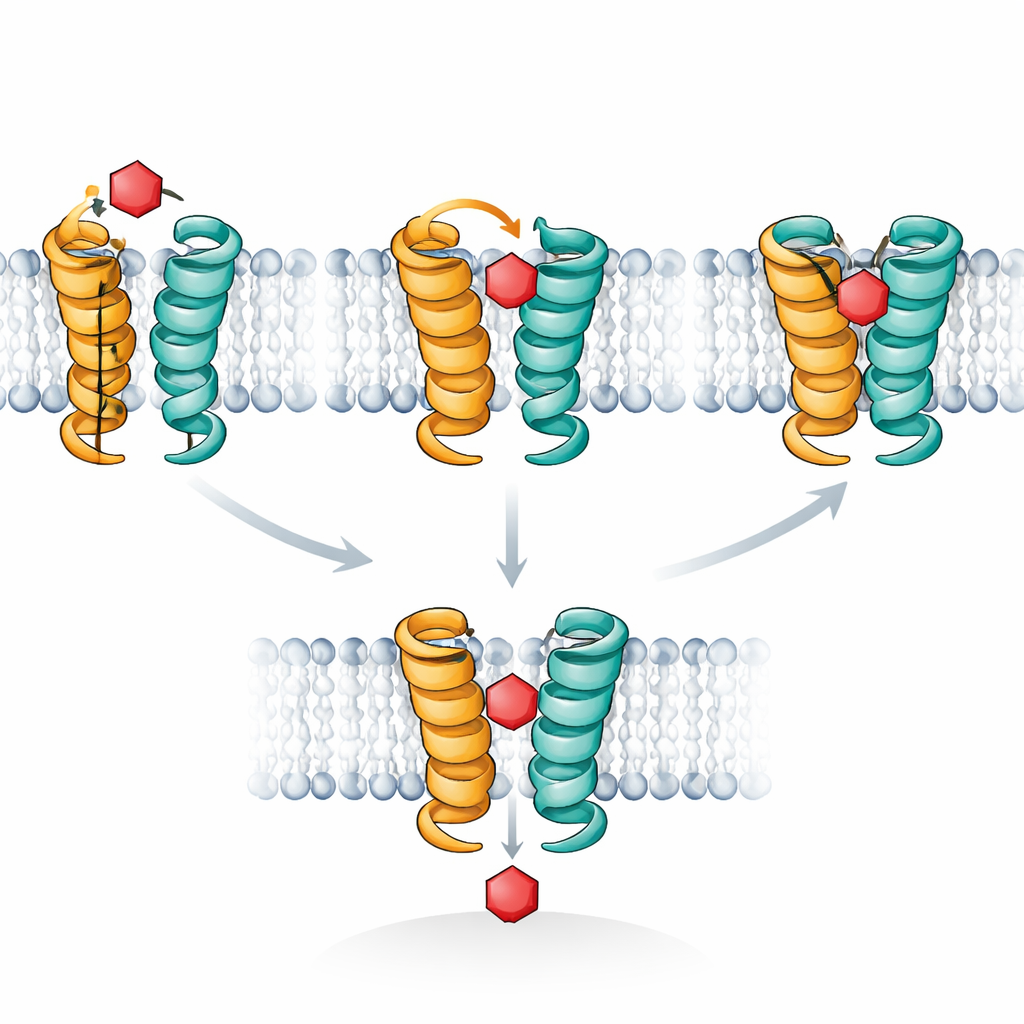
Un passo intermedio nascosto nel viaggio
Le simulazioni al computer hanno fornito un film molecolare per spiegare queste osservazioni. XylE, come i trasportatori del glucosio umani, funziona alternando conformazioni che si aprono alternativamente verso l’esterno e verso l’interno della cellula, con uno stato intermedio “occluso” in cui lo zucchero è isolato da entrambi i lati. Gli autori si sono concentrati su un breve segmento elicoidale, chiamato TM7b, che agisce come una porta esterna. Le loro simulazioni hanno mostrato che quando la xilosa si trova nella posa giusta, TM7b può chiudersi completamente, stabilizzando lo stato profondamente occluso in cui lo zucchero è strettamente avvolto. Il glucosio, al contrario, tende a oscillare e non guida in modo coerente TM7b a completare questa chiusura; rimane bloccato in una posa occlusa esternamente più superficiale che blocca il percorso senza portare a termine il trasporto. I segnali STD NMR rispecchiano esattamente questa differenza su quanto a lungo gli zuccheri dimorano nella configurazione completamente occlusa e ad alto contatto.
Lezioni da un trasportatore della malaria e da uno specialista del fruttosio
Per verificare se questo principio vale oltre XylE, i ricercatori hanno studiato PfHT1, un trasportatore di zuccheri del parassita della malaria che può muovere sia glucosio sia fruttosio, e GLUT5, uno specialista del fruttosio nell’intestino dei mammiferi. Usando STD NMR, strutture cristalline, crio-microscopia elettronica e ulteriori simulazioni, hanno trovato che anche questi trasportatori si affidano a TM7b per coordinare gli zuccheri durante lo stato occluso. Un’unica asparagina nella TM7b gioca un ruolo centrale, contattando gruppi ossidrilici chiave sull’anello zuccherino mentre la porta si chiude. In PfHT1, uno scatto crio-EM ad alta risoluzione ha catturato una posa “a metà strada” occlusa verso l’interno dove lo zucchero è solo parzialmente coordinato; una struttura cristallina precedentemente determinata ha mostrato la posa completamente occlusa. Confrontando le due si è visto lo spostamento dello zucchero di appena due miliardesimi di metro, eppure l’acquisizione di una rete di contatti aggiuntivi rende la forma occlusa simile a uno stato di transizione molto più strettamente legata.
I trasportatori come piccoli enzimi
Mettendo insieme tutte le evidenze, gli autori propongono che i portatori di zuccheri operino in modo simile agli enzimi, con la specificità governata non dal primo passo di legame ma da quanto bene uno zucchero si adatti a uno stato di transizione effimero. I trasportatori fluttuano spontaneamente tra forme occluse verso l’esterno e verso l’interno anche senza zucchero. Uno zucchero compatibile prima “sceglie” una di queste pose preesistenti (selezione conformazionale), quindi innesca un serraggio finale della porta in uno stato completamente occluso (adattamento indotto) che obbliga la proteina a ribaltarsi e rilasciare lo zucchero dall’altra parte. Zuccheri non compatibili possono comunque legarsi, talvolta con forza, ma non riescono a guidare quest’ultimo serraggio, così agiscono come inibitori piuttosto che come carico. Riconoscere che lo stato occluso è il vero punto decisionale suggerisce nuove strategie per progettare farmaci che congelino i trasportatori in una posa simile allo stato di transizione, potenzialmente affamando le cellule tumorali o i parassiti bloccando la loro fornitura di zuccheri.
Citazione: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Parole chiave: trasportatori del glucosio, traslocazione degli zuccheri, proteine di membrana, STD NMR, specificità dello stato di transizione