Clear Sky Science · de
Ein zweistufiger Mechanismus für Zuckertranslokation
Wie Zellen den richtigen Zucker auswählen
Jede Zelle in Ihrem Körper ist auf eine konstante Zufuhr von Zucker als Energiequelle angewiesen, besonders das Gehirn und schnell wachsende Gewebe wie Tumoren. Dieser Zucker muss eine fetthaltige Zellmembran passieren, was über spezialisierte „Tore“ geschieht, die Transporter genannt werden. Dieser Artikel untersucht eine auf den ersten Blick einfache Frage mit weitreichenden medizinischen Folgen: Wenn viele ähnliche Zucker gleichzeitig vorhanden sind, wie entscheidet ein Transporter, welche passieren dürfen und welche blockiert werden? Die Antwort liegt nicht im ersten Kontakt zwischen Zucker und Protein, sondern in einem subtilen zweistufigen Tanz tief in der Membran. 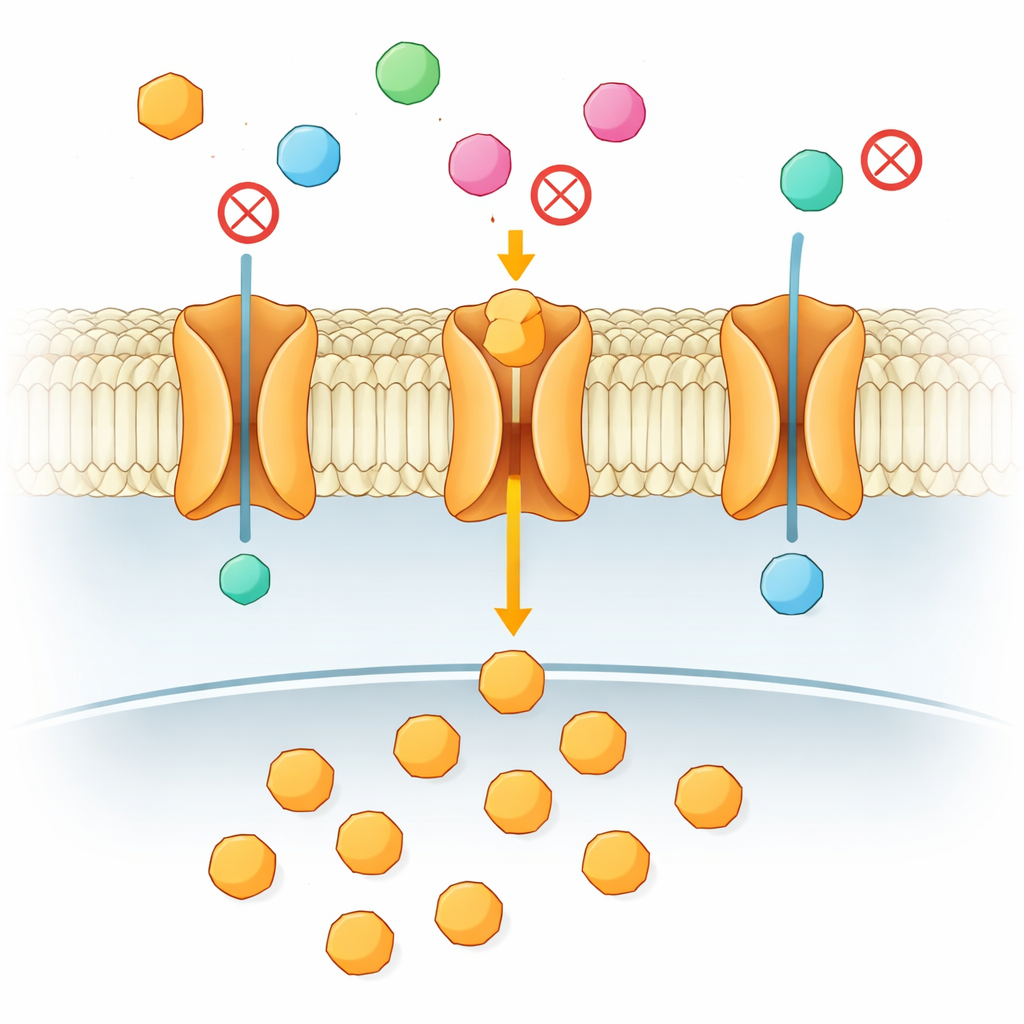
Warum sich ähnliche Zucker so unterschiedlich verhalten
Beim Menschen gibt es 14 eng verwandte Glukosetransporter, die an der Bindestelle sehr ähnlich aussehen. Dennoch transportieren sie unterschiedliche Zucker mit unterschiedlichen Geschwindigkeiten und sind mit Erkrankungen von Diabetes bis Krebs verbunden. Um dieses Rätsel zu lösen, untersuchten die Autoren einen bakteriellen Verwandten menschlicher Transporter, ein Protein namens XylE. XylE befördert den Zucker Xylose, bindet aber Glukose mit nahezu gleicher Stärke, obwohl Glukose nicht durchpasst und stattdessen das Tor verstopft. Dieses ungewöhnliche Verhalten macht XylE zu einem idealen Modell, um zu fragen, was wirklich einen transportierten Zucker von einem unterscheidet, der nur das System blockiert.
Zucker mithilfe der Magnetresonanz abhören
Das Team verwendete eine Methode der Magnetresonanz namens Saturation Transfer Difference (STD) NMR als eine Art „Stethoskop“ für Zucker–Transporter-Begegnungen. Sie rekonstruierten gereinigte Transporter in winzigen künstlichen Membranen, sogenannten Liposomen, um die natürliche Umgebung nachzuahmen. Bei STD NMR nehmen nur Zuckermoleküle, die lange genug in der Nähe des Proteins verweilen, ein nachweisbares Signal auf. Überraschenderweise zeigte XylE starke Signale mit Xylose, seinem natürlichen Frachtstoff, aber nahezu keine mit Glukose, obwohl beide Zucker binden. Wenn die Forscher XylE genetisch so blockierten, dass es seine Form nicht mehr ändern und nicht mehr transportieren konnte, verschwand das Xylose-Signal praktisch. Umgekehrt erschienen starke Glukose-Signale, wenn sie XylE so veränderten, dass es Glukose transportieren konnte. Mit anderen Worten: Nur Zucker–Transporter-Paare, die die Reise durch die Membran tatsächlich vollenden, geben in diesem Experiment ein Signal.
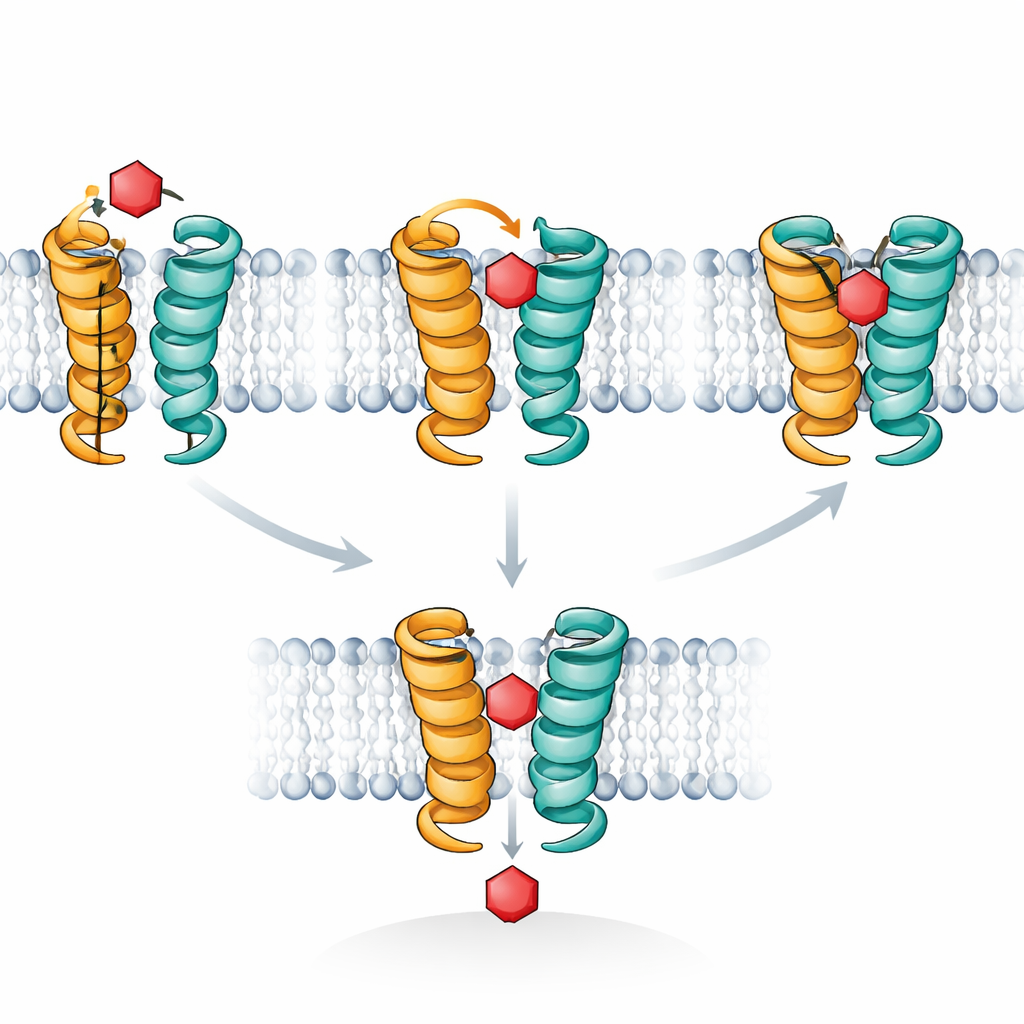
Ein verborgenes Zwischenstadium auf der Reise
Computersimulationen lieferten einen molekularen Film zur Erklärung dieser Beobachtungen. XylE, wie auch menschliche Glukosetransporter, arbeitet, indem es zwischen Formen wechselt, die abwechselnd nach außen und nach innen geöffnet sind, mit einem dazwischenliegenden „okkludierten“ Zustand, in dem der Zucker von beiden Seiten abgeriegelt ist. Die Autoren konzentrierten sich auf ein kurzes Helixsegment, genannt TM7b, das als äußeres Tor fungiert. Ihre Simulationen zeigten, dass, wenn Xylose in genau der richtigen Pose sitzt, TM7b vollständig zuschlagen kann und so den tief okkludierten Zustand stabilisiert, in dem der Zucker eng umschlossen ist. Glukose hingegen neigt dazu zu wackeln und treibt TM7b nie konsequent zu diesem vollständigen Verschluss; sie bleibt in einer flacheren, außen-okkludierten Pose stecken, die den Weg blockiert, ohne den Transport abzuschließen. Die STD-NMR-Signale spiegeln genau diesen Unterschied wider, wie lange Zucker in der vollständig okkludierten, hochkontaktieren Konfiguration verweilen.
Lehren aus einem Malaria-Transporter und einem Fruktose-Spezialisten
Um zu prüfen, ob dieses Prinzip über XylE hinaus gilt, betrachteten die Forscher PfHT1, einen Zuckertransporter des Malaria-Parasiten, der sowohl Glukose als auch Fruktose bewegen kann, und das Säugetierprotein GLUT5, einen Fruktose-Spezialisten im Darm. Mithilfe von STD NMR, Kristallstrukturen, Kryo-Elektronenmikroskopie und weiteren Simulationen fanden sie heraus, dass auch diese Transporter TM7b nutzen, um Zucker während des okkludierten Schritts zu koordinieren. Eine einzelne Asparagin-Aminosäure in TM7b spielt eine zentrale Rolle, indem sie beim Schließen des Tores Kontakt zu wichtigen Hydroxylgruppen am Zucker erhält. In PfHT1 fing eine hochauflösende Kryo-EM-Aufnahme eine „halbwegs“ nach innen-okkludierte Pose ein, in der der Zucker nur teilweise koordiniert ist; eine zuvor bestimmte Kristallstruktur zeigte die vollständig okkludierte Pose. Der Vergleich der beiden zeigte, dass sich der Zucker nur um etwa zwei Milliardstel Meter verschiebt, dabei aber ein Netzwerk zusätzlicher Kontakte aufbaut, die die übergangszustandsähnliche okkludierte Form deutlich enger binden.
Transporter als winzige Enzyme
Aus allen Befunden schlagen die Autoren vor, dass Zuckerporter ähnlich wie Enzyme funktionieren, wobei die Spezifität nicht durch den ersten Bindungsschritt bestimmt wird, sondern dadurch, wie gut ein Zucker in einen flüchtigen Übergangszustand passt. Transporter flimmern spontan in außen- und innen-okkludierte Formen, auch ohne Zucker. Ein kompatibler Zucker „wählt“ zunächst eine dieser vorexistierenden Posen (konformationelle Selektion) und löst dann ein abschließendes Festziehen des Tores zu einem vollständig okkludierten Zustand (induzierte Anpassung) aus, das das Protein verpflichtet, umzuschlagen und den Zucker auf der anderen Seite freizusetzen. Ungeeignete Zucker können zwar binden, manchmal stark, schaffen es aber nicht, diesen letzten Verschluss auszulösen, sodass sie als Inhibitoren statt als Fracht wirken. Die Erkenntnis, dass der okkludierte Zustand der eigentliche Entscheidungspunkt ist, eröffnet neue Möglichkeiten, Wirkstoffe zu entwerfen, die Transporter in einer übergangszustandsähnlichen Pose einfrieren und so möglicherweise Krebszellen oder Parasiten durch Blockade ihrer Zuckerzufuhr aushungern.
Zitation: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Schlüsselwörter: Glukosetransporter, Zuckertranslokation, Membranproteine, STD NMR, Spezifität des Übergangszustands