Clear Sky Science · pt
Um mecanismo em duas etapas para a translocação de açúcares
Como as células escolhem o açúcar certo
Cada célula do seu corpo depende de um suprimento constante de açúcar para obter energia, especialmente o cérebro e tecidos que crescem rapidamente, como tumores. Esse açúcar precisa atravessar uma membrana celular lipídica, e o faz por meio de “portões” especializados chamados transportadores. Este artigo explora uma pergunta aparentemente simples com grandes implicações médicas: quando muitos açúcares semelhantes estão presentes, como um transportador decide quais deixar passar e quais bloquear? A resposta não está no primeiro contato entre açúcar e proteína, mas numa dança sutil em duas etapas no interior da membrana. 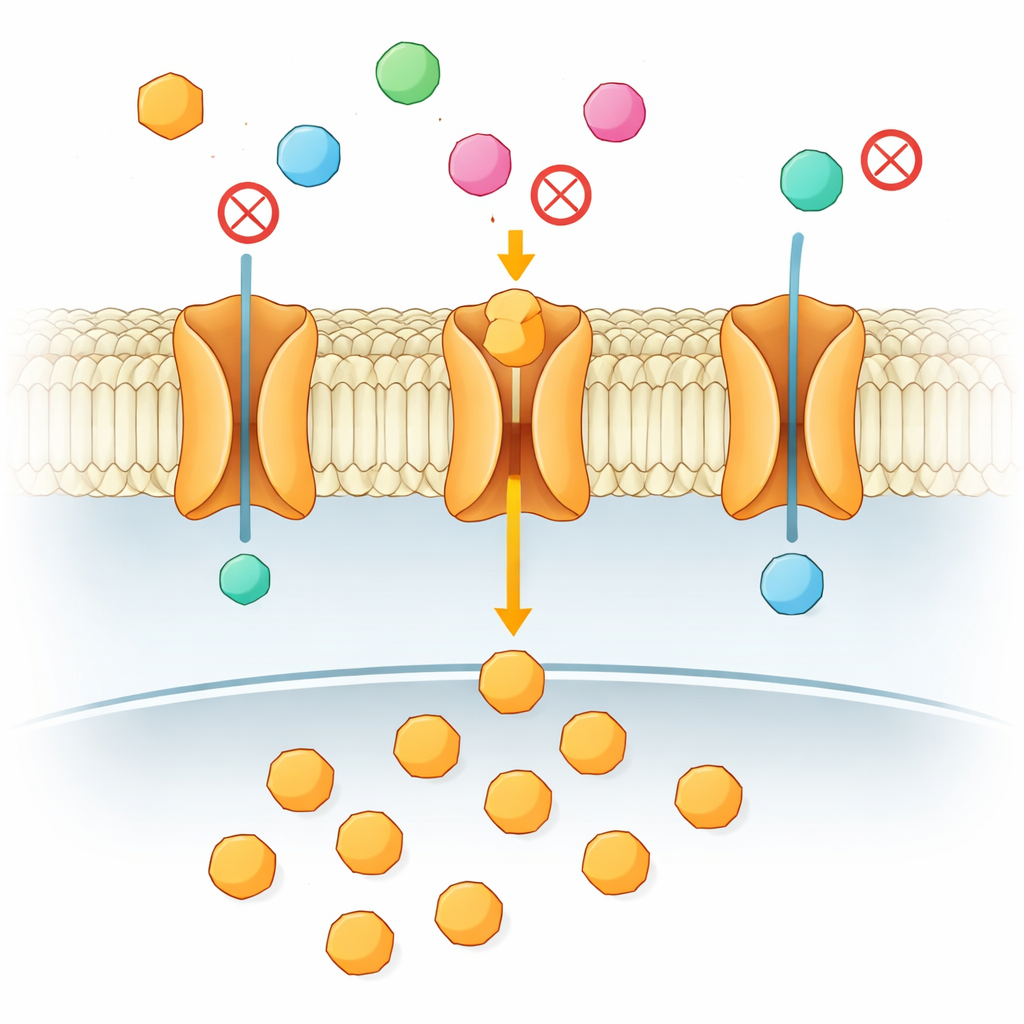
Por que açúcares semelhantes se comportam tão diferente
Em humanos existem 14 transportadores de glicose intimamente relacionados que parecem notavelmente iguais no ponto onde o açúcar se liga. Ainda assim, eles movem açúcares distintos em velocidades diferentes e estão associados a condições que vão desde diabetes até câncer. Para desvendar esse enigma, os autores recorreram a um parente bacteriano dos transportadores humanos, uma proteína chamada XylE. XylE transporta o açúcar xilose, mas se liga à glicose com quase a mesma afinidade, embora a glicose não consiga atravessar e, em vez disso, entupa o portão. Esse comportamento estranho torna XylE um modelo ideal para perguntar o que realmente distingue um açúcar transportado de um que simplesmente trava o sistema.
Ouvindo os açúcares com ressonância magnética
A equipe usou um método de ressonância magnética conhecido como saturation transfer difference (STD) NMR como uma espécie de “estetoscópio” para os encontros açúcar–transportador. Eles reconstituíram transportadores purificados em pequenas membranas artificiais chamadas lipossomos, imitando o ambiente natural. No STD NMR, apenas moléculas de açúcar que permanecem perto da proteína tempo suficiente captam um sinal detectável. A descoberta surpreendente foi que XylE produziu sinais fortes com xilose, sua carga natural, mas quase nenhum com glicose, mesmo que ambos os açúcares se liguem. Quando os pesquisadores geneticamente travaram o XylE de modo que ele não pudesse mais mudar de forma e transportar, o sinal de xilose praticamente desapareceu. Por outro lado, quando engenheiraram o XylE para ganhar a capacidade de mover glicose, surgiram sinais fortes de glicose. Em outras palavras, apenas pares açúcar–transportador que completam efetivamente a travessia da membrana acendem neste experimento. 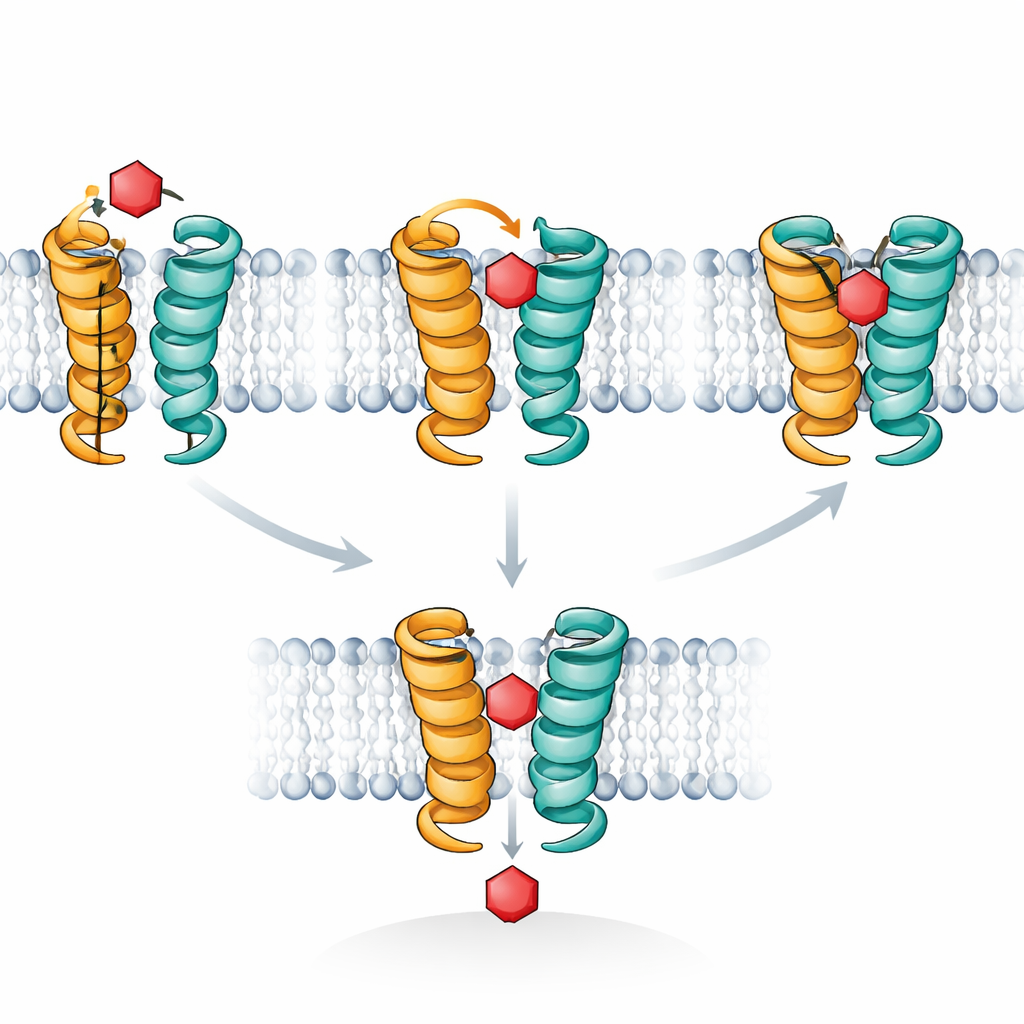
Um passo intermediário oculto na jornada
Simulações por computador forneceram um filme molecular para explicar essas observações. XylE, como os transportadores humanos de glicose, funciona ciclindando por formas que se abrem alternativamente para fora e para dentro da célula, com um estado intermediário “ocluído” onde o açúcar fica isolado de ambos os lados. Os autores focaram num curto segmento helicoidal, chamado TM7b, que atua como um portão externo. Suas simulações mostraram que quando a xilose se posiciona exatamente certo, o TM7b pode fechar totalmente, estabilizando o estado profundamente ocluído onde o açúcar é fortemente abraçado. A glicose, em contraste, tende a oscilar e nunca força consistentemente o TM7b a completar esse fechamento; ela permanece presa numa pose mais rasa, ocluída para fora, que bloqueia o caminho sem finalizar o transporte. Os sinais de STD NMR acompanham exatamente essa diferença em quanto tempo os açúcares permanecem na configuração totalmente ocluída e de alto contato.
Lições de um transportador da malária e de um especialista em frutose
Para ver se esse princípio vale além do XylE, os pesquisadores voltaram-se para PfHT1, um transportador de açúcares do parasita da malária que pode mover tanto glicose quanto frutose, e para a GLUT5 mamífera, um especialista em frutose no intestino. Usando STD NMR, estruturas por cristalografia, criomicroscopia eletrônica e simulações adicionais, eles descobriram que esses transportadores também dependem do TM7b para coordenar os açúcares durante o passo ocluído. Uma única asparagina no TM7b desempenha papel central, contactando grupos hidroxila-chave no anel do açúcar à medida que o portão se fecha. Em PfHT1, uma imagem de alta resolução por crio-EM capturou uma pose “pela metade”, ocluída para dentro, onde o açúcar está apenas parcialmente coordenado; uma estrutura cristalográfica previamente determinada registrou a pose totalmente ocluída. Comparar as duas mostrou o açúcar deslocando-se por apenas cerca de dois bilionésimos de metro, mas formando uma rede de contatos adicionais que torna a forma ocluída, semelhante a um estado de transição, muito mais firmemente ligada.
Transportadores como pequenas enzimas
Juntando todas as evidências, os autores propõem que os portadores de açúcar funcionam muito como enzimas, com especificidade governada não pelo primeiro passo de ligação, mas por quão bem um açúcar se ajusta a um estado de transição efêmero. Transportadores piscam espontaneamente em formas ocluídas para fora e para dentro mesmo sem açúcar. Um açúcar compatível primeiro “escolhe” uma dessas poses pré-existentes (seleção conformacional), então desencadeia um apertamento final do portão numa forma totalmente ocluída (ajuste induzido) que compromete a proteína a virar e liberar o açúcar do outro lado. Açúcares incompatíveis ainda podem se ligar, às vezes fortemente, mas não conseguem impulsionar esse último aperto, atuando assim como inibidores em vez de carga. Reconhecer que o estado ocluído é o verdadeiro ponto de decisão sugere novas maneiras de projetar fármacos que congelem transportadores numa pose semelhante a um estado de transição, potencialmente privando células cancerosas ou parasitas ao bloquear seu suprimento de açúcar.
Citação: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Palavras-chave: transportadores de glicose, translocação de açúcares, proteínas de membrana, STD NMR, especificidade do estado de transição