Clear Sky Science · ru
Двухэтапный механизм переноса сахара
Как клетки выбирают подходящий сахар
Каждая клетка в вашем организме зависит от постоянного поступления сахара для получения энергии, особенно мозг и быстро растущие ткани, такие как опухоли. Этот сахар должен пересечь липидную мембрану клетки, и делает он это через специализированные «ворота», называемые переносчиками. В этой статье рассматривается на первый взгляд простой вопрос с серьезными медицинскими последствиями: когда одновременно присутствует много похожих сахаров, как переносчик решает, какие пропустить, а какие заблокировать? Оказалось, что ответ не кроется в первом прикосновении сахара к белку, а в тонком двухэтапном танце глубоко внутри мембраны. 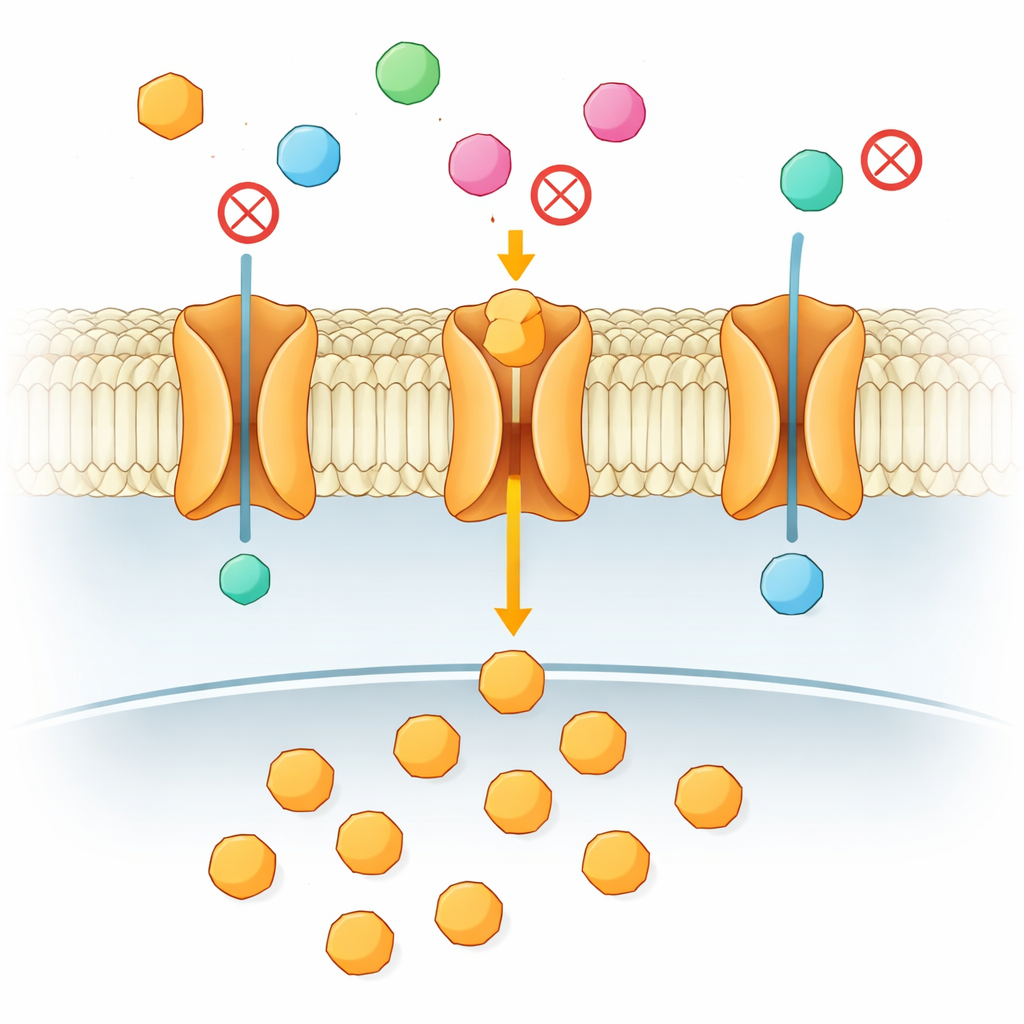
Почему похожие сахара ведут себя так по‑разному
У человека есть 14 тесно родственных транспортёров глюкозы, которые выглядят удивительно похоже в области, где собственно и связывается сахар. Тем не менее они переносят разные сахара с разной скоростью и связаны с состояниями от диабета до рака. Чтобы разобраться в этой загадке, авторы обратились к бактериальному «кузину» человеческих переносчиков, белку под названием XylE. XylE транспортирует ксилозу, но связывает глюкозу с почти такой же силой, хотя глюкоза не проходит и вместо этого забивает ворота. Такое странное поведение делает XylE идеальной моделью для выяснения того, что на самом деле отличает транспортируемый сахар от того, который просто засоряет систему.
Слушая сахара с помощью магнитного резонанса
Команда использовала метод магнитного резонанса, известный как saturation transfer difference (STD) NMR, как своего рода «стетоскоп» для контактов сахар–переносчик. Они реконституировали очищенные переносчики в крошечных искусственных мембранах — липосомах, имитируя естественную среду. В STD NMR только молекулы сахара, которые задерживаются достаточно близко к белку, получают обнаруживаемый сигнал. Удивительным оказалось то, что XylE давал сильные сигналы с ксилозой, своим природным грузом, но почти не давал сигналов с глюкозой, хотя обе молекулы связываются. Когда исследователи генетически зафиксировали XylE так, что он больше не мог менять форму и транспортировать, сигнал от ксилозы практически исчез. И наоборот: когда они модифицировали XylE, чтобы он приобрёл способность переносить глюкозу, появились сильные сигналы от глюкозы. Иными словами, в этом эксперименте «светятся» только пары сахар–переносчик, которые действительно завершают переход через мембрану. 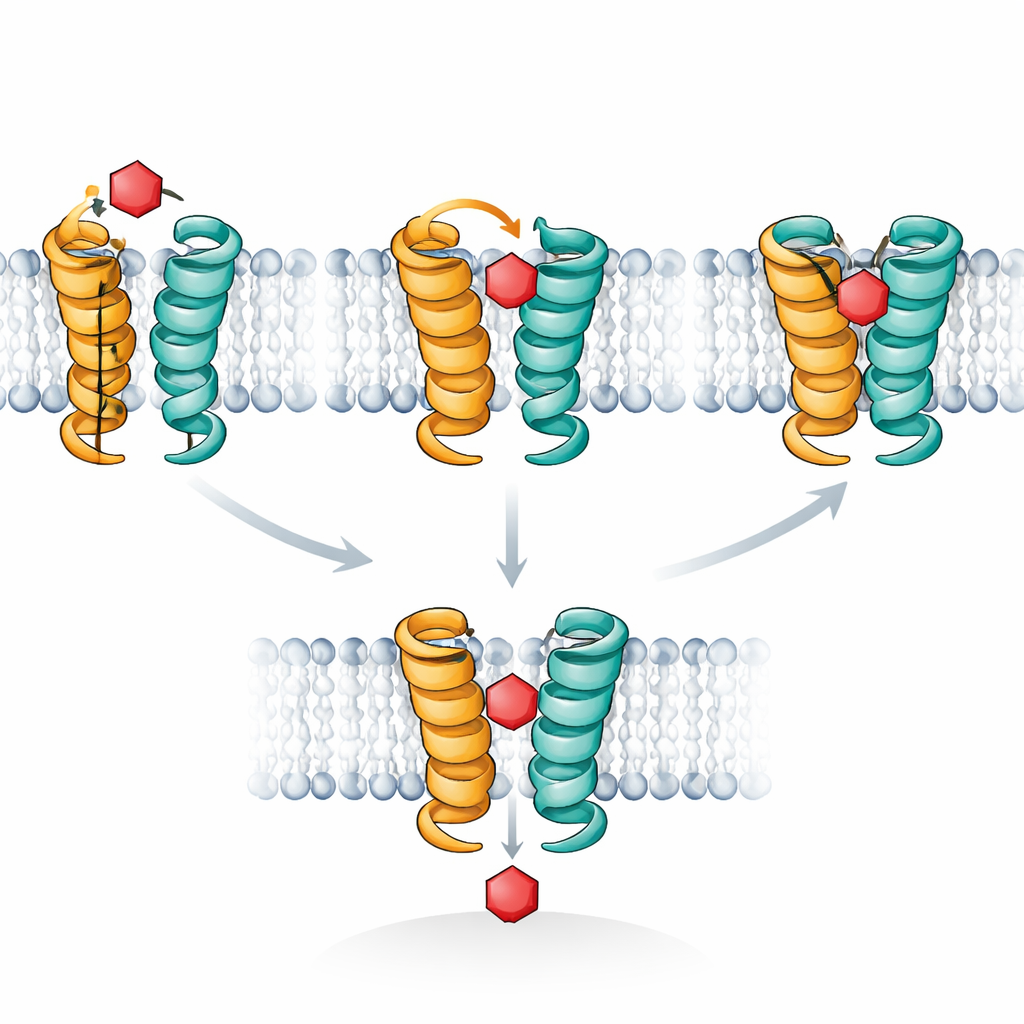
Скрытый промежуточный этап в путешествии
Компьютерные симуляции предоставили молекулярный фильм, объясняющий эти наблюдения. XylE, как и человеческие переносчики глюкозы, работает, циклично меняя формы, которые поочередно открываются наружу и внутрь клетки, с промежуточным «окклюдированным» состоянием, в котором сахар заперт от обеих сторон. Авторы сосредоточились на коротком спиральном участке, называемом TM7b, который действует как внешняя заслонка. Симуляции показали, что когда ксилоза занимает именно ту позу, TM7b может полностью захлопнуться, стабилизируя глубоко окклюдированное состояние, в котором сахар плотно охвачен. Глюкоза, напротив, склонна к колебаниям и не вызывает устойчивого закрытия TM7b; она остаётся в более мелком, наружно‑окклюдированном положении, которое блокирует путь, не завершая транспорт. Сигналы STD NMR точно отражают эту разницу во времени нахождения сахаров в полностью окклюдированном конфигурации с большим числом контактов.
Уроки от переносчика малярии и специалиста по фруктозе
Чтобы проверить, справедливо ли это за пределами XylE, исследователи обратились к PfHT1 — транспортёру сахаров из паразита малярии, который может переносить и глюкозу, и фруктозу, и к млекопитающему GLUT5 — специализированному переносчику фруктозы в кишечнике. С помощью STD NMR, рентгеноструктур, крио‑электронной микроскопии и дополнительных симуляций они обнаружили, что эти переносчики также полагаются на TM7b для координации сахаров в окклюдированном шаге. Одна аспарагиновая аминокислота в TM7b играет центральную роль, контактируя с ключевыми гидроксильными группами на кольце сахара по мере закрывания заслонки. В PfHT1 высокоразрешающее крио‑ЭМ изображение зафиксировало «полупромежуточную» внутрь‑окклюдированную позу, где сахар лишь частично скоординирован; ранее полученная рентгеноструктура запечатлела полностью окклюдированное состояние. Сравнение двух состояний показало, что сахар сместился всего на порядка двух миллиардных метра, но приобрёл сеть дополнительных контактов, делающих переходное, окклюдированное состояние значительно более плотно связанным.
Переносчики как крошечные ферменты
Собрав все данные воедино, авторы предлагают рассматривать портёры сахара подобно ферментам, где специфичность определяется не первым шагом связывания, а тем, насколько хорошо сахар подходит для мимолётного переходного состояния. Переносчики спонтанно фликерят в наружные и внутренние окклюдированные формы даже без сахара. Совместимый сахар сначала «выбирает» одну из этих заранее существующих поз (конформационный отбор), затем вызывает окончательное затягивание заслонки в полностью окклюдированное состояние (индуцированный пригон), что обязывает белок перевернуться и освободить сахар по другую сторону. Несовместимые сахара всё ещё могут связываться, иногда сильно, но не способны привести к этому последнему затягиванию, поэтому они действуют как ингибиторы, а не как груз. Осознание того, что именно окклюдированное состояние — настоящий момент принятия решения, открывает новые пути для разработки препаратов, которые замораживают переносчики в переходоподобной позе, потенциально лишая раковые клетки или паразитов источника сахара.
Цитирование: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Ключевые слова: транспортёры глюкозы, перенос сахара, мембранные белки, STD NMR, специфичность переходного состояния