Clear Sky Science · es
Un mecanismo en dos pasos para la translocación de azúcares
Cómo las células eligen el azúcar correcto
Cada célula de tu cuerpo depende de un suministro constante de azúcares para obtener energía, especialmente el cerebro y los tejidos de rápido crecimiento como los tumores. Ese azúcar debe atravesar una membrana celular grasa, y lo hace mediante “puertas” especializadas llamadas transportadores. Este artículo explora una pregunta aparentemente simple con grandes implicaciones médicas: cuando hay muchos azúcares similares presentes, ¿cómo decide un transportador cuáles dejar pasar y cuáles bloquear? La respuesta resulta no residir en el primer contacto entre azúcar y proteína, sino en una sutil danza en dos pasos en lo profundo de la membrana. 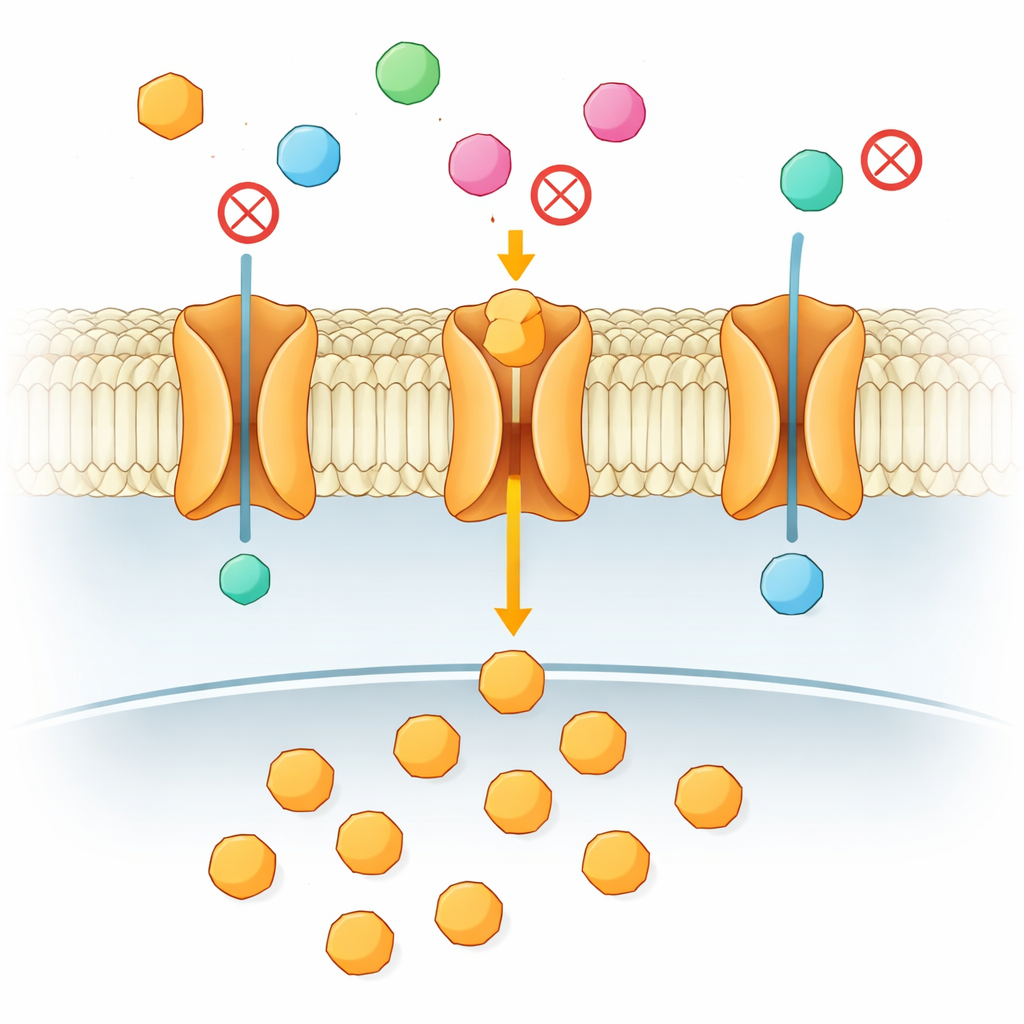
Por qué azúcares similares se comportan de forma tan distinta
En humanos hay 14 transportadores de glucosa estrechamente relacionados que se parecen notablemente en el lugar donde realmente se une el azúcar. Sin embargo, mueven distintos azúcares a diferentes velocidades y están asociados a afecciones que van desde la diabetes hasta el cáncer. Para desenmarañar este rompecabezas, los autores recurrieron a un pariente bacteriano de los transportadores humanos, una proteína llamada XylE. XylE transporta la xilosa pero se une a la glucosa con casi la misma afinidad, aunque la glucosa no puede atravesar y en su lugar atasca la puerta. Ese comportamiento extraño convierte a XylE en un modelo ideal para preguntar qué distingue realmente a un azúcar transportado de otro que simplemente bloquea el sistema.
Escuchar azúcares con resonancia magnética
El equipo utilizó un método de resonancia magnética conocido como saturación de transferencia por diferencia (STD NMR) como una especie de “estetoscopio” para los encuentros azúcar–transportador. Reconstituyeron transportadores purificados en pequeñas membranas artificiales llamadas liposomas, imitando el entorno natural. En STD NMR, solo las moléculas de azúcar que permanecen cerca de la proteína el tiempo suficiente adquieren una señal detectable. El hallazgo sorprendente fue que XylE produjo señales fuertes con xilosa, su carga natural, pero casi ninguna con glucosa, a pesar de que ambos azúcares se unen. Cuando los investigadores bloquearon genéticamente XylE para que ya no pudiera cambiar de forma y transportar, la señal de xilosa prácticamente desapareció. Por el contrario, cuando diseñaron XylE para que adquiriera la capacidad de mover glucosa, aparecieron señales fuertes de glucosa. En otras palabras, solo los pares azúcar–transportador que realmente completan el recorrido a través de la membrana se iluminan en este experimento. 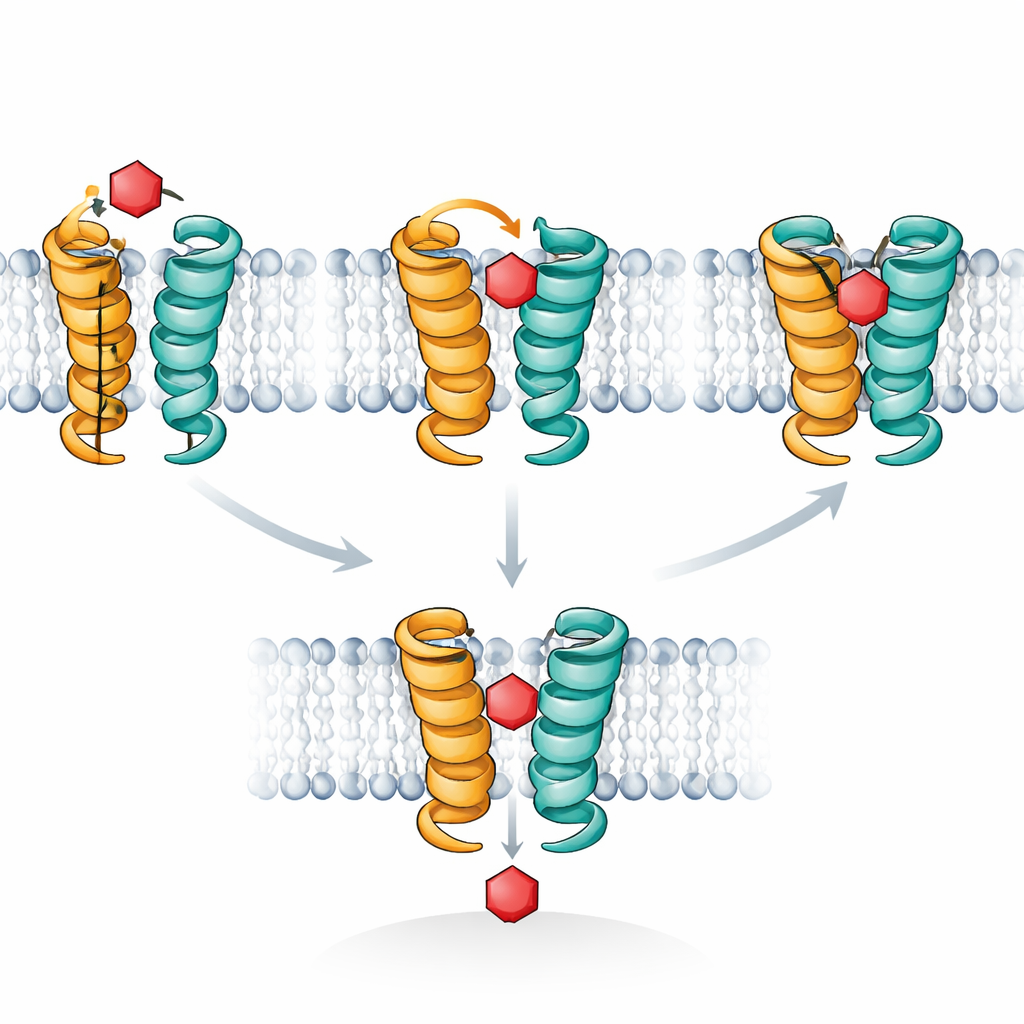
Un paso intermedio oculto en el viaje
Las simulaciones por ordenador proporcionaron una película molecular para explicar estas observaciones. XylE, como los transportadores de glucosa humanos, funciona ciclando entre formas que se abren alternativamente al exterior y al interior de la célula, con un estado intermedio “ocluido” donde el azúcar queda aislado de ambos lados. Los autores se centraron en un segmento helicoidal corto, llamado TM7b, que actúa como una compuerta exterior. Sus simulaciones mostraron que cuando la xilosa se sitúa en la pose adecuada, TM7b puede cerrarse completamente, estabilizando el estado profundamente ocluido donde el azúcar queda fuertemente abrazado. La glucosa, en contraste, tiende a tambalearse y nunca impulsa de forma constante a TM7b a completar ese cierre; permanece atrapada en una pose ocluida hacia afuera más superficial que bloquea el camino sin terminar el transporte. Las señales de STD NMR siguen exactamente esta diferencia en cuánto tiempo los azúcares habitan la configuración totalmente ocluida y de alto contacto.
Lecciones de un transportador de la malaria y de un especialista en fructosa
Para ver si este principio se sostiene más allá de XylE, los investigadores estudiaron PfHT1, un transportador de azúcares del parásito de la malaria que puede mover tanto glucosa como fructosa, y GLUT5 de mamíferos, un especialista en fructosa del intestino. Usando STD NMR, estructuras cristalográficas, crio-microscopía electrónica y más simulaciones, encontraron que estos transportadores también dependen de TM7b para coordinar los azúcares durante el paso ocluido. Un único aminoácido asparagina en TM7b juega un papel central, contactando grupos hidroxilo clave del anillo de azúcar mientras la puerta se cierra. En PfHT1, una instantánea de alta resolución por crio-EM capturó una pose “a medio camino” ocluida hacia el interior en la que el azúcar está solo parcialmente coordinado; una estructura cristalográfica previamente determinada mostró la pose totalmente ocluida. Comparar ambas mostró que el azúcar se desplaza solo en torno a dos milmillonésimas de metro, pero adquiere una red de contactos adicionales que hace que la forma ocluida, similar a un estado de transición, quede mucho más fuertemente ligada.
Transportadores como pequeñas enzimas
Reuniendo todas las pruebas, los autores proponen que los portadores de azúcares operan de manera muy parecida a las enzimas, con una especificidad gobernada no por el primer paso de unión sino por qué tan bien encaja un azúcar en un efímero estado de transición. Los transportadores parpadean espontáneamente entre formas ocluidas hacia afuera y hacia adentro incluso sin azúcar. Un azúcar compatible primero “elige” una de estas poses preexistentes (selección conformacional), luego desencadena un ajuste final de la compuerta hacia una forma totalmente ocluida (ajuste inducido) que compromete a la proteína a voltearse y liberar el azúcar al otro lado. Los azúcares incompatibles aún pueden unirse, a veces con fuerza, pero no logran impulsar ese último apretamiento, por lo que actúan como inhibidores en lugar de como carga. Reconocer que el estado ocluido es el verdadero punto de decisión sugiere nuevas formas de diseñar fármacos que congelen a los transportadores en una pose similar a la de transición, potencialmente privando de azúcar a células cancerosas o parásitos al bloquear su suministro.»
Cita: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
Palabras clave: transportadores de glucosa, translocación de azúcares, proteínas de membrana, STD NMR, especificidad del estado de transición