Clear Sky Science · ja
糖の移送における二段階メカニズム
細胞はどの糖を選ぶか
体内のあらゆる細胞は、特に脳や腫瘍のような急速に増殖する組織にとって、エネルギー源として安定した糖の供給に依存しています。その糖は脂質性の細胞膜を横切らねばならず、輸送体と呼ばれる特殊な「ゲート」を通って移動します。本稿は、似たような糖が多数存在するときに輸送体がどの糖を通し、どれを遮断するかをどう決めるのかという、一見単純だが医療的に重要な問いを探ります。答えは糖とタンパク質の最初の接触にあるのではなく、膜の深部で起こる微妙な二段階のダンスにあることがわかりました。 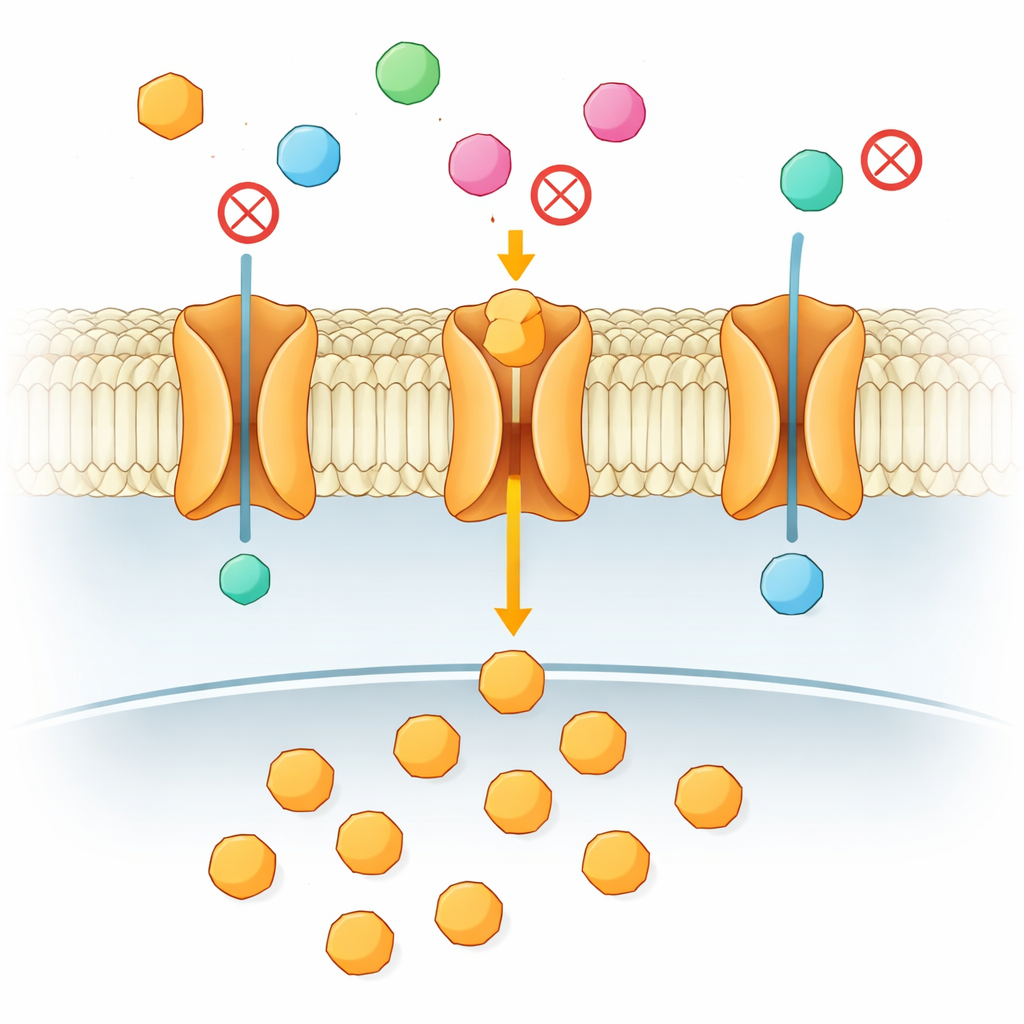
似た糖が異なる振る舞いを示す理由
ヒトには14種類の密接に関連したグルコース輸送体があり、糖が実際に結合する部位は非常によく似ています。それでもそれぞれが異なる糖を異なる速度で運び、糖尿病からがんまでさまざまな状態と結びついています。この謎を解くために、著者らはヒト輸送体の細菌性の近縁体であるXylEというタンパク質に注目しました。XylEはキシロースを輸送しますが、グルコースとほぼ同等の強さで結合する一方で、グルコースは通過できずゲートを詰まらせます。その奇妙な振る舞いは、輸送される糖と単に詰まらせる糖を区別する要因を問う理想的なモデルになります。
磁気共鳴で糖に“耳を傾ける”
チームは飽和伝達差(STD)NMRという磁気共鳴法を、糖—輸送体の出会いを聴く“聴診器”として用いました。精製した輸送体をリポソームと呼ばれる小さな人工膜に再構成し、自然な環境を模しました。STD NMRでは、タンパク質の近くに十分長くとどまる糖分子だけが検出可能な信号を受け取ります。驚くべき発見は、XylEが本来の基質であるキシロースでは強い信号を出すのに対し、グルコースではほとんど信号が出ないことでした(両者は結合するにもかかわらず)。研究者がXylEを遺伝的に固定して形を変えられず輸送できないようにすると、キシロースの信号はほぼ消えました。逆に、グルコースを動かす能力をXylEに獲得させると、強いグルコース信号が現れました。言い換えれば、この実験で光るのは実際に膜を横切る旅を完遂する糖—輸送体の組み合わせだけだったのです。 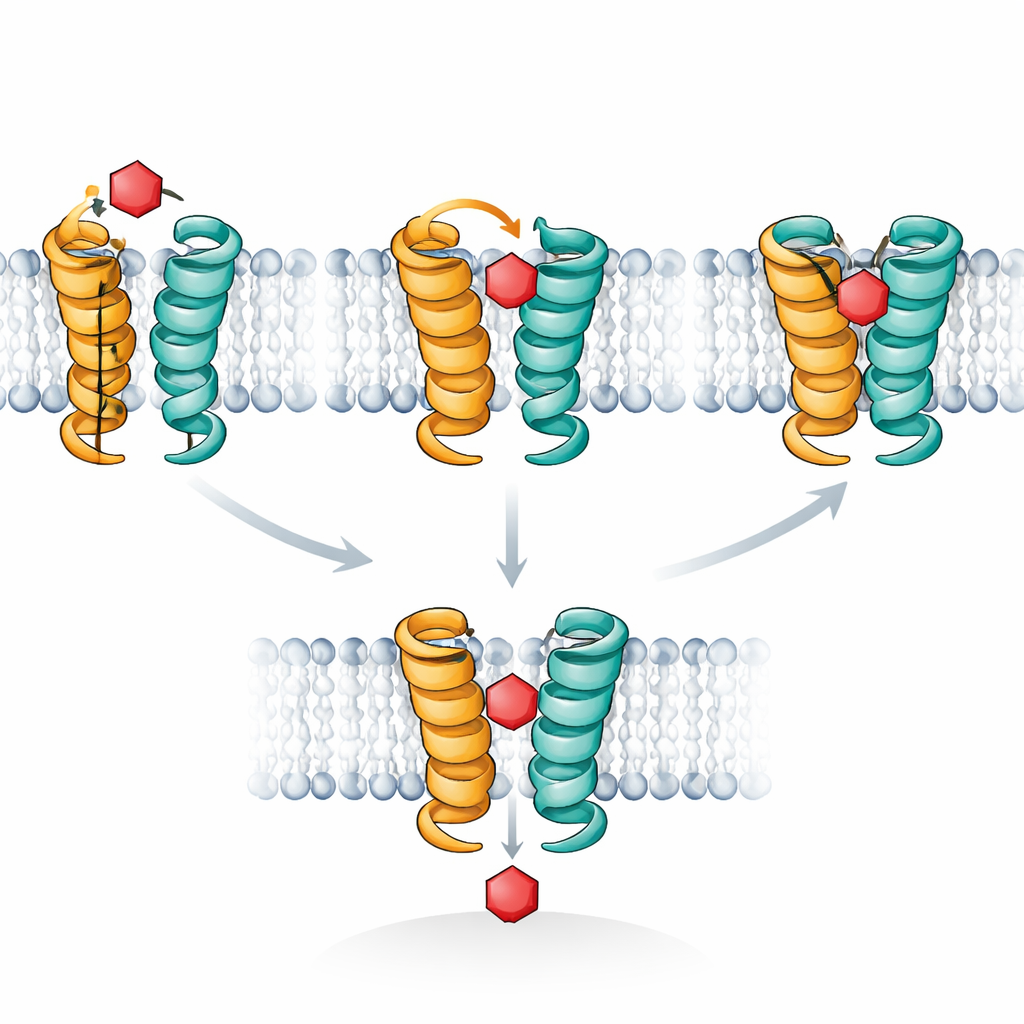
旅路に隠れた中間段階
コンピュータシミュレーションはこれらの観察を説明する分子の映画を提供しました。XylEはヒトのグルコース輸送体と同様に、外側と内側に交互に開く形へとサイクルし、その中間に糖が両側から遮断される「閉塞(オクルード)状態」があります。著者らは外側のゲートとして働く短いヘリカルセグメント、TM7bに注目しました。シミュレーションは、キシロースがちょうど適切な姿勢で位置するとTM7bが完全に閉じることができ、糖が深く閉塞された状態で強く抱え込まれることを示しました。これに対してグルコースは揺らぎやすく、TM7bを一貫して完全閉鎖へ駆動することはなく、浅い外向き閉塞状態に留まりがちで、輸送を完了しないまま経路を塞いでしまいます。STD NMRの信号は、糖が完全に閉塞した高接触構成でどれだけ長く留まるかという差と正確に対応していました。
マラリア輸送体とフルクトース専門輸送体からの教訓
この原理がXylEに限られないかを調べるため、研究者らはマラリア原虫由来でグルコースとフルクトースの両方を運ぶPfHT1と、腸にあるフルクトース専門の哺乳類GLUT5に目を向けました。STD NMR、結晶構造、クライオ電子顕微鏡、さらなるシミュレーションを用いて、これらの輸送体も閉塞段階で糖を協調するためにTM7bを利用していることが明らかになりました。TM7bの中の単一のアスパラギン残基が中心的な役割を果たし、ゲートが閉じる際に糖環の重要なヒドロキシル基と接触します。PfHT1では高分解能のクライオEMスナップショットが糖が部分的にしか協調されていない“途中”の内向き閉塞姿勢をとらえ、以前の結晶構造が完全閉塞姿勢を捉えていました。両者を比較すると糖の移動はわずか約2ナノメートルの数分の一(注:本文では約2ギガ分のメートル=2×10^-9 m)にすぎませんが、遷移状態様の閉塞形に移ると追加の接触ネットワークを獲得し、はるかに強く結合するようになります。
輸送体は小さな酵素のように振る舞う
すべての証拠を総合すると、著者らは糖ポーターが酵素とよく似た働きをし、特異性は最初の結合段階ではなく一時的な遷移状態にどれだけ適合するかによって支配されると提案します。輸送体は糖がなくても自発的に外向き・内向きの閉塞形にちらつきます。適合する糖はまずこれらの既存の姿勢の一つを“選ぶ”(立体選択)、ついでゲートが最終的に締まって完全閉塞状態になる(誘導適合)ことでタンパク質が反転して糖を反対側に放出することにコミットします。不適合な糖は強く結合することもありますが、この最後の締め付けを駆動できないため、貨物ではなく阻害剤として振る舞います。閉塞状態が真の判断点であると認識することで、輸送体を遷移様の姿勢で固定する薬剤の設計といった新たな方法が示唆され、がん細胞や寄生虫の糖供給を遮断して飢餓状態に追い込む可能性があります。
引用: Ahn, DH., Alleva, C., Reichenbach, T. et al. A two-step mechanism for sugar translocation. Nat Struct Mol Biol 33, 652–663 (2026). https://doi.org/10.1038/s41594-026-01784-w
キーワード: グルコース輸送体, 糖の移送, 膜タンパク質, STD NMR, 遷移状態特異性