Clear Sky Science · tr
Tek Bir Derin Öğrenme Modeli Kullanılarak Standart LC-MS İş Akışlarına Alternatif Parçalanma Tekniklerinin Entegrasyonu, Proteom Kapsamını Genişletir
Yaşamın Protein Makinelerini Daha Fazla Görmek
Vücudunuzdaki her hücre, her biri belirli bir görevi yürüten binlerce farklı proteinle doludur. Modern kütle spektrometrisi, proteinleri parçalara ayırıp bu parçaların kütlelerini ölçerek birçok proteini zaten okuyabiliyor, ancak sıra dışı protein formları ve sağlığı veya hastalığı etkileyen ince kimyasal değişiklikler gibi önemli bölümler hâlâ görünmez kalıyor. Bu çalışma, birkaç gelişmiş parçalanma yöntemini tek bir yapay zeka modeliyle birleştirmenin yeni bir yolunu tanımlayarak, bilim insanlarının rutin bir deneyde protein dünyasını çok daha geniş bir biçimde görmesini sağlıyor.
Proteinler Genellikle Nasıl Okunur
Çoğu laboratuvarda proteinler önce peptit adı verilen daha küçük parçacıklara doğranır ve ardından bunlar ayrıştırıp tartan bir cihaza verilir. Her peptidin dizisini belirlemek için cihaz bu parçaları kasıtlı olarak parçalar ve kırıntı desenlerini kaydeder; bir vazoyu kırıp parçalarından şeklini çıkarmaya benzer. Yıllardır, peptitlerin gaz molekülleriyle çarpıştırılarak parçalandığı çarpışma tabanlı yöntem, hızlı, sağlam ve yazılım desteği iyi olduğundan ana yöntem oldu. Ancak bu standart yaklaşım, hassas kimyasal işaretleri korumakta zorlanır ve karmaşık protein formlarının bazı bölümlerini kaçırır; bu da biyolojiyi anlama konusunda kör noktalar bırakır.
Proteinleri Parçalamanın Yeni Yolları
Araştırmacılar peptitleri kırmak için ultraviyole ışık veya elektron demetleri gibi farklı yollar geliştirdi; bunlar proteinleri farklı yollarla keser ve çoğu zaman kırılgan özellikleri korur. Bu yaklaşımlar daha zengin ve bilgi verici kırık desenleri üretebilir, ancak daha yavaştır, teknik açıdan zordur ve veri analiz araçları tarafından zayıf desteklenir. Bunu ele almak için yazarlar, çarpışma-, elektron- ve foton tabanlı parçalama yöntemlerini tek bir platformda ve standart sıvı kromatografisi–kütle spektrometrisi iş akışlarının gerektirdiği zaman ölçeğinde uygulayabilen özel bir kütle spektrometresi üzerine inşa ettiler. Her yöntemin işletme koşullarını—örneğin lazer enerjisi veya elektron maruz kalma süresi—dikkatle ayarladılar, böylece karmaşık insan hücre örneklerinden her birinden mümkün olduğunca çok faydalı spektrum elde ettiler.
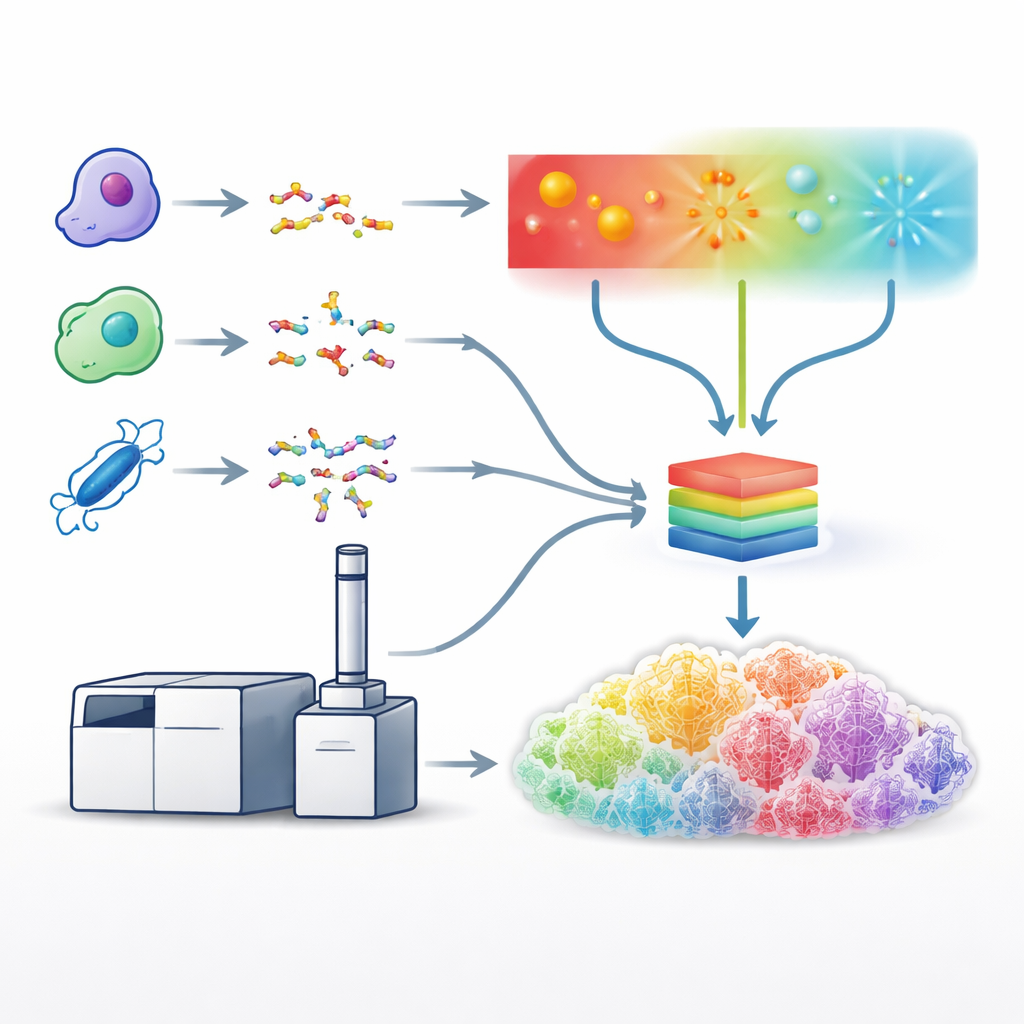
Birleşik Bir Öğrenme Modeli Kurmak
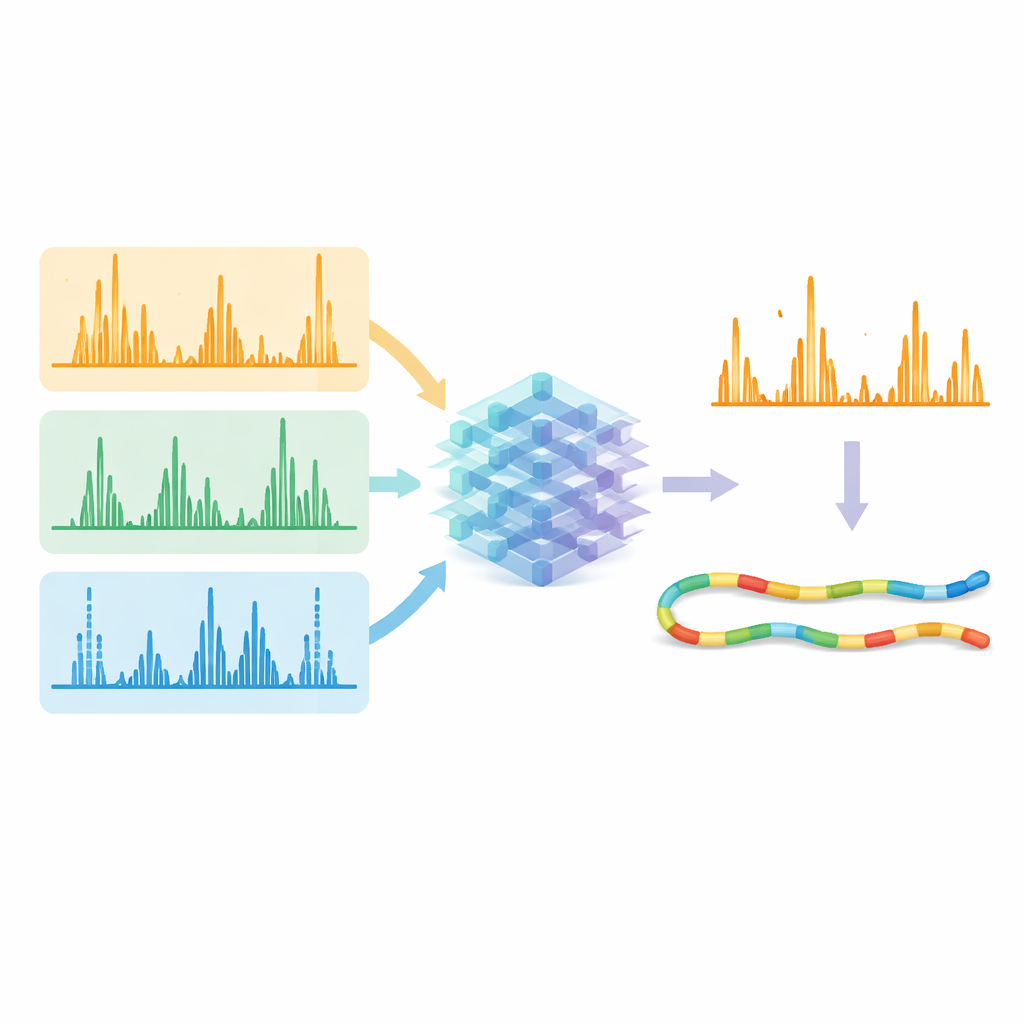
Bu optimize edilmiş yöntemler hazır olduğunda, ekip beş farklı protein kesici enzim kullanarak büyük veri setleri üretti; bu da çok çeşitli peptit dizileri sağladı. Ardından bu veri setlerini, Prosit adlı sistemin geliştirilmiş bir versiyonu olan tek bir derin öğrenme modelini, tüm parçalanma türleri için aynı anda kırıntı piklerinin ayrıntılı desenini ve yoğunluğunu tahmin etmesi için eğitmekte kullandılar. Her yöntemi ayrı ayrı ele almak yerine model, giriş olarak peptit dizisini, yükünü ve hangi parçalanma yönteminin kullanıldığını alıyor ve yüzlerce olası kırıntı türü için beklenen yoğunlukları veriyor. Tahmin edilen spektrumlar, yöntemler arasında deneysel verilerle çok yakın eşleşti; bu da modelin ışık-, elektron- ve çarpışma tabanlı kırılmaların karakteristik "parmak izlerini" etkin biçimde öğrendiğini gösterdi.
Yapay Zeka Sinyali Temizlesin
Gerçek sınav, bu tahminlerin ham veriden kaç peptidin güvenle tanımlanabildiğini iyileştirip iyileştiremeyeceğiydi. Araştırmacılar ölçülen spektrumları ve AI tarafından tahmin edilen desenleri mevcut arama ve yeniden puanlama araçlarına beslediler. Yazılımdan modelin güçlü ve mevcut olması gerektiğini söylediği kırıntılara odaklanmasını istediklerinde, doğru eşleşmeler yanlış olanlardan daha belirgin hale geldi. Farklı parçalanma yöntemleri ve enzimlerle toplanan verilerde, güvenle tanımlanan peptit–spektrum eşleşmelerinin sayısı tipik olarak %10’dan fazla arttı, bazı zorlu durumlarda %30’un üzerinde yükseldi. Önemli olarak, elektron ve ultraviyole ışık kullanan alternatif yöntemler artık standart çarpışma yöntemine benzer tanımlama verimliliğine ulaşırken daha geniş dizi kapsaması ve proteinler hakkında daha benzersiz bilgiler sağladı.
Gelişmiş Yöntemleri Günlük Kullanıma Taşımak
AI modeli ücretsiz olarak sunulduğu ve popüler kütle spektrometrisi yazılımlarına entegre edildiği için, yalnızca geleneksel hedefe yönelik ölçümler için değil aynı zamanda örneğin geniş bir örneği aynı anda tarayan veri-bağımsız edinim stratejileri için de kullanılabilir. İnsan, bitki ve bakteri hücre karışımları üzerinde yapılan testler modelin türler arasında iyi genelleştiğini gösterdi. Pratik açıdan, bu çalışma güçlü ama az kullanılan parçalanma yöntemlerini uzmanların elinden çıkaran önemli bir engeli ortadan kaldırıyor. Farklı protein parçalama yollarını tek bir öngörücü model altında birleştirerek, çalışma karmaşık protein manzaralarının rutin, yüksek kapsama sahip analizine giden bir yol sunuyor; böylece araştırmacıların nadir varyantları tespit etmelerini, modifikasyonları haritalamalarını ve nihayetinde proteinlerin sağlık ve hastalıkta nasıl davrandığına dair daha eksiksiz bir tablo elde etmelerini kolaylaştırıyor.
Atıf: Levin, N., Saylan, C.C., Lapin, J. et al. Integration of alternative fragmentation techniques into standard LC-MS workflows using a single deep learning model enhances proteome coverage. Nat Methods 23, 805–814 (2026). https://doi.org/10.1038/s41592-026-03042-9
Anahtar kelimeler: proteomik, kütle spektrometrisi, derin öğrenme, protein parçalanması, spektral öngörü