Clear Sky Science · pt
Integração de técnicas alternativas de fragmentação em fluxos de trabalho padrão de LC-MS usando um único modelo de aprendizado profundo aumenta a cobertura do proteoma
Vendo Mais da Maquinaria Proteica da Vida
Cada célula do seu corpo está repleta de milhares de proteínas diferentes, cada uma desempenhando uma função específica. A espectrometria de massas moderna já consegue ler muitas dessas proteínas ao quebrá‑las em fragmentos e pesar esses fragmentos, mas partes importantes ainda permanecem invisíveis—especialmente formas incomuns de proteínas e modificações químicas sutis que impulsionam a saúde e a doença. Este estudo descreve uma nova forma de combinar vários métodos avançados de fragmentação com um único modelo de inteligência artificial para que os cientistas possam observar muito mais do mundo das proteínas em um experimento rotineiro.
Como as Proteínas Costumam Ser Lidas
Na maioria dos laboratórios, as proteínas são primeiro cortadas em pedaços menores chamados peptídeos e então introduzidas em um instrumento que os separa e os pesa. Para determinar a sequência de cada peptídeo, o instrumento os fragmenta deliberadamente e registra o padrão dos fragmentos, como estilhaçar um vaso e inferir sua forma pelos cacos. Durante anos, um método baseado em colisões—no qual os peptídeos são quebrados ao colidirem com moléculas de gás—tem sido o cavalo de batalha porque é rápido, robusto e bem suportado por software. No entanto, essa abordagem padrão tem dificuldade em manter marcadores químicos delicados na proteína intactos e perde partes de formas proteicas complexas, deixando pontos cegos em nossa compreensão da biologia.
Novas Maneiras de Quebrar Proteínas
Pesquisadores desenvolveram outras formas de fragmentar peptídeos: usando luz ultravioleta ou feixes de elétrons, que cortam proteínas por caminhos diferentes e frequentemente preservam características frágeis. Essas abordagens podem gerar padrões de fragmentos mais ricos e informativos, mas são mais lentas, tecnicamente exigentes e têm pouco suporte por ferramentas de análise de dados. Para enfrentar isso, os autores se basearam em um espectrômetro de massas especializado que pode aplicar métodos de fragmentação por colisão, elétrons e fótons em uma única plataforma e na escala de tempo necessária para fluxos de trabalho padrão de cromatografia líquida–espectrometria de massas. Eles ajustaram cuidadosamente as condições operacionais de cada método—como a energia do laser ou o tempo de exposição aos elétrons—de modo que cada um produzisse o máximo possível de espectros úteis a partir de amostras complexas de células humanas.
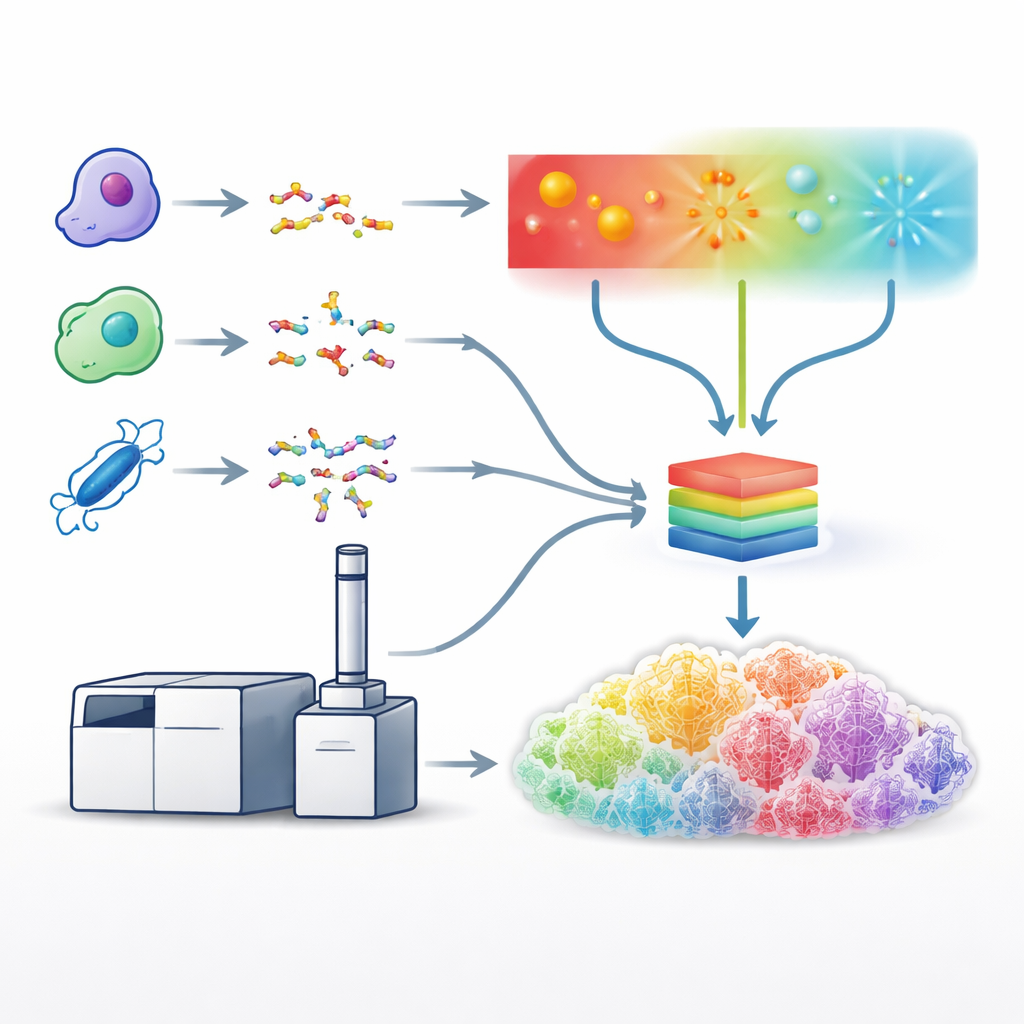
Construindo um Modelo de Aprendizado Unificado
Com esses métodos otimizados em funcionamento, a equipe gerou grandes conjuntos de dados usando cinco enzimas diferentes de clivagem de proteínas, o que produziu uma enorme diversidade de sequências peptídicas. Eles então usaram esses conjuntos para treinar um único modelo de aprendizado profundo, uma versão aprimorada de um sistema chamado Prosit, para prever o padrão detalhado e a intensidade dos picos de fragmentos para todos os tipos de fragmentação ao mesmo tempo. Em vez de tratar cada método separadamente, o modelo recebe como entrada a sequência do peptídeo, sua carga e qual método de fragmentação foi usado, e retorna as intensidades previstas para centenas de possíveis tipos de fragmento. Os espectros previstos corresponderam muito bem aos dados experimentais através dos métodos, mostrando que o modelo havia aprendido efetivamente as “impressões digitais” características produzidas pela fragmentação por luz, elétrons e colisões.
Permitindo que a IA Limpe o Sinal
O teste real foi verificar se essas predições poderiam melhorar quantos peptídeos são identificados com confiança a partir dos dados brutos. Os pesquisadores alimentaram tanto os espectros medidos quanto os padrões previstos pela IA em ferramentas existentes de busca e reavaliação. Quando pediram ao software para focar em fragmentos que o modelo dizia que deveriam ser fortes e presentes, as correspondências corretas sobressaíam mais claramente em relação às falsas. Nos dados coletados por diferentes métodos de fragmentação e enzimas, o número de correspondências peptídeo–espectro identificadas com confiança aumentou tipicamente mais de 10%, e em alguns casos desafiadores mais de 30%. Importante, métodos alternativos usando elétrons e luz ultravioleta agora alcançaram eficiência de identificação semelhante ao método padrão por colisão, enquanto proporcionavam cobertura de sequência mais ampla e informações mais únicas sobre as proteínas.
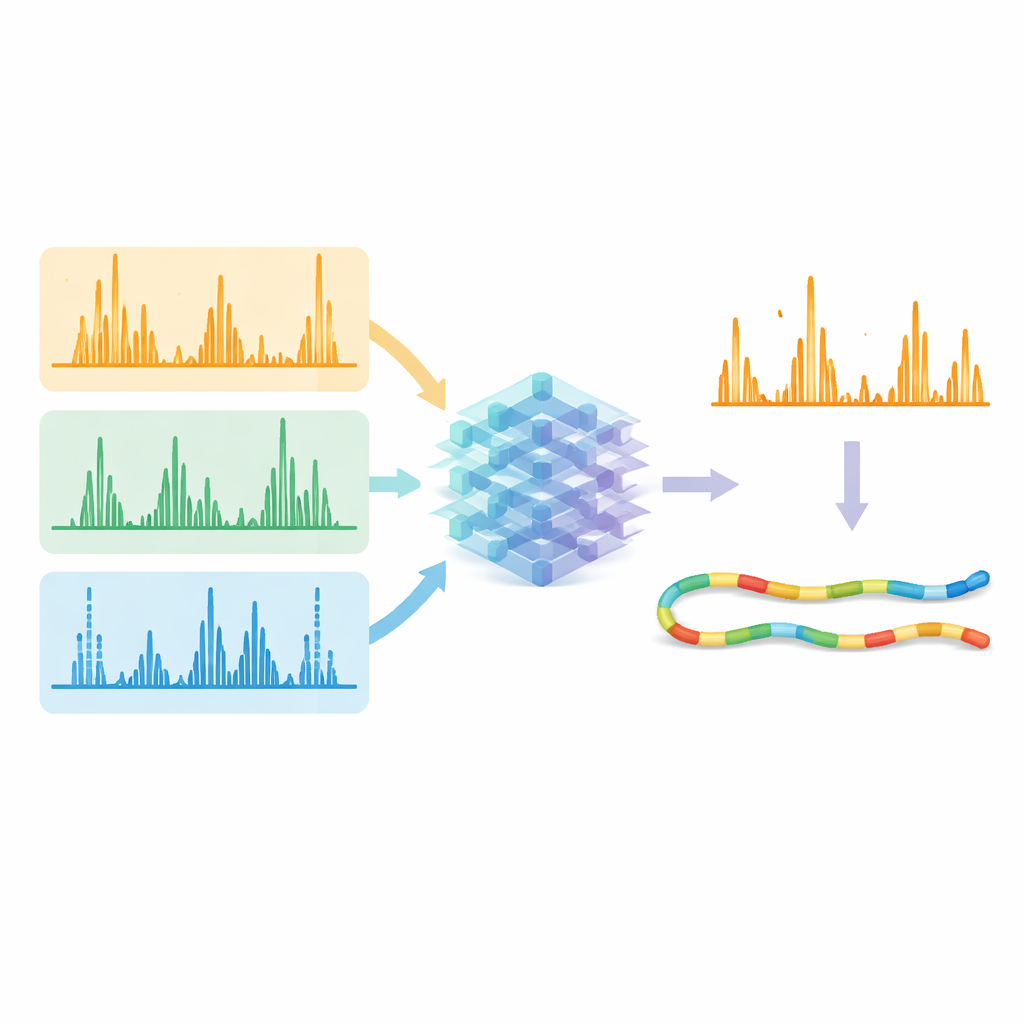
Levando Métodos Avançados ao Uso Cotidiano
Como o modelo de IA está disponível gratuitamente e integrado a softwares populares de espectrometria de massas, ele pode ser usado não apenas para medições tradicionais e direcionadas, mas também para estratégias mais novas de aquisição independente de dados que escaneiam amplas faixas da amostra de uma vez. Testes em misturas de células humanas, vegetais e bacterianas mostraram que o modelo generaliza bem entre espécies. Em termos práticos, este trabalho remove um obstáculo chave que mantinha métodos de fragmentação poderosos, mas pouco usados, confinados a especialistas. Ao unificar diferentes maneiras de fragmentar proteínas sob um modelo preditivo, o estudo fornece um caminho para análises rotineiras e de alta cobertura de paisagens proteicas complexas, facilitando a detecção de variantes raras, o mapeamento de modificações e, em última instância, a obtenção de uma imagem mais completa de como as proteínas se comportam na saúde e na doença.
Citação: Levin, N., Saylan, C.C., Lapin, J. et al. Integration of alternative fragmentation techniques into standard LC-MS workflows using a single deep learning model enhances proteome coverage. Nat Methods 23, 805–814 (2026). https://doi.org/10.1038/s41592-026-03042-9
Palavras-chave: proteômica, espectrometria de massas, aprendizado profundo, fragmentação de proteínas, predição espectral