Clear Sky Science · de
Integration alternativer Fragmentierungstechniken in Standard-LC-MS-Workflows mit einem einzigen Deep-Learning-Modell verbessert die Proteomabdeckung
Mehr von den Proteinmaschinen des Lebens sehen
Jede Zelle Ihres Körpers ist vollgepackt mit tausenden verschiedener Proteine, die jeweils eine spezifische Aufgabe erfüllen. Die moderne Massenspektrometrie kann bereits viele dieser Proteine lesen, indem sie sie in Teile zerlegt und die Fragmente wiegt, doch wichtige Bereiche bleiben nach wie vor unsichtbar – besonders ungewöhnliche Proteinformen und feine chemische Modifikationen, die Gesundheit und Krankheit antreiben. Diese Studie beschreibt einen neuen Weg, mehrere fortgeschrittene Fragmentierungsmethoden mit einem einzigen künstlichen Intelligenzmodell zu kombinieren, sodass Wissenschaftler in einem routinemäßigen Experiment deutlich mehr von der Proteinwelt sehen können.
Wie Proteine normalerweise gelesen werden
In den meisten Laboren werden Proteine zunächst in kleinere Stücke, sogenannte Peptide, zerteilt und dann in ein Instrument eingespeist, das sie trennt und wiegt. Um die Sequenz jedes Peptids zu bestimmen, lässt das Gerät diese Stücke gezielt zerbrechen und zeichnet das Fragmentmuster auf – ähnlich wie beim Zerbrechen einer Vase und dem Rückschluss auf ihre Form aus den Scherben. Jahrelang war eine kollisionsbasierte Methode – bei der Peptide durch Zusammenstöße mit Gasmolekülen gebrochen werden – das Arbeitspferd, weil sie schnell, robust und gut durch Software unterstützt ist. Allerdings hat dieser Standardansatz Schwierigkeiten, empfindliche chemische Anhänge am Protein intakt zu lassen, und übersieht Teile komplexer Proteinformen, wodurch in unserem Verständnis der Biologie blinde Flecken entstehen.
Neue Wege, Proteine auseinanderzubrechen
Forscher haben andere Möglichkeiten entwickelt, Peptide zu spalten: mittels ultraviolettem Licht oder Elektronenstrahlen, die Proteine entlang anderer Pfade schneiden und oft fragile Merkmale erhalten. Diese Ansätze können reichhaltigere und informativerere Fragmentmuster erzeugen, sind jedoch langsamer, technisch anspruchsvoller und werden von Datenanalysetools schlecht unterstützt. Um dies zu beheben, bauten die Autorinnen und Autoren auf einem spezialisierten Massenspektrometer auf, das Kollisions-, Elektronen- und Photonen-basierte Fragmentierungsmethoden auf einer Plattform und in dem für Standard-LC–MS-Workflows nötigen Zeitrahmen anwenden kann. Sie stimmten die Betriebsbedingungen für jede Methode sorgfältig ab – etwa Laserenergie oder Elektronenexpositionszeit –, sodass jede Methode aus komplexen humanen Zellproben möglichst viele nützliche Spektren erzeugte.
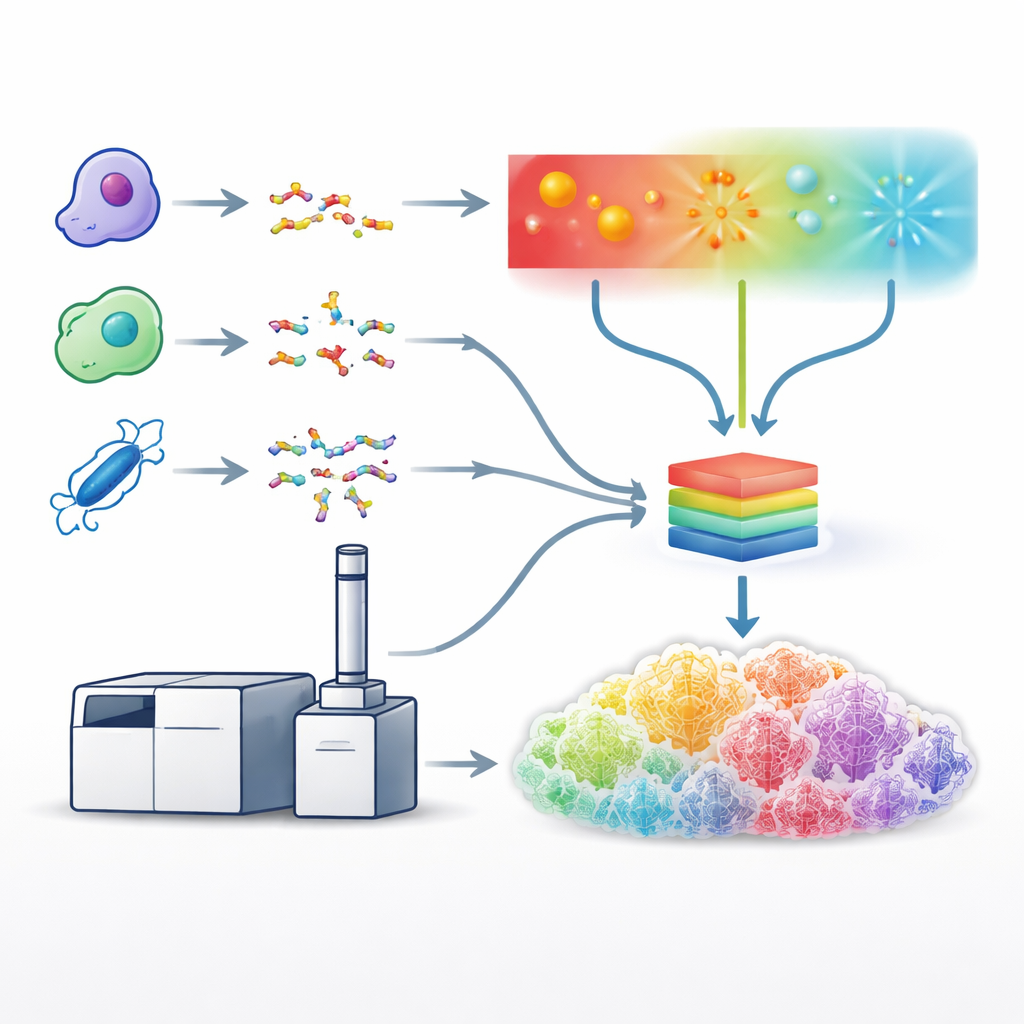
Aufbau eines einheitlichen Lernmodells
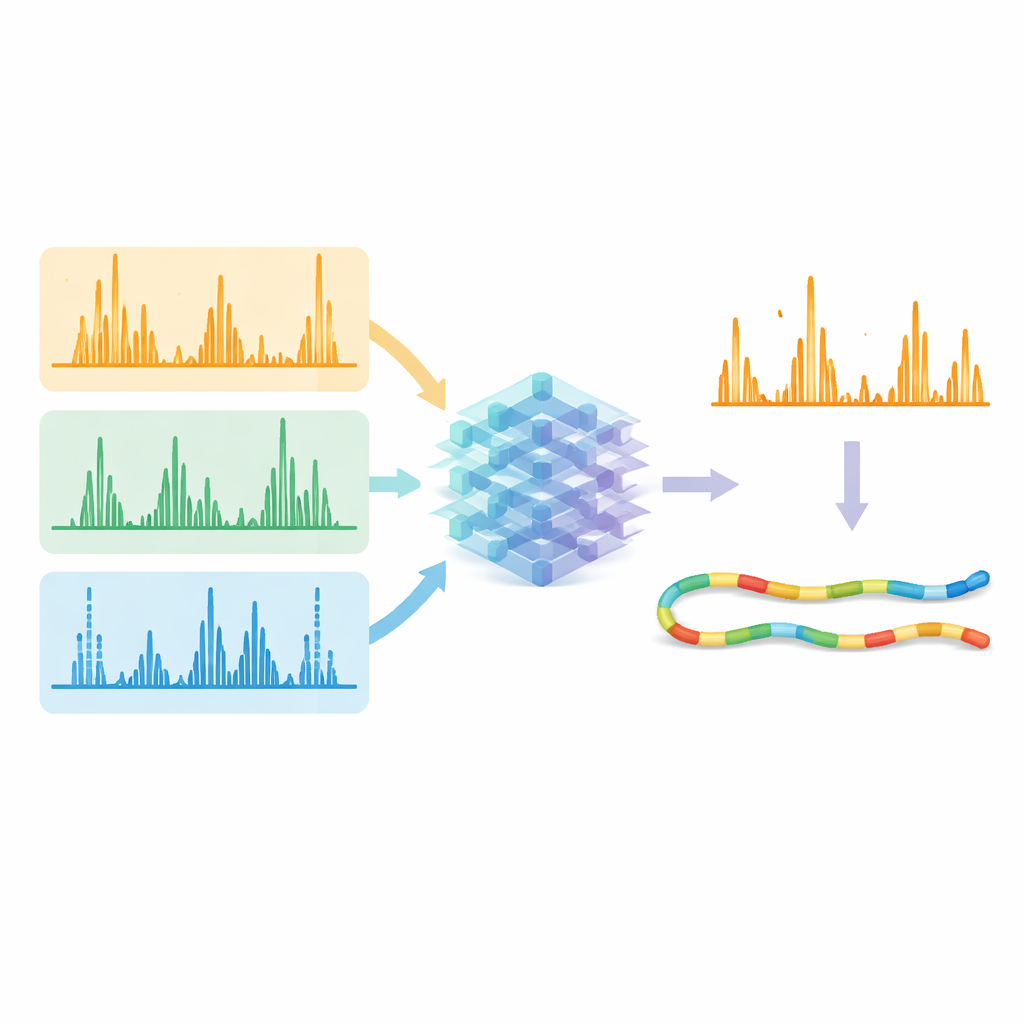
Mit diesen optimierten Methoden erzeugte das Team umfangreiche Datensätze unter Verwendung von fünf verschiedenen proteinspaltenden Enzymen, was eine große Vielfalt an Peptidsequenzen ergab. Diese Datensätze nutzten sie, um ein einziges Deep-Learning-Modell zu trainieren – eine weiterentwickelte Version eines Systems namens Prosit –, das die detaillierten Muster und Intensitäten von Fragmentpeaks für alle Fragmentierungstypen gleichzeitig vorhersagen kann. Anstatt jede Methode getrennt zu behandeln, nimmt das Modell als Eingabe die Peptidsequenz, ihre Ladung und die eingesetzte Fragmentierungsmethode und liefert die erwarteten Intensitäten für Hunderte möglicher Fragmenttypen. Die vorhergesagten Spektren stimmten experimentellen Daten über die Methoden hinweg sehr genau, was zeigte, dass das Modell die charakteristischen „Fingerabdrücke“ der licht-, elektron- und kollisionsbasierten Fragmentierung effektiv erlernt hatte.
Die KI das Signal bereinigen lassen
Der eigentliche Test war, ob diese Vorhersagen die Anzahl der Peptide erhöhen können, die aus Rohdaten zuverlässig identifiziert werden. Die Forschenden speisten sowohl die gemessenen Spektren als auch die KI-vorhergesagten Muster in vorhandene Such- und Rescoring-Tools. Wenn die Software sich auf Fragmente konzentrieren sollte, die das Modell als stark und vorhanden vorhersagte, traten korrekte Treffer klarer gegenüber falschen hervor. Über Daten, die mit verschiedenen Fragmentierungsmethoden und Enzymen gewonnen wurden, stieg die Zahl der zuverlässig identifizierten Peptid–Spektrum-Treffer typischerweise um mehr als 10 %, in einigen schwierigen Fällen sogar um über 30 %. Wichtig ist, dass alternative Methoden mit Elektronen und ultraviolettem Licht nun eine Erkennungsleistung erreichten, die mit der Standard-Kollisionsmethode vergleichbar ist, dabei jedoch eine breitere Sequenzabdeckung und mehr einzigartige Informationen über Proteine liefert.
Fortgeschrittene Methoden in den Alltag bringen
Da das KI-Modell frei verfügbar und in populäre Massenspektrometrie-Software integriert ist, kann es nicht nur für traditionelle, zielgerichtete Messungen, sondern auch für neuere datenunabhängige Erfassungsstrategien (data-independent acquisition) verwendet werden, die weite Bereiche der Probe gleichzeitig abtasten. Tests an Mischungen aus menschlichen, pflanzlichen und bakteriellen Zellen zeigten, dass das Modell gut über Spezies hinweg generalisiert. Praktisch gesehen beseitigt diese Arbeit eine wesentliche Hürde, die leistungsfähige, aber wenig genutzte Fragmentierungsmethoden bislang Spezialisten vorbehalten hatte. Indem verschiedene Weise, Proteine zu fragmentieren, unter einem vorhersagenden Modell vereinheitlicht werden, eröffnet die Studie einen Weg zu routinemäßigen, hochabdeckenden Analysen komplexer Proteinlandschaften, wodurch es Forschenden leichter fällt, seltene Varianten zu entdecken, Modifikationen zu kartieren und letztlich ein vollständigeres Bild des Proteinverhaltens in Gesundheit und Krankheit zu gewinnen.
Zitation: Levin, N., Saylan, C.C., Lapin, J. et al. Integration of alternative fragmentation techniques into standard LC-MS workflows using a single deep learning model enhances proteome coverage. Nat Methods 23, 805–814 (2026). https://doi.org/10.1038/s41592-026-03042-9
Schlüsselwörter: Proteomik, Massenspektrometrie, Deep Learning, Proteinfragmentierung, Spektralvorhersage