Clear Sky Science · tr
Bir nükleotid kodu Lis1’in dynein otoinhibitasyonunu gidermesini yönetiyor
Hücreler küçük yük taşıyıcılarını nasıl kontrol altında tutar
Her hücrenin içinde, minyatür makineler ince raylar boyunca yük taşır; dokuları şekillendirmeye, kromozomları bölmeye ve çekirdeği konumlandırmaya yardımcı olurlar. Bu taşıyıcıların en önemlilerinden biri dynein adlı bir motor proteindir. Dynein hem çok güçlü hem de geniş ölçüde kullanıldığından, hücreler bunu gerektiğinde açılacak şekilde güvenli biçimde kapalı tutmak zorundadır. Bu çalışma, başka bir protein olan Lis1’in (mayada Pac1 olarak adlandırılır) dyneindeki ince bir “nükleotid kodunu” nasıl okuduğunu ve motoru katlanmış, kilitli bir durumdan açık, yük taşıyabilecek aktif bir forma nasıl çevirdiğini ortaya koyuyor.
Emniyet kilidi olan moleküler bir motor
Dynein, veziküller, RNA ve hatta tüm çekirdekleri taşıyarak hücrenin iç rayları olan mikrotübüller boyunca yürüyen büyük, çok parçalı bir motordur. Yanlış teslimatı önlemek için dynein normalde iki motor başını birbirine katlayıp mikrotübüllerle neredeyse etkileşime girmeyen kendi kendini kilitleyen, “phi” parçacığı olarak anılan otoinhibitli bir konformasyonda oturur. Uzun mesafe taşımacılığı için dynein önce açılmalı, sonra dynactin adlı başka bir kompleks ve bir yük adaptörü ile birleşmelidir. Önceki çalışmalar Lis1’in dyneini kilidinden çıkarmaya yardım ettiğine işaret etmişti, ancak ayrıntılar belirsizdi; kısmen bunun nedeni dynein motorunun her birine farklı ATP veya ADP formları bağlayabilen birkaç nükleotid bağlayıcı cebe sahip olmasıydı. Yazarlar, bu ceplerin ve Lis1 bağlanmasının dyneinin şeklini nasıl birlikte kontrol ettiğini çözmeyi hedeflediler.
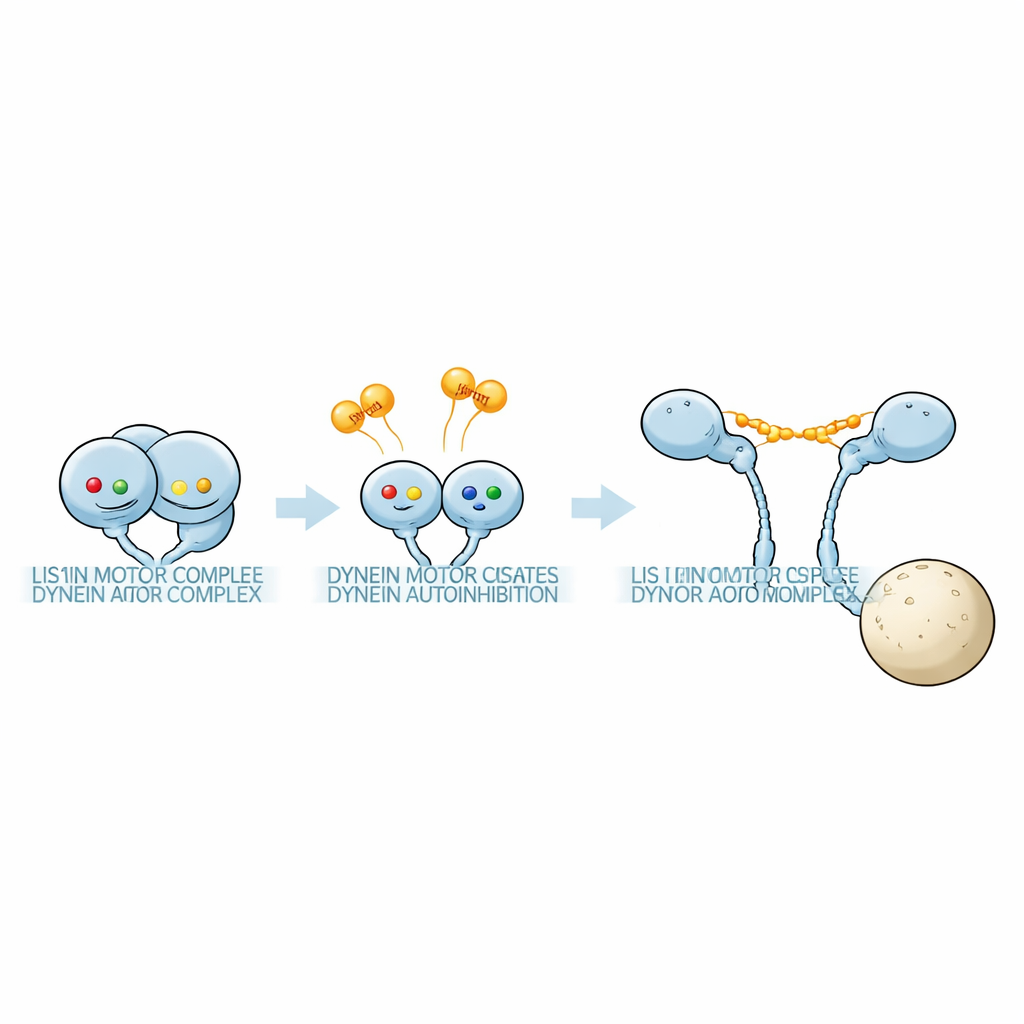
Gizli bir nükleotid “kodunu” keşfetmek
Grup, dynein motor fragmentleri ve Pac1 içeren çözeltilerde çok sayıda nükleotid koşulu altında protein komplekslerini tartmak için hassas kütle fotometrisi kullandı. Dynein motor halkası üç aktif cebe sahiptir: AAA1, AAA3 ve AAA4. Her cebi tanımlı bir duruma kilitleyecek şekilde nükleotid bağlanmasını engelleyen veya ATP hidrolizini bloke eden hassas mutasyonlar yaparak araştırmacılar tek tek yerleri sabit hâllere kilitleyebildiler. Bu üç sitedeki nükleotid kombinasyonunun Pac1’in ne kadar sıkı bağlanacağını ve çok önemli olarak her bir dyneine kaç Pac1 ünitesinin tutunacağını güçlü biçimde etkilediğini buldular. Bazı nükleotid kombinasyonlarında bir Pac1 dimeri iki ayrı dynein motorunu köprülerken; bazılarında sadece bir motora temas etti; başka durumlarda ise neredeyse hiç bağlanmadı. Bu desenler, ayrı nükleotid “kodlarının” 1:1 dynein:Pac1 kompleksi ile fazladan Pac1 bağlı 1:2 kompleksi arasında seçim yaptığını ortaya koydu.
Lis1 motoru nasıl yeniden şekillendiriyor
Daha sonra elektron mikroskopisi bağlanma modunu şekille ilişkilendirdi. Pac1, tam uzunluk dynein ile 1:1 kompleks oluşturduğunda, motorlar neredeyse tamamen phi konformasyonundan ayrılarak iki başın sabit bir mesafede ayrı olduğu açık bir forma geçti. Negatif boyama görüntüleri Pac1 dimerlerinin iki motor domenini köprülediğini gösterdi; bu, izole motor–Pac1 çiftlerinde görülen aralığa karşılık geliyordu. Buna karşılık, koşullar 1:2 kompleksi desteklediğinde, dynein phi-benzeri bir düzenlemede kaldı: daha esnek ve hafifçe bozulmuş, ama tam olarak açık değil; hâlâ kompakt. Böylece önemli olan sadece Pac1’in varlığı değil, kaç Pac1 molekülünün bağlandığı ve nereye bağlandığıdır.
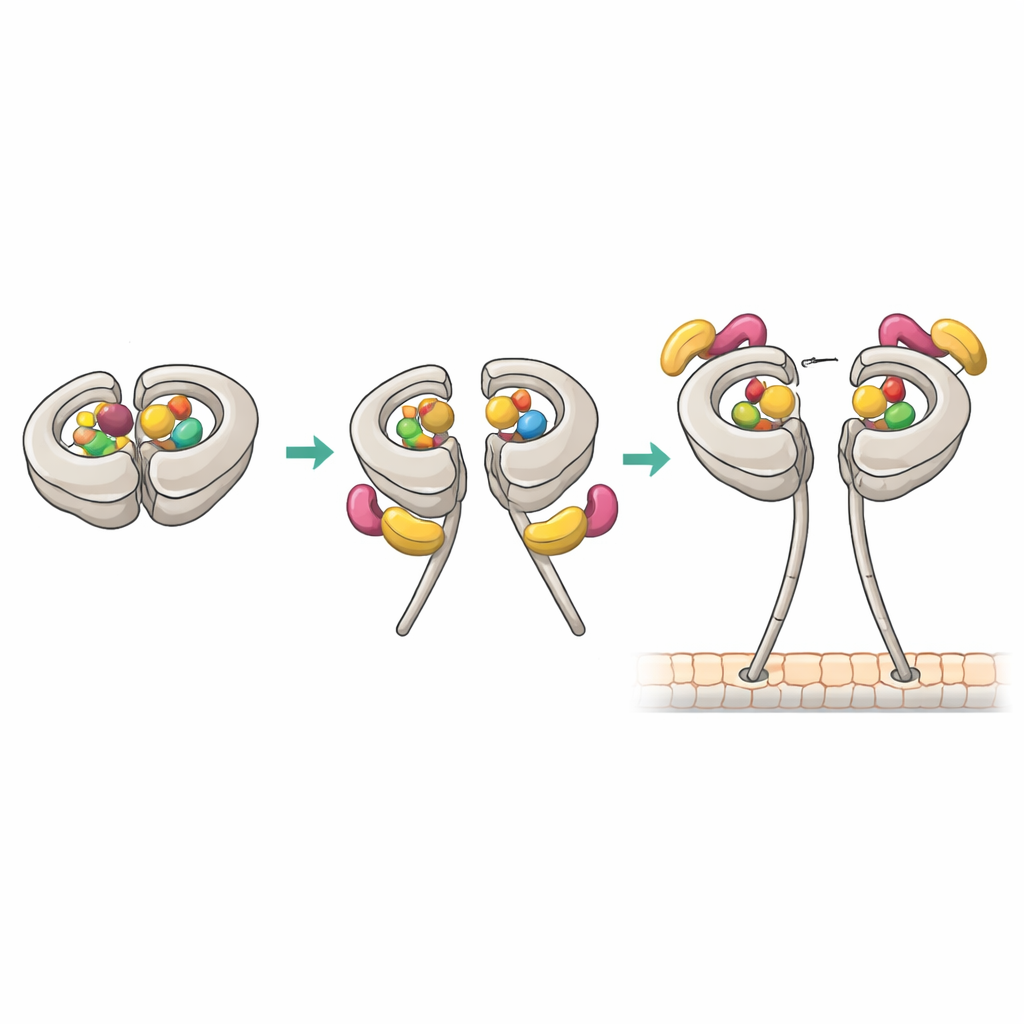
Klamayı açan yeni temas noktaları
Kryo-elektron mikroskopisi yakın-atomik çözünürlükte, üretken 1:1 kompleksin nasıl kurulduğunu ortaya çıkardı. Bu durumda, dynein’in birincil bölgesi AAA1 ve düzenleyici bölge AAA4 her ikisi de ADP tutarken, AAA3 boştu. Bu nükleotid deseni Pac1 için yüksek afiniteyle ilişkiliydi. Pac1’in bir WD40 “bıçağı” motor halkasında daha önce bilinen bir yere otururken, yapı aynı zamanda dynein’in esnek bağlayıcı (linker) bölgesinde ikinci bir teması da ortaya çıkardı. Bu çift kavrama noktaları bağlayıcının değiştirilmiş bir “vuruş sonrası” konumunu stabilize eder ve Pac1’i hafifçe sap yönüne doğru iter; bu da başka bir Pac1 WD40’ının normalde konumlanacağı halka bitişiğindeki ikinci bağlanma yerini engeller. Bağlayıcı temasını mutasyona uğratmak, Pac1’in dyneini açma yeteneğini zayıflattı, bağlanma stekiyometrisini değiştirdi ve temel motor aktivitesi korunmasına rağmen mayada dynein kaynaklı iğ hareketlerini bozdu.
Biyokimyasal anahtardan hücresel harekete
Bu sonuçları birleştirerek yazarlar aşamalı bir aktivasyon yolu öneriyorlar. Dynein tipik olarak birkaç cepte ADP ile phi durumunda oturur; bu durum Pac1’in motoru açmayan bir şekilde bağlanmasına izin verir. Nadiren, bir düzenleyici cep (AAA3) ADP’yi bırakır ve bağlayıcı belirli bir pozisyona sallanır. O anda Pac1, her bir motor başının halkasına ve bağlayıcısına aynı anda kenetlenerek baş çiftini köprüleyen tek bir Pac1 dimeri oluşturabilir ve mikrotübüller için yüksek afiniteli açık bir konformasyonu stabilize edebilir. Bu açık durum sonra dynactin ve yük adaptörlerine bağlanmaya hazırlanarak tam hareketli bir taşıma makinesi oluşturur. Dynein bir mikrotübüle bağlanıp yürümeye başladığında, Pac1’in kavraması zayıflar ve ayrılır; denetimi diğer düzenleyicilere devreder.
Sağlık ve hastalık açısından önemi
Uzman olmayan bir okuyucu için ana mesaj, dyneinin sadece açık ya da kapalı olmadığı; bunun yerine nükleotid durumlarının ve Lis1 bağlanmasının bir kombinasyonuyla ayarlandığı ve bunun bir emniyet mantığı oluşturduğu. Yalnızca doğru nükleotid kodu ortaya çıktığında Lis1 moleküler bir kama gibi davranarak motoru açar ve onun dynactin ile uzun mesafe taşıma ekibine katılmasını sağlar. İnsan Lis1’in beyin gelişimi için hayati olması ve bozukluğunun lissensefali ve diğer nörolojik bozukluklara yol açması nedeniyle, bu kodu atomik ayrıntıda anlamak Lis1 veya dyneindeki ince değişikliklerin hücresel lojistiği ve nihayetinde organizma gelişimini nasıl bozabileceğine dair bir yol haritası sunar.
Atıf: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Anahtar kelimeler: dynein motoru, Lis1 Pac1, moleküler taşınım, protein otoinhibisyonu, kryo elektron mikroskopisi