Clear Sky Science · he
קוד נוקלאוטידי שולט ביכולת של Lis1 לשחרר את האוטואינהיביציה של דינאין
איך תאים שומרים על הנהגים הקטנים שלהם מבוקרים
בתוך כל תא, מכונות זעירות גוררות מטענים לאורך מסילות דקיקות, ותורמות לעיצוב רקמות, לחלוקת כרומוזומים ולהצבת הגרעין. אחד ממוביליהן החשובים הוא חלבון מנוע בשם דינאין. מאחר שדינאין חזק ונמצא בשימוש נרחב, התאים חייבים לשמור אותו כבוי עד ובמתי שהוא נדרש. העבודה הזו חושפת כיצד חלבון נוסף, Lis1 (בשמטרה שמו הוא Pac1 בשמרים), קורא «קוד נוקלאוטידי» עדין בדינאין כדי להפוך אותו ממצב מקופל ונעול לצורה פתוחה ופעילה היכולת להזיז מטען.
מנוע מולקולרי עם מנגנון בטיחות
דינאין הוא מנוע גדול רב-חלקי ההולך על מיקרוטובולים, המסילות הפנימיות של התא, ונושא וזיקולות, RNA ואפילו גרעינים שלמים. כדי למנוע הובלה שגויה, דינאין בדרך כלל נמצא בקונפורמציה אוטואינהיביטורית עצמית המכונה חלקיק «פיי», שבה שתי ראשי המנוע מתקפלים יחד ובאופן דל מתקיימים אינטראקציות עם המיקרוטובולים. לצורך מסלולים למרחקים ארוכים, דינאין חייב קודם להתפרש ואז להתחבר למורכב אחר, הדינתקטין, בנוסף למתווך מטען. עבודות קודמות רמזו כי Lis1 מסייע לשחרר את דינאין, אך הפרטים היו עמומים, בין היתר משום שמנוע דינאין מכיל כמה אתרי קשירה לנוקלאוטידים שיכולים להכיל צורות שונות של ATP או ADP. המחברים יצאו לפענח כיצד אתרים אלה, וקשירת Lis1, פועלים ביחד כדי לשלוט במבנה הדינאין.
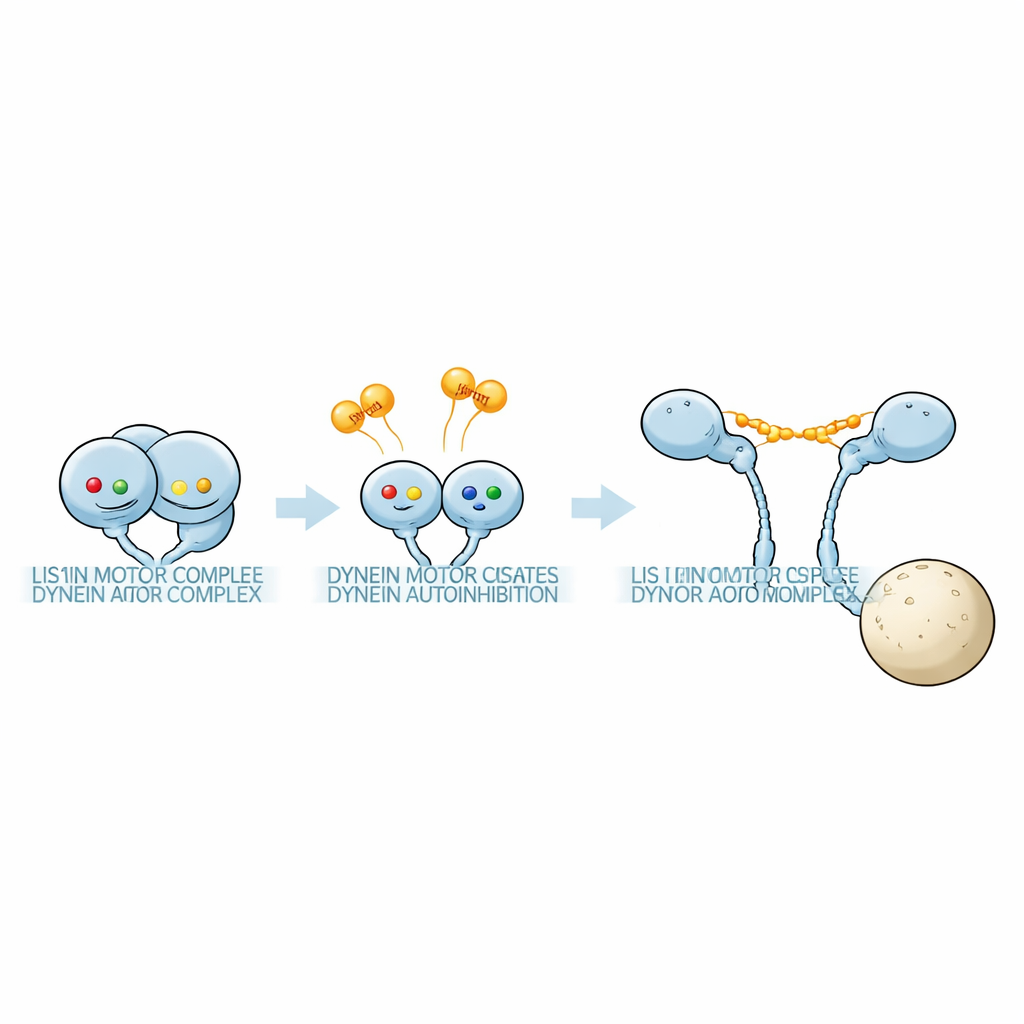
גילוי «קוד» נוקלאוטידי חבוי
הקבוצה השתמשה בפוטומטריה מסת-רגישה לשקול קומפלקסים חלבוניים בתמיסות שכללו מקטעי מנוע דינאין ו-Pac1 בתנאי נוקלאוטידים שונים. טבעת המנוע של דינאין נושאת שלושה אתרים פעילים, AAA1, AAA3 ו-AAA4. על ידי הכנסת מוטציות מדויקות שמנעות קשירת נוקלאוטיד או חוסמות הידרוליזת ATP בכל אתר, החוקרים יכלו לנעול כל אתר במצב מוגדר. הם מצאו ששילוב הנוקלאוטידים בשלושת האתרים השפיע בחוזקה על מידת הקשירה של Pac1 וחשוב מכך — על מספר יחידות Pac1 שכרוכות על כל דינאין. בחלק משילובי הנוקלאוטידים דימר של Pac1 גשר בין שני מנועי דינאין נפרדים; באחרים הוא נגע רק במנוע אחד; ובחלק נוסף כמעט שלא נקשר בכלל. דפוסים אלה חשפו כי «קודי» נוקלאוטידים מובחנים בוחרים בין קומפלקס 1:1 של דינאין:Pac1 לקומפלקס 1:2 עם Pac1 נוסף קשור.
איך Lis1 מעצבת את המנוע
מיקרוסקופיה אלקטרונית קישרה אחר כך את אופן הקשירה לצורה. כאשר Pac1 יצר קומפלקס 1:1 עם דינאין באורך מלא, המנועים השתנו כמעט לחלוטין מהקונפורמציה פיי לצורה פתוחה, כשהשניים הראשיים מופרדים במרחק קבוע. תמונות בצביעה שלילית הראו דימרים של Pac1 מגשרים בין שני תחומי המנוע, בהתאמה לריווח שנצפה בזוגות מנוע–Pac1 מבודדים. לעומת זאת, כאשר התנאים הטו לקומפלקס 1:2, דינאין נשאר במבנה הדומה לפיי: גמיש יותר ומעוות מעט, אך עדיין קומפקטי ולא פתוח לגמרי. לפיכך, לא מספיק נוכחות Pac1 עצמה — מה שקובע הוא בדיוק כמה מולקולות Pac1 נקשרות ולאן.
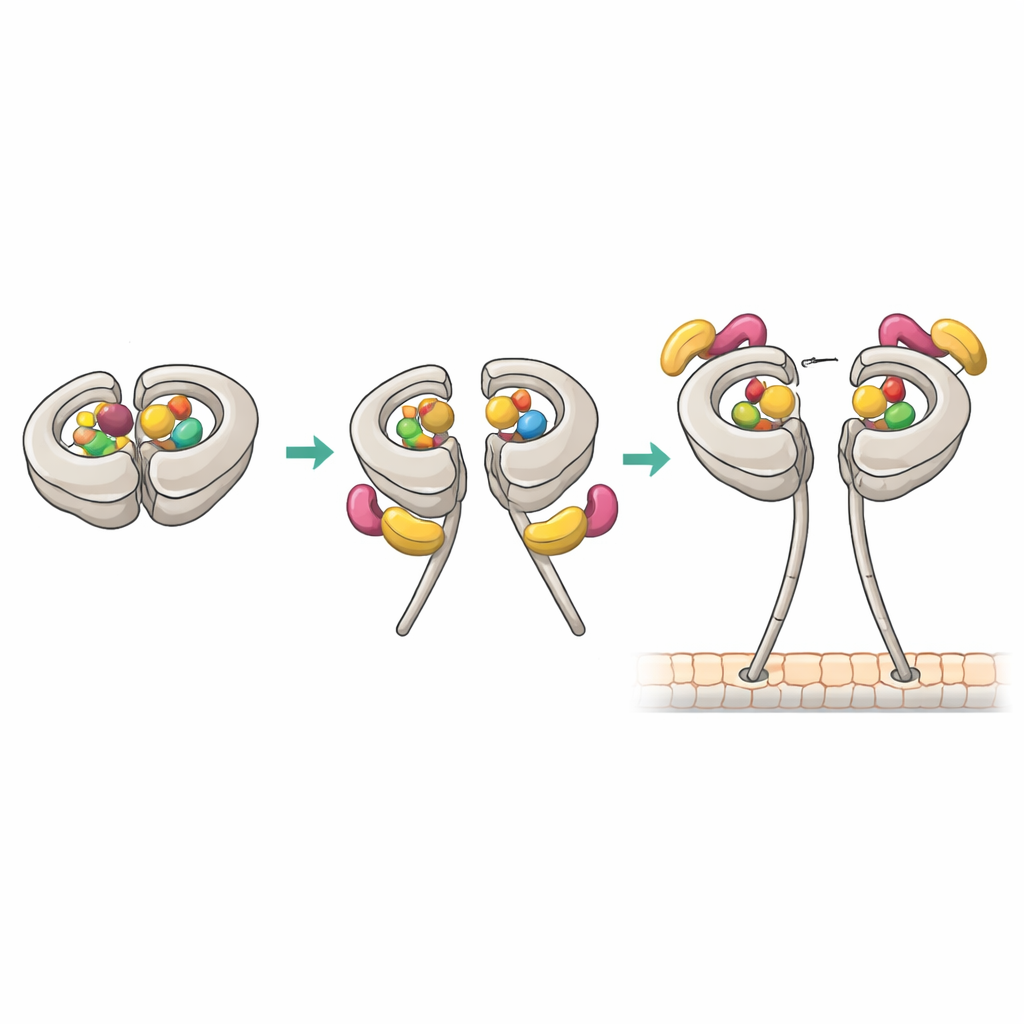
נקודות מגע חדשות ששחררות את הקליפ
קריו-מיקרוסקופיה אלקטרונית ברזולוציה כמעט אטומית חשפה כיצד קומפלקס 1:1 פרודוקטיבי נבנה. במצב זה, האתר הראשי של דינאין AAA1 ואתר רגולטורי AAA4 מחזיקים שניהם ADP, בעוד AAA3 ריק. תבנית נוקלאוטידים זו מתואמת עם זיקה גבוהה ל-Pac1. אחת הלהבים של WD40 ב-Pac1 יושבת באתר של טבעת המנוע שהיה ידוע קודם, אך המבנה חשף גם נקודת מגע שנייה באזור הקישור הגמיש של הלינקר של דינאין. שתי נקודות האחיזה הללו מייצבות מיקום לינקר משונה בדמות «פוסט-סטroke» ודוחפות את Pac1 מעט לכיוון הסטוק, מה שחוסם במקביל קשירה באתר סמוך לטבעת שברוב המקרים היה מארח WD40 של Pac1 נוסף. מוטציות בנקודת המגע בלינקר החלישו את יכולת Pac1 לפתוח את דינאין, שינו את סטויכיומטריית הקשירה ופגעו בתנועות הזיגוג המונעות על ידי דינאין בתאים של שמרים, אף על פי שהפעילות המנועית הבסיסית נותרה שלמה.
ממתג ביוכימי לתנועה תאית
בהרכבת התוצאות הללו יחד, המחברים מציעים מסלול הפעלה בשלבים. דינאין בדרך כלל יושב בפיי עם ADP בכמה אתרים, המצב שמאפשר ל-Pac1 להיקשר בצורה שאינה פותחת את המנוע. מעת לעת אחד האתרים הרגולטוריים (AAA3) משחרר ADP, מה שמאפשר ללינקר לנוע למיקום מסוים. ברגע זה, Pac1 יכול לאחוז הן בטבעת והן בלינקר של כל ראש מנוע, ליצור דימר יחיד של Pac1 שמגשר בין זוג הראשיים ולייצב קונפורמציה פתוחה עם זיקה גבוהה למיקרוטובולים. מצב פתוח זה יוצג אז למעגן על דיינקטין ולמתווכי מטען כדי ליצור מכונת הובלה ניידת באופן מלא. כאשר דינאין מתיישב על מיקרוטובול ומתחיל ללכת, אחיזת Pac1 נחלשת והוא מתנתק, ומעביר את השליטה לווסתים אחרים.
מדוע זה חשוב לבריאות ומחלה
ללא רקע מקצועי, המסר המרכזי הוא שדינאין אינו פשוט מתחלף מצב דלוק/כבה; הוא מכוּון על ידי צירוף של מצבי נוקלאוטידים וקשירת Lis1 היוצרים יחד לוגיקת בטיחות. רק כאשר מופיע הקוד הנוקלאוטידי הנכון Lis1 פועל כמדף מולקולרי, פותח את המנוע ומאפשר לו להצטרף לצוות ההובלה למרחקים ארוכים עם דיינקטין. מכיוון ש-Lis1 האנושי חיוני להתפתחות המוח וכשגיאה בו גורמת לליסנצפליה ולמחלות נוירולוגיות נוספות, הבנת הקוד הזה ברזולוציה אטומית מציעה מפת דרכים להבהיר כיצד שינויים עדינים ב-Lis1 או בדינאין יכולים לסטות את הלוגיסטיקה התאית ולפגוע בסופו של דבר בהתפתחות האורגניזם.
ציטוט: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
מילות מפתח: מנוע דינאין, Lis1 Pac1, הובלה מולקולרית, אוטואינהיביציה של חלבון, קריו-מיקרוסקופיה אלקטרונית