Clear Sky Science · de
Ein Nukleotidcode steuert Lis1s Fähigkeit, die Dynein-Autoinhibition aufzuheben
Wie Zellen ihre winzigen Frachttransporter in Schach halten
Im Inneren jeder Zelle transportieren winzige Maschinen Fracht entlang schlanker Schienen, formen Gewebe, teilen Chromosomen und positionieren den Zellkern. Einer der wichtigsten dieser Transporter ist das Motorprotein Dynein. Weil Dynein so kraftvoll und weit verbreitet ist, müssen Zellen es sicher abgeschaltet halten, solange es nicht gebraucht wird. Diese Studie zeigt, wie ein anderes Protein, Lis1 (in Hefen Pac1 genannt), einen subtilen „Nukleotidcode“ in Dynein liest, um es aus einem gefalteten, verriegelten Zustand in eine offene, aktive Form zu überführen, die Fracht bewegen kann.
Ein molekularer Motor mit einer Sicherheitssperre
Dynein ist ein großer, mehrteiliger Motor, der entlang von Mikrotubuli, den inneren Schienen der Zelle, wandert und Vesikel, RNA und sogar ganze Zellkerne befördert. Um Fehlleitung zu vermeiden, liegt Dynein normalerweise in einer selbstgeklemten, autoinhibierten Konformation vor, der sogenannten „Phi“-Partikel, in der sich seine beiden Motorhäupter zusammenfalten und kaum mit Mikrotubuli interagieren. Für Langstreckenläufe muss Dynein zuerst entfalten und sich dann mit einem weiteren Komplex, Dynactin, sowie einem Frachtadapter verbinden. Frühere Arbeiten deuteten an, dass Lis1 beim Entriegeln von Dynein hilft, doch die Details waren unklar, unter anderem weil der Motor mehrere Nukleotid-Bindetaschen enthält, die verschiedene Formen von ATP oder ADP halten können. Die Autorinnen und Autoren machten sich daran zu entschlüsseln, wie diese Taschen und die Bindung von Lis1 zusammenwirken, um Dyneins Form zu steuern.
Entdeckung eines verborgenen Nukleotid-„Codes“
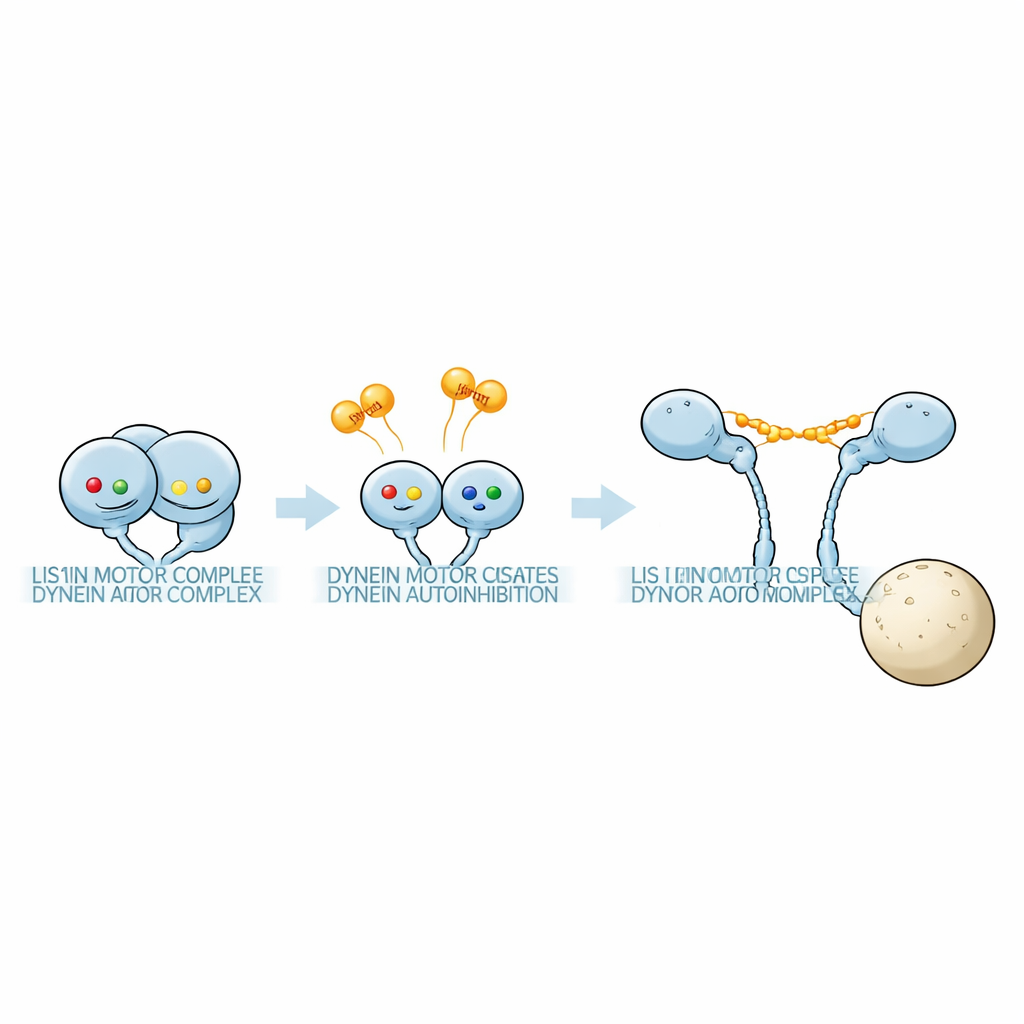
Das Team verwendete empfindliche Massenspektrometrie (Mass Photometry), um Proteinkomplexe in Lösungen mit Dynein-Motorfragmenten und Pac1 unter verschiedenen Nukleotidbedingungen zu wiegen. Der Motorring von Dynein trägt drei aktive Taschen, AAA1, AAA3 und AAA4. Durch gezielte Mutationen, die entweder die Nukleotidbindung verhindern oder die ATP-Hydrolyse in einer einzelnen Tasche blockieren, konnten die Forscher einzelne Stellen in definierte Zustände sperren. Sie fanden heraus, dass die Kombination der Nukleotide an diesen drei Stellen stark beeinflusste, wie fest Pac1 bindet und — entscheidend — wie viele Pac1-Moleküle an jedes Dynein gebunden werden. Unter manchen Nukleotidkombinationen überbrückte ein Pac1-Dimer zwei getrennte Dynein-Motoren; in anderen Kontakt nahm es nur einen Motor; und wieder in anderen Fällen band es kaum. Diese Muster zeigten, dass unterschiedliche Nukleotid-„Codes“ zwischen einem 1:1-Dynein:Pac1-Komplex und einem 1:2-Komplex mit zusätzlichem Pac1 unterscheiden.
Wie Lis1 den Motor umgestaltet
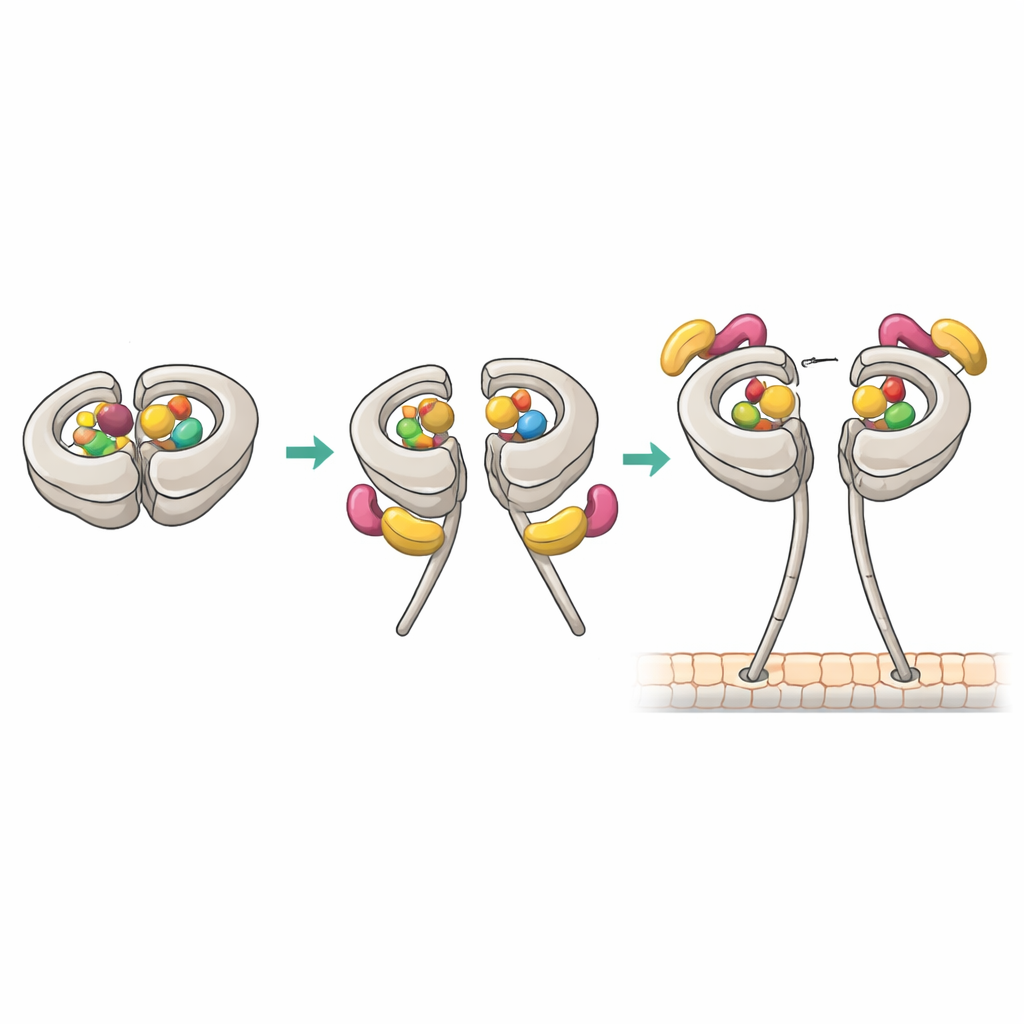
Elektronenmikroskopie verband dann den Bindungsmodus mit der Form. Wenn Pac1 einen 1:1-Komplex mit vollständig-längerem Dynein bildete, gingen die Motoren fast vollständig von der Phi-Konformation in eine offene Form über, bei der die beiden Köpfe in einem festen Abstand getrennt waren. Negative-Staining-Aufnahmen zeigten Pac1-Dimere, die die beiden Motordomänen überbrückten, was dem Abstand entsprach, der bei isolierten Motor–Pac1-Paaren beobachtet wurde. Im Gegensatz dazu blieb unter Bedingungen, die einen 1:2-Komplex begünstigten, Dynein in einer phi-ähnlichen Anordnung: flexibler und leicht verzerrt, aber weiterhin kompakt statt vollständig offen. Daraus folgt, dass nicht allein die Präsenz von Pac1 zählt, sondern genau, wie viele Pac1-Moleküle binden und an welchen Stellen.
Neue Kontaktpunkte, die die Klemme entriegeln
Cryo-Elektronenmikroskopie bei annähernd atomarer Auflösung zeigte, wie der produktive 1:1-Komplex aufgebaut ist. In diesem Zustand halten Dyneins primäre Stelle AAA1 und die regulatorische Stelle AAA4 jeweils ADP, während AAA3 leer ist. Dieses Nukleotidmuster korreliert mit hoher Affinität für Pac1. Eine WD40-„Klinge“ von Pac1 dockt an einer zuvor bekannten Stelle am Motorring an, aber die Struktur enthüllte außerdem einen zweiten Kontakt im flexiblen Linkerbereich von Dynein. Diese doppelte Greifstelle stabilisiert eine modifizierte „post-stroke“-Position des Linkers und drückt Pac1 leicht in Richtung des Stiels (Stalk), was wiederum die Bindung an einer zweiten ringnahen Stelle blockiert, die sonst eine weitere Pac1-WD40 beherbergen würde. Mutation des Linker-Kontakts schwächte Pac1s Fähigkeit, Dynein zu öffnen, veränderte die Bindungsstöchiometrie und beeinträchtigte dyneingetriebene Spindelbewegungen in Hefezellen, obwohl die grundlegende Motoraktivität erhalten blieb.
Vom biochemischen Schalter zur zellulären Bewegung
Aus der Verknüpfung dieser Ergebnisse schlagen die Autoren einen stufenweisen Aktivierungspfad vor. Dynein sitzt typischerweise in Phi mit ADP in mehreren Taschen, was Pac1 eine Bindung in einer Weise erlaubt, die den Motor nicht öffnet. Gelegentlich setzt eine regulatorische Tasche (AAA3) ADP frei, wodurch der Linker in eine bestimmte Position schwenken kann. In diesem Moment kann Pac1 sowohl am Ring als auch am Linker jedes Motorhaupts anklammern, sodass ein einzelnes Pac1-Dimer die beiden Köpfe überbrückt und eine offene Konformation stabilisiert, die eine hohe Affinität zu Mikrotubuli aufweist. Dieser offene Zustand ist dann bereit zur Andockung an Dynactin und Frachtadapter, um eine vollständig motile Transporteinheit zu bilden. Sobald Dynein ein Mikrotubulus bindet und zu laufen beginnt, schwächt sich Pac1s Griff und es dissoziiert, wodurch die Kontrolle an andere Regulatoren übergeben wird.
Warum das für Gesundheit und Krankheit wichtig ist
Für Nicht-Spezialisten lautet die Kernbotschaft: Dynein ist nicht einfach an- oder ausgeschaltet; es wird durch eine Kombination von Nukleotidzuständen und Lis1-Bindung fein abgestimmt, die zusammen eine Sicherheitslogik bilden. Erst wenn der richtige Nukleotidcode erscheint, wirkt Lis1 als molekularer Keil, öffnet den Motor und ermöglicht ihm, sich mit Dynactin zur Langstreckentransportmannschaft zusammenzuschließen. Da menschliches Lis1 für die Gehirnentwicklung essentiell ist und Fehlfunktionen Lissencephalie und andere neurologische Störungen verursachen, bietet das Verständnis dieses Codes auf atomarer Ebene eine Landkarte dafür, wie subtile Veränderungen in Lis1 oder Dynein die zelluläre Logistik und letztlich die Entwicklung des Organismus entgleisen können.
Zitation: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Schlüsselwörter: Dynein-Motor, Lis1 Pac1, molekularer Transport, Protein-Autoinhibition, Cryo-Elektronenmikroskopie