Clear Sky Science · pl
Kod nukleotydowy steruje zdolnością Lis1 do znoszenia autoinhibicji dyneiny
Jak komórki kontrolują swoje maleńkie pojazdy ładunkowe
Wnętrze każdej komórki zajmują miniaturowe maszyny, które przewożą ładunki wzdłuż cienkich torów, pomagając kształtować tkanki, dzielić chromosomy i ustawiać jądro. Jednym z najważniejszych takich przewoźników jest białko motoryczne dyneina. Ponieważ dyneina jest bardzo silna i szeroko wykorzystywana, komórki muszą utrzymywać ją bezpiecznie wyłączoną, dopóki nie będzie potrzebna. W tej pracy pokazano, jak inne białko — Lis1 (w drożdżach zwane Pac1) — odczytuje subtelny „kod nukleotydowy” w dyneinie, przełączając ją ze stanu złożonego, zablokowanego, do postaci otwartej i aktywnej, zdolnej do przemieszczania ładunku.
Molekularny silnik z blokadą bezpieczeństwa
Dyneina to duży, wieloczęściowy silnik, który porusza się po mikrotubulach, wewnętrznych torach komórki, transportując pęcherzyki, RNA, a nawet całe jądra. Aby uniknąć błędnego dostarczenia ładunku, dyneina zwykle pozostaje w samo-zaciskającej, autoinhibowanej konformacji nazywanej cząsteczką „phi”, w której jej dwie głowy silnikowe składają się razem i prawie nie oddziałują z mikrotubulami. Do długodystansowych biegów dyneina musi najpierw się rozłożyć, a następnie połączyć z kolejnym kompleksem — dynaktyną — oraz adaptorem ładunku. Wcześniejsze prace sugerowały, że Lis1 pomaga odblokować dyneinę, lecz szczegóły były niejasne, częściowo dlatego że pierścień motorowy dyneiny zawiera kilka kieszeni wiążących nukleotydy, z których każda może zawierać różne formy ATP lub ADP. Autorzy postanowili rozszyfrować, jak te kieszenie i wiązanie Lis1 razem kontrolują kształt dyneiny.
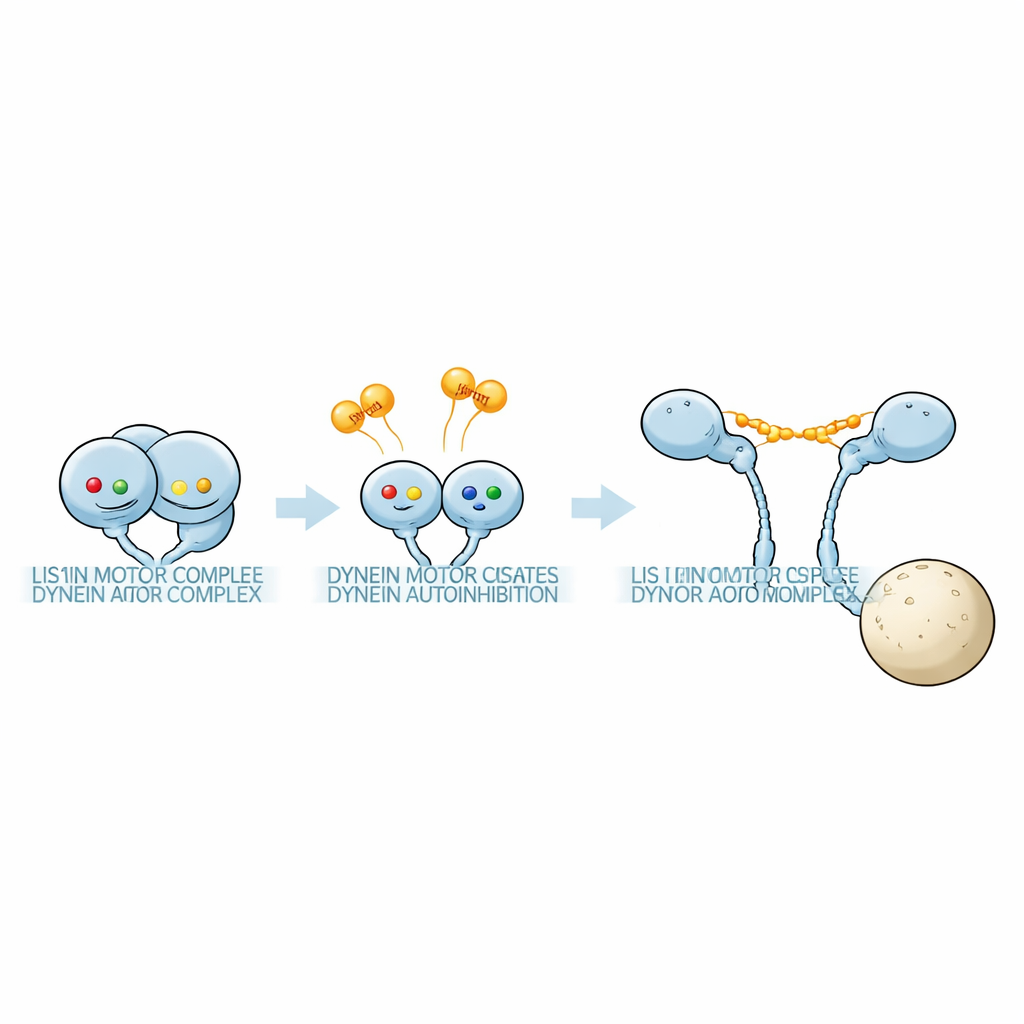
Odkrycie ukrytego nukleotydowego „kodu”
Zespół użył czułej fotometrii masowej, aby zważyć kompleksy białkowe w roztworach zawierających fragmenty motorowe dyneiny i Pac1 w różnych warunkach nukleotydowych. Pierścień motorowy dyneiny ma trzy aktywne kieszenie: AAA1, AAA3 i AAA4. Poprzez wprowadzenie precyzyjnych mutacji, które albo uniemożliwiały wiązanie nukleotydu, albo blokowały hydrolizę ATP w każdej z kieszeni, badacze mogli zamrozić poszczególne miejsca w określonych stanach. Stwierdzili, że kombinacja nukleotydów w tych trzech miejscach silnie wpływała na to, jak mocno Pac1 się wiązał i — co kluczowe — ile jednostek Pac1 przyłączało się do jednej dyneiny. W niektórych kombinacjach nukleotydowych dimer Pac1 mostkował dwie oddzielne cząsteczki dyneiny; w innych kontaktował się tylko z jednym silnikiem; a jeszcze w innych prawie wcale się nie wiązał. Te wzory ujawniły, że różne nukleotydowe „kody” wybierają między kompleksem 1:1 dyneina:Pac1 a kompleksem 1:2 z dodatkowymi jednostkami Pac1.
Jak Lis1 przekształca silnik
Mikroskopia elektronowa połączyła następnie tryb wiązania z kształtem. Gdy Pac1 tworzył kompleks 1:1 z pełnej długości dyneiną, silniki prawie całkowicie przeszły ze konformacji phi do formy otwartej, z dwiema głowami rozdzielonymi na ustaloną odległość. Obrazy barwione negatywnie pokazały dimer Pac1 mostkujący dwie domeny motorowe, co odpowiada odstępowi widzianemu w izolowanych parach motor–Pac1. W przeciwieństwie do tego, gdy warunki sprzyjały kompleksowi 1:2, dyneina pozostawała w układzie podobnym do phi: bardziej elastyczna i nieco zdeformowana, ale nadal zwarta zamiast w pełni otwartej. Zatem nie sama obecność Pac1 jest decydująca, lecz dokładnie ile cząsteczek Pac1 wiąże się i gdzie.
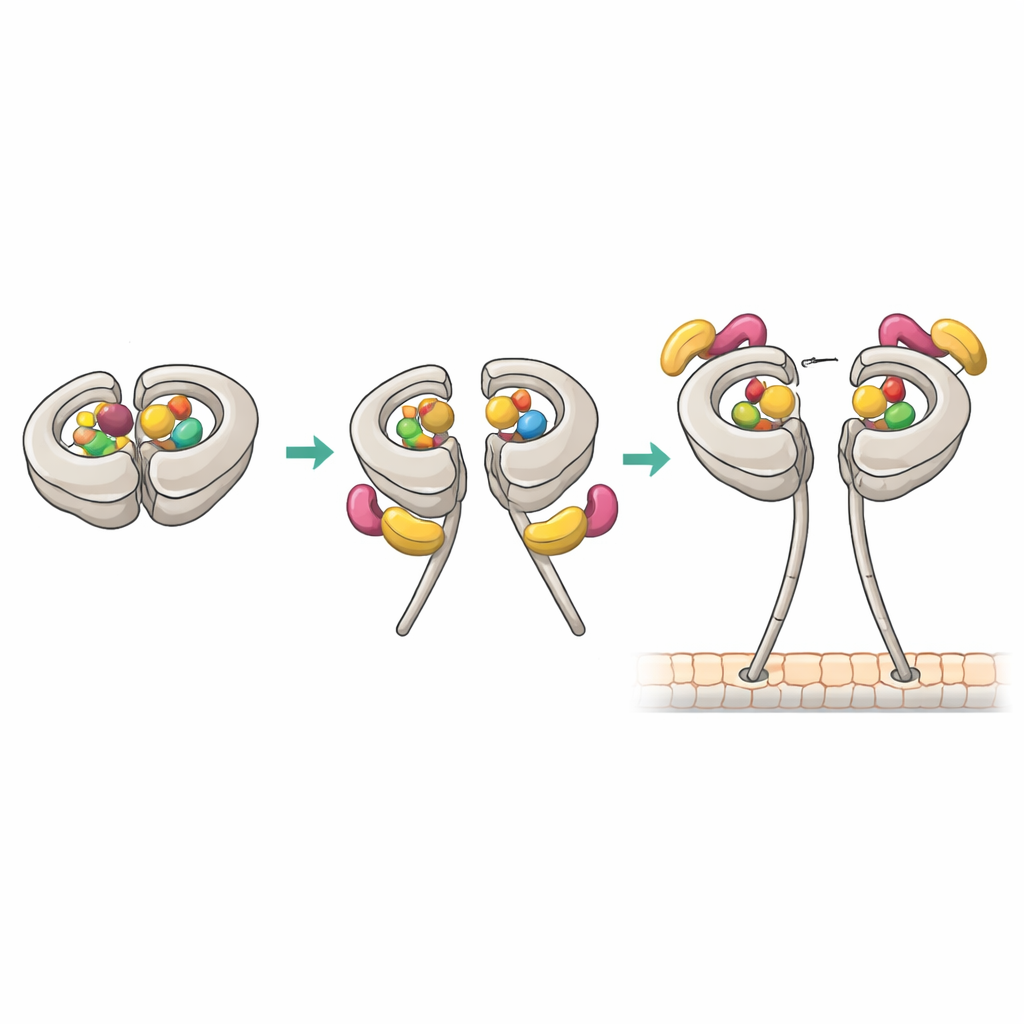
Nowe punkty kontaktu, które odblokowują zacisk
Krio-elektronowa mikroskopia o niemal atomowej rozdzielczości ujawniła, jak zbudowany jest produktywny kompleks 1:1. W tym stanie główne miejsce AAA1 dyneiny i regulacyjne AAA4 zawierały ADP, podczas gdy AAA3 było puste. Ten wzorzec nukleotydowy korelował z wysokim powinowactwem do Pac1. Jedno ostrze WD40 Pac1 dokuje w wcześniej znanym miejscu na pierścieniu motorowym, ale struktura odkryła także drugi punkt kontaktu na elastycznym odcinku łącznika dyneiny. Te podwójne punkty uchwytu stabilizują zmodyfikowaną, „pouderzeniową” pozycję łącznika i przesuwają Pac1 nieco w stronę trzonu (stalk), co z kolei blokuje wiązanie na drugim sąsiednim miejscu przy pierścieniu, które w przeciwnym razie mogłoby pomieścić kolejne WD40 Pac1. Mutacje w kontakcie łącznikowym osłabiły zdolność Pac1 do otwierania dyneiny, przesunęły stosunek wiązania i upośledziły ruchy wrzeciona napędzane przez dyneinę w komórkach drożdżowych, mimo że podstawowa aktywność silnika pozostała nienaruszona.
Od biochemicznego przełącznika do ruchu komórkowego
Skladując te wyniki, autorzy proponują krokową ścieżkę aktywacji. Dyneina zwykle siedzi w phi z ADP w kilku kieszeniach, co pozwala Pac1 wiązać się w sposób, który nie otwiera silnika. Sporadycznie jedno regulacyjne miejsce (AAA3) uwalnia ADP, pozwalając łącznikowi przechylić się do określonej pozycji. W tym momencie Pac1 może zablokować się zarówno na pierścieniu, jak i na łączniku każdej głowy silnikowej, tworząc pojedynczy dimer Pac1 mostkujący parę głów i stabilizując otwartą konformację o wysokim powinowactwie do mikrotubul. Ten stan otwarty jest następnie przygotowany do zadokowania na dynactynie i adapterach ładunku, tworząc w pełni ruchomą maszynę transportową. Gdy dyneina zaczyna angażować się z mikrotubulą i się poruszać, uścisk Pac1 słabnie i ulega dysocjacji, przekazując kontrolę innym regulatorom.
Dlaczego to ważne dla zdrowia i chorób
Dla czytelnika niebędącego specjalistą kluczowe przesłanie jest takie, że dyneina nie jest po prostu włączona lub wyłączona; jest regulowana przez kombinację stanów nukleotydowych i wiązania Lis1, które razem tworzą logikę bezpieczeństwa. Tylko gdy pojawi się odpowiedni kod nukleotydowy, Lis1 działa jak molekularny klin, otwierając silnik i umożliwiając mu dołączenie do długodystansowego zespołu transportowego z dynactyną. Ponieważ ludzki Lis1 jest niezbędny dla rozwoju mózgu, a jego zaburzenia powodują lissencefalię i inne choroby neurologiczne, zrozumienie tego kodu na atomowym poziomie daje mapę drogową, jak subtelne zmiany w Lis1 lub dyneinie mogą wykoleić logistykę komórkową, a ostatecznie rozwój organizmu.
Cytowanie: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Słowa kluczowe: kinetyka dyneiny, Lis1 Pac1, transport molekularny, autoinhibicja białka, krioelektronowa mikroskopia