Clear Sky Science · fr
Un code nucléotidique gouverne la capacité de Lis1 à lever l’autoinhibition de la dynéine
Comment les cellules contrôlent leurs minuscules transporteurs
À l’intérieur de chaque cellule, de minuscules machines transportent des cargaisons le long de rails fins, contribuant à façonner les tissus, à séparer les chromosomes et à positionner le noyau. L’un des plus importants de ces transporteurs est une protéine motrice appelée dynéine. Parce que la dynéine est très puissante et largement utilisée, les cellules doivent la maintenir désactivée tant qu’elle n’est pas nécessaire. Cet article révèle comment une autre protéine, Lis1 (appelée Pac1 chez la levure), lit un subtil « code nucléotidique » dans la dynéine pour la faire passer d’un état replié et verrouillé à une forme ouverte et active capable de déplacer des cargaisons.
Un moteur moléculaire avec un verrou de sécurité
La dynéine est un grand moteur multipartite qui chemine le long des microtubules, les rails internes de la cellule, transportant vésicules, ARN et même des noyaux entiers. Pour éviter les erreurs d’acheminement, la dynéine est normalement dans une conformation autoinhibée, auto-sertie, surnommée la particule « phi », dans laquelle ses deux têtes motrices se replient l’une sur l’autre et interagissent à peine avec les microtubules. Pour les trajets longue distance, la dynéine doit d’abord se déplier puis s’associer à un autre complexe, la dynactine, et à un adaptateur de cargaison. Des travaux antérieurs suggéraient que Lis1 aide à déverrouiller la dynéine, mais les détails restaient flous, en partie parce que le moteur de la dynéine contient plusieurs poches de liaison aux nucléotides pouvant chacune héberger différentes formes d’ATP ou d’ADP. Les auteurs ont entrepris de décoder comment ces poches, et la liaison de Lis1, coopèrent pour contrôler la conformation de la dynéine.
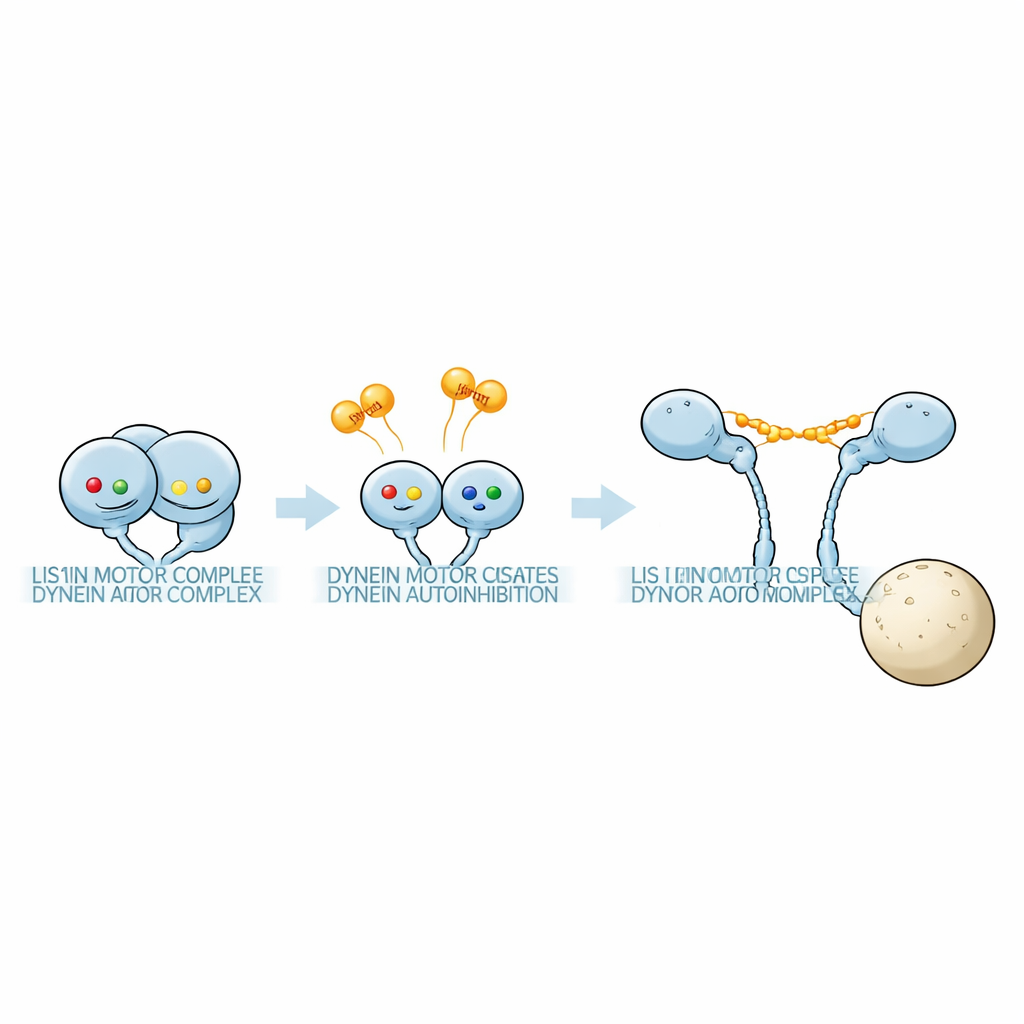
Découvrir un « code » nucléotidique caché
L’équipe a utilisé la photométrie de masse sensible pour mesurer la masse de complexes protéiques en solution contenant des fragments moteurs de la dynéine et Pac1 sous de nombreuses conditions nucléotidiques. La couronne motrice de la dynéine porte trois poches actives, AAA1, AAA3 et AAA4. En introduisant des mutations précises empêchant soit la liaison des nucléotides soit l’hydrolyse de l’ATP à chaque poche, les chercheurs ont pu verrouiller individuellement ces sites dans des états définis. Ils ont constaté que la combinaison de nucléotides dans ces trois sites influençait fortement l’affinité de liaison de Pac1 et, de manière cruciale, le nombre d’unités Pac1 attachées à chaque dynéine. Pour certaines combinaisons nucléotidiques, un dimère Pac1 relayait deux moteurs dynéine distincts ; pour d’autres, il ne contactait qu’un seul moteur ; et dans d’autres cas encore, il se liait à peine. Ces motifs ont révélé que des « codes » nucléotidiques distincts sélectionnent soit un complexe 1:1 dynéine:Pac1, soit un complexe 1:2 avec un Pac1 supplémentaire lié.
Comment Lis1 reconfigure le moteur
La microscopie électronique a ensuite relié le mode de liaison à la conformation. Lorsque Pac1 formait un complexe 1:1 avec la dynéine en pleine longueur, les moteurs passaient presque complètement de la conformation phi à une forme ouverte, les deux têtes étant séparées à une distance fixe. Des images en contraste négatif montraient des dimères Pac1 faisant la liaison entre les deux domaines moteurs, correspondant à l’espacement observé avec des paires moteur–Pac1 isolées. En revanche, lorsque les conditions favorisaient un complexe 1:2, la dynéine restait dans un agencement de type phi : plus flexible et légèrement déformée, mais toujours compacte plutôt que complètement ouverte. Ainsi, ce n’est pas simplement la présence de Pac1 qui importe, mais précisément combien de molécules de Pac1 se lient et où elles se fixent.
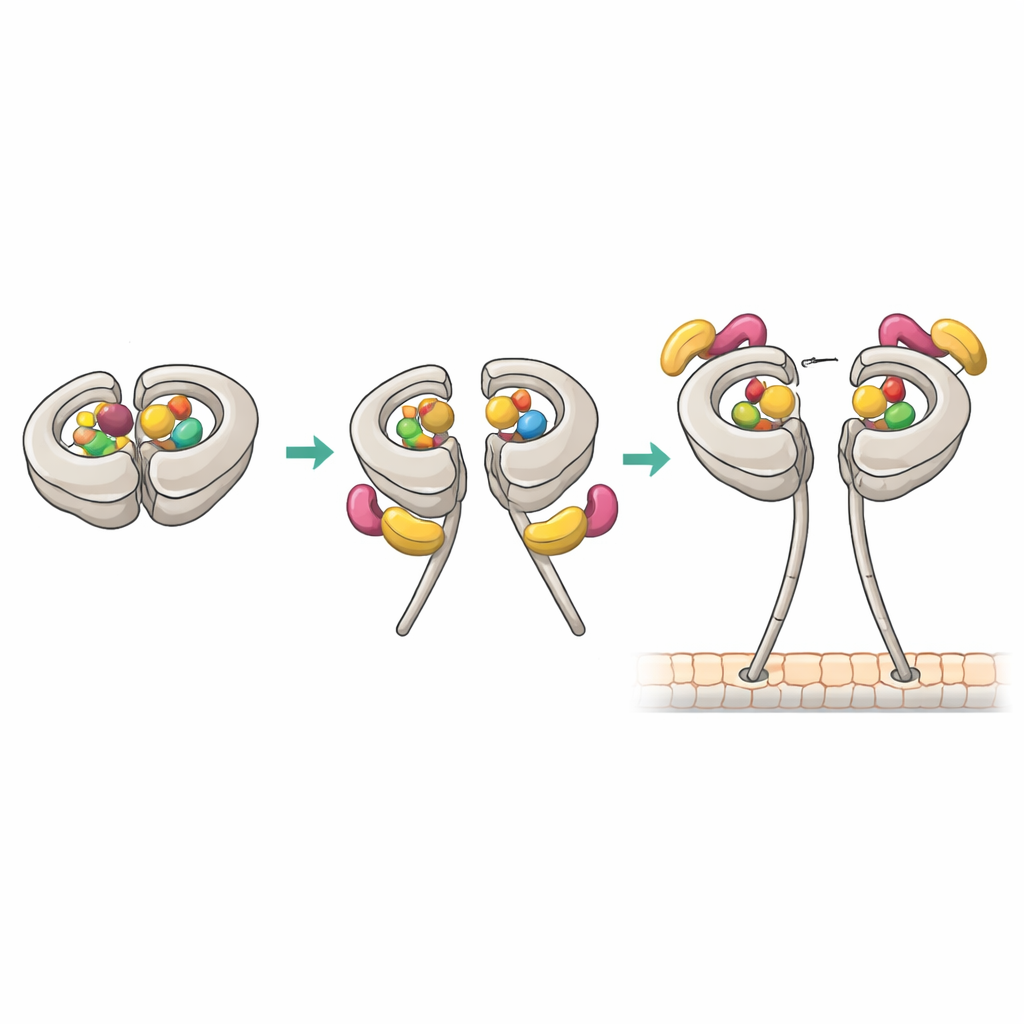
Nouveaux points de contact qui déverrouillent la pince
La cryo-microscopie électronique à résolution quasi atomique a révélé comment le complexe productif 1:1 est assemblé. Dans cet état, le site primaire de la dynéine, AAA1, et un site régulateur AAA4 contiennent tous deux de l’ADP, tandis que AAA3 est vide. Ce motif nucléotidique corrèle avec une forte affinité pour Pac1. Une « lame » WD40 de Pac1 s’arrime à un site déjà connu sur la couronne motrice, mais la structure a également mis au jour un second point de contact sur la région flexible du linker de la dynéine. Ces deux points d’ancrage stabilisent une position modifiée « post-stroke » du linker et poussent légèrement Pac1 vers la tige (stalk), ce qui bloque à son tour la liaison à un second site adjacent à la couronne qui hébergerait autrement un autre domaine WD40 de Pac1. La mutation du contact sur le linker affaiblissait la capacité de Pac1 à ouvrir la dynéine, modifiait la stœchiométrie de liaison et altérait les mouvements du fuseau induits par la dynéine dans des cellules de levure, bien que l’activité motrice de base reste intacte.
Du commutateur biochimique au mouvement cellulaire
En rassemblant ces résultats, les auteurs proposent une voie d’activation en plusieurs étapes. La dynéine se trouve typiquement en phi avec de l’ADP dans plusieurs poches, ce qui permet à Pac1 de se lier d’une manière qui n’ouvre pas le moteur. Parfois, une poche régulatrice (AAA3) libère l’ADP, permettant au linker de basculer dans une position particulière. À ce moment-là, Pac1 peut se fixer à la fois sur la couronne et sur le linker de chaque tête motrice, créant un dimère Pac1 unique reliant la paire de têtes et stabilisant une conformation ouverte avec une forte affinité pour les microtubules. Cet état ouvert est alors prêt à s’amarrer sur la dynactine et les adaptateurs de cargaison pour former une machine de transport pleinement motile. Une fois que la dynéine engage un microtubule et commence à marcher, la prise de Pac1 s’affaiblit et il se dissocie, transférant le contrôle à d’autres régulateurs.
Pourquoi cela compte pour la santé et la maladie
Pour un non-spécialiste, le message clé est que la dynéine n’est pas simplement allumée ou éteinte ; elle est réglée par une combinaison d’états nucléotidiques et par la liaison de Lis1 qui, ensemble, forment une logique de sécurité. Ce n’est que lorsque le bon code nucléotidique apparaît que Lis1 agit comme un coin moléculaire, ouvrant le moteur et lui permettant de rejoindre l’équipe de transport longue distance avec la dynactine. Parce que Lis1 humain est essentiel au développement cérébral et que son dysfonctionnement cause la lissencéphalie et d’autres troubles neurologiques, comprendre ce code au niveau atomique offre une feuille de route expliquant comment de subtiles altérations de Lis1 ou de la dynéine peuvent perturber la logistique cellulaire et, en fin de compte, le développement de l’organisme.
Citation: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Mots-clés: moteur dynéine, Lis1 Pac1, transport moléculaire, autoinhibition des protéines, cryo-microscopie électronique