Clear Sky Science · it
Un codice nucleotidico governa la capacità di Lis1 di alleviare l’autoinibizione della dineina
Come le cellule tengono sotto controllo i loro minuscoli trasportatori
All’interno di ogni cellula, macchine in miniatura trascinano carichi lungo sottili binari, contribuendo a modellare i tessuti, dividere i cromosomi e posizionare il nucleo. Uno dei più importanti di questi trasportatori è una proteina motrice chiamata dineina. Poiché la dineina è così potente e così ampiamente utilizzata, le cellule devono mantenerla spenta in modo sicuro fino al momento in cui serve. Questo articolo rivela come un’altra proteina, Lis1 (chiamata Pac1 nei lieviti), legga un sottile “codice nucleotidico” nella dineina per farla passare da uno stato ripiegato e bloccato a una forma aperta e attiva capace di muovere carico.
Un motore molecolare con un blocco di sicurezza
La dineina è un grande motore multiparte che cammina lungo i microtubuli, i binari interni della cellula, trasportando vescicole, RNA e persino interi nuclei. Per evitare consegne errate, la dineina normalmente si trova in una conformazione auto-bloccata e autoinibita soprannominata particella “phi”, nella quale le sue due teste motorie si ripiegano insieme e interagiscono debolmente con i microtubuli. Per corse a lunga distanza, la dineina deve prima dispiegarsi e poi associarsi a un altro complesso, la dinactina, più un adattatore del carico. Lavori precedenti avevano suggerito che Lis1 aiuti a sbloccare la dineina, ma i dettagli erano poco chiari, in parte perché il motore della dineina contiene diversi siti di legame per nucleotidi che possono ciascuno ospitare diverse forme di ATP o ADP. Gli autori si sono dunque posti l’obiettivo di decodificare come questi siti e il legame di Lis1 cooperino per controllare la forma della dineina.
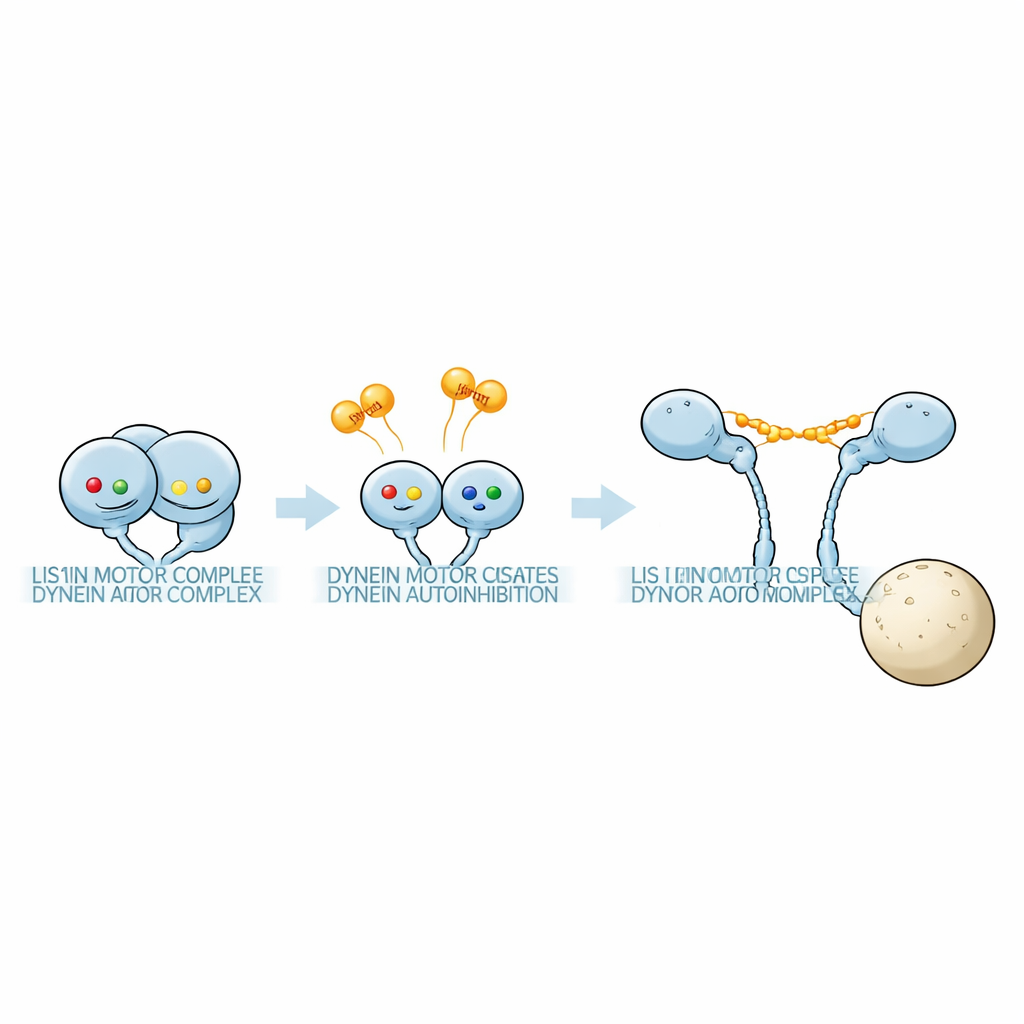
Scoprire un nascosto “codice” nucleotidico
Il gruppo ha usato una fotometria di massa sensibile per pesare complessi proteici in soluzioni contenenti frammenti del motore della dineina e Pac1 in molte condizioni nucleotidiche. Il anello motore della dineina porta tre siti attivi, AAA1, AAA3 e AAA4. Introdotto con mutazioni precise che impedivano il legame del nucleotide o bloccavano l’idrolisi dell’ATP in ciascun sito, i ricercatori hanno potuto fissare singoli siti in stati definiti. Hanno scoperto che la combinazione di nucleotidi in questi tre siti influenzava fortemente quanto strettamente Pac1 si legava e, cosa cruciale, quante unità di Pac1 si attaccavano a ogni dineina. In alcune combinazioni nucleotidiche, un dimero di Pac1 collegava due motori di dineina separati; in altre, contattava solo un motore; e in altre ancora si legava a malapena. Questi schemi hanno rivelato che distinti “codici” nucleotidici selezionano tra un complesso 1:1 dineina:Pac1 e un complesso 1:2 con Pac1 aggiuntivo legato.
Come Lis1 rimodella il motore
La microscopia elettronica ha poi correlato la modalità di legame con la forma. Quando Pac1 formava un complesso 1:1 con la dineina a lunghezza intera, i motori passavano quasi completamente dalla conformazione phi a una forma aperta, con le due teste separate a una distanza fissa. Immagini con contrasto negativo mostravano dimeri di Pac1 che collegavano i due domini motori, corrispondendo alla spaziatura osservata con coppie isolate motore–Pac1. Al contrario, quando le condizioni favorivano un complesso 1:2, la dineina restava in un arrangiamento simile al phi: più flessibile e leggermente distorto, ma ancora compatto anziché completamente aperto. Quindi non è semplicemente la presenza di Pac1 a contare, ma esattamente quante molecole di Pac1 si legano e dove.
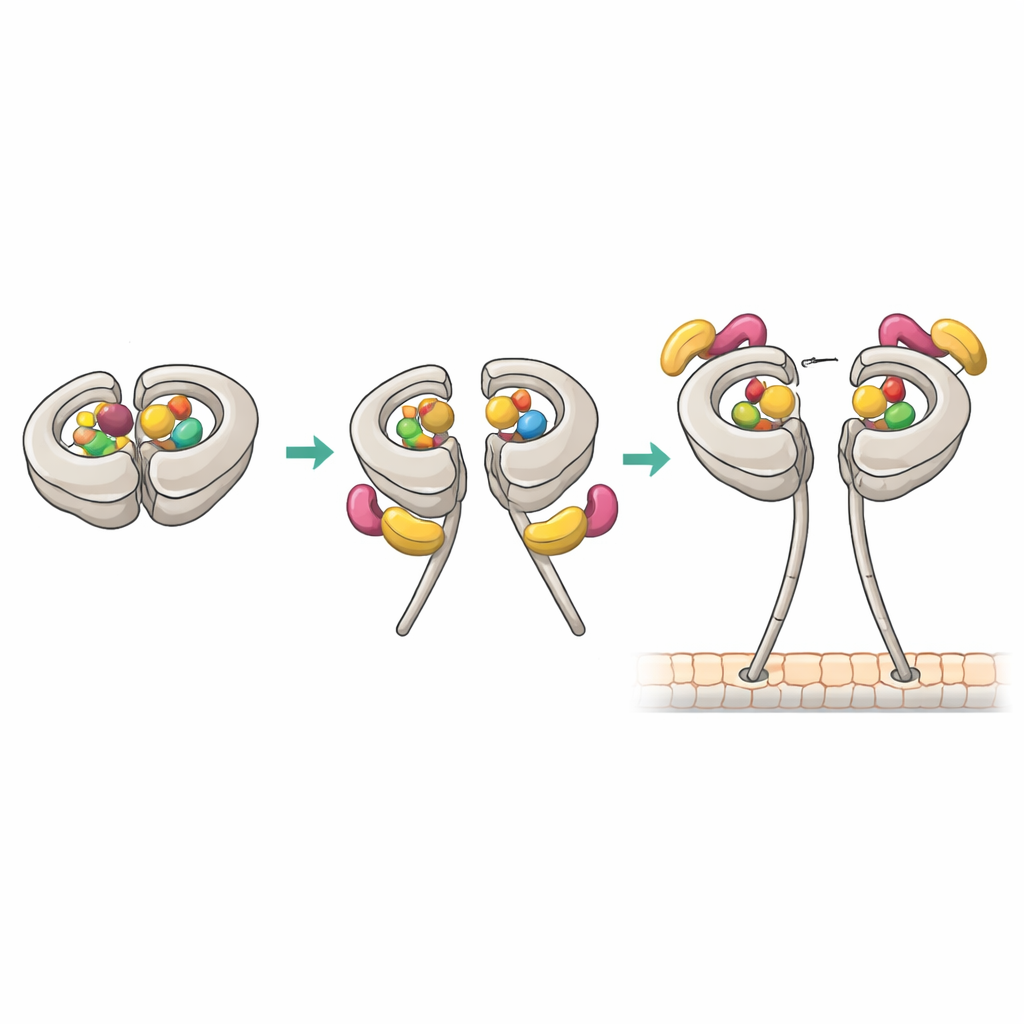
Nuovi punti di contatto che sbloccano la morsa
La crio-microscopia elettronica a risoluzione quasi atomica ha rivelato come è costruito il complesso produttivo 1:1. In quello stato, il sito primario della dineina AAA1 e un sito regolatorio AAA4 tengono entrambi ADP, mentre AAA3 è vuoto. Questo schema nucleotidico correla con un’alta affinità per Pac1. Una “lama” WD40 di Pac1 si ancora a un sito già noto sull’anello motore, ma la struttura ha anche scoperto un secondo contatto sulla regione flessibile del linker della dineina. Questi punti di presa doppi stabilizzano una posizione modificata del linker detta “post-stroke” e spostano leggermente Pac1 verso lo stelo, il che a sua volta blocca il legame a un secondo sito adiacente all’anello che altrimenti ospiterebbe un altro WD40 di Pac1. Mutare il contatto sul linker indeboliva la capacità di Pac1 di aprire la dineina, spostava la stechiometria del legame e comprometteva i movimenti del fuso guidati dalla dineina nelle cellule di lievito, sebbene l’attività motoria di base rimanesse intatta.
Dal commutatore biochimico al movimento cellulare
Mettendo insieme questi risultati, gli autori propongono un percorso di attivazione a tappe. La dineina tipicamente si trova in phi con ADP in diversi siti, il che permette a Pac1 di legarsi in modo che non apra il motore. Occasionalmente, un sito regolatorio (AAA3) rilascia ADP, permettendo al linker di oscillare in una posizione particolare. In quel momento, Pac1 può bloccare sia l’anello sia il linker di ciascuna testa motoria, creando un singolo dimero di Pac1 che collega la coppia di teste e stabilizza una conformazione aperta con alta affinità per i microtubuli. Questo stato aperto è quindi pronto per il docking sulla dinactina e sugli adattatori di carico per formare una macchina di trasporto pienamente motile. Una volta che la dineina si aggancia a un microtubulo e comincia a camminare, la presa di Pac1 si indebolisce e si dissocia, passando il controllo ad altri regolatori.
Perché questo è importante per salute e malattia
Per un non specialista, il messaggio chiave è che la dineina non è semplicemente accesa o spenta; essa è regolata da una combinazione di stati nucleotidici e dal legame di Lis1 che insieme formano una logica di sicurezza. Solo quando appare il giusto codice nucleotidico Lis1 agisce come uno spessore molecolare, aprendo il motore e permettendogli di unirsi al team di trasporto a lunga distanza con la dinactina. Poiché la Lis1 umana è essenziale per lo sviluppo cerebrale e il suo malfunzionamento causa la lissencefalia e altri disturbi neurologici, comprendere questo codice a livello atomico offre una mappa di come cambiamenti sottili in Lis1 o nella dineina possano mandare in tilt la logistica cellulare e, in ultima analisi, lo sviluppo dell’organismo.
Citazione: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Parole chiave: motore dineina, Lis1 Pac1, trasporto molecolare, autoinibizione proteica, crio microscopia elettronica