Clear Sky Science · es
Un código nucleotídico gobierna la capacidad de Lis1 para aliviar la autoinhibición de la dineína
Cómo las células mantienen bajo control a sus diminutos porteadores
Dentro de cada célula, máquinas en miniatura transportan carga a lo largo de finas vías, contribuyendo a moldear tejidos, dividir cromosomas y posicionar el núcleo. Uno de los portadores más importantes es una proteína motora llamada dineína. Debido a que la dineína es muy potente y ampliamente utilizada, las células deben mantenerla apagada de forma segura hasta que sea necesaria. Este artículo revela cómo otra proteína, Lis1 (llamada Pac1 en levaduras), interpreta un sutil “código nucleotídico” en la dineína para cambiarla de un estado plegado y bloqueado a una forma abierta y activa capaz de mover carga.
Un motor molecular con un seguro de seguridad
La dineína es un gran motor multipartito que camina sobre microtúbulos, las vías internas de la célula, transportando vesículas, ARN e incluso núcleos completos. Para evitar entregas equivocadas, la dineína normalmente permanece en una conformación auto-asegurada y autoinhibida apodada la partícula “phi”, en la que sus dos cabezas motoras se pliegan juntas y apenas interactúan con los microtúbulos. Para trayectos de larga distancia, la dineína debe primero desplegarse y luego asociarse con otro complejo, la dinactina, además de un adaptador de carga. Trabajos anteriores sugerían que Lis1 ayuda a desbloquear la dineína, pero los detalles eran confusos, en parte porque el motor de la dineína contiene varios bolsillos de unión a nucleótidos que pueden albergar distintas formas de ATP o ADP. Los autores se propusieron descifrar cómo esos bolsillos y la unión de Lis1 actúan conjuntamente para controlar la forma de la dineína.
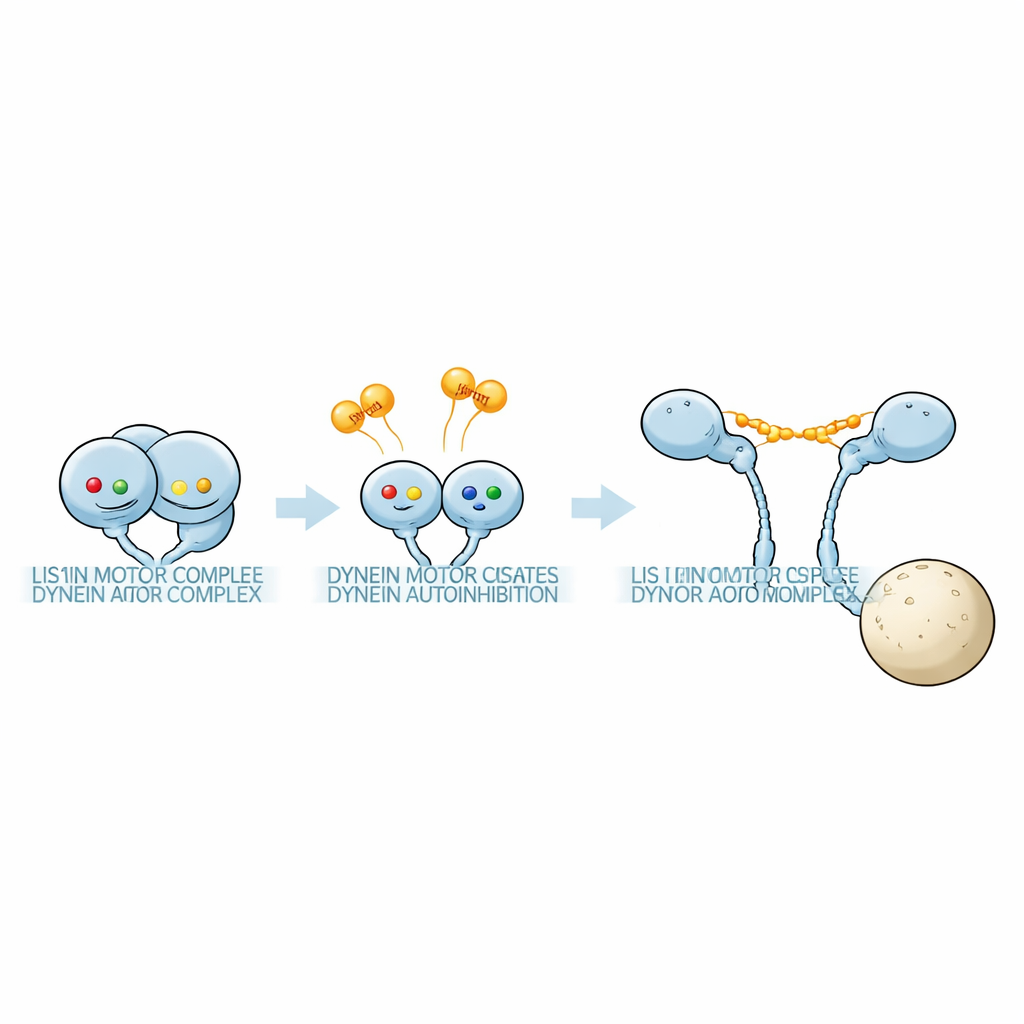
Descubriendo un “código” nucleotídico oculto
El equipo utilizó fotometría de masas sensible para pesar complejos proteicos en soluciones que contenían fragmentos del motor de la dineína y Pac1 bajo diversas condiciones nucleotídicas. El anillo motor de la dineína alberga tres bolsillos activos, AAA1, AAA3 y AAA4. Introduciendo mutaciones precisas que impiden la unión de nucleótidos o bloquean la hidrólisis de ATP en cada bolsillo, los investigadores pudieron fijar sitios individuales en estados definidos. Encontraron que la combinación de nucleótidos en estos tres sitios influye fuertemente en la afinidad de unión de Pac1 y, de forma crucial, en cuántas unidades de Pac1 se asociaban a cada dineína. En algunas combinaciones nucleotídicas, un dímero de Pac1 puenteaba dos motores de dineína separados; en otras, contactaba solo un motor; y en otras apenas se unía. Estos patrones revelaron que distintos “códigos” nucleotídicos seleccionan entre un complejo 1:1 dineína:Pac1 y un complejo 1:2 con Pac1 adicional unido.
Cómo Lis1 remodela el motor
La microscopia electrónica vinculó luego el modo de unión con la conformación. Cuando Pac1 formaba un complejo 1:1 con la dineína de longitud completa, los motores casi por completo cambiaban de la conformación phi a una forma abierta, con las dos cabezas separadas a una distancia fija. Imágenes con tinción negativa mostraron dímeros de Pac1 puenteando los dos dominios motores, coincidiendo con la separación observada en pares aislados motor–Pac1. En contraste, cuando las condiciones favorecían un complejo 1:2, la dineína permanecía en una disposición similar a phi: más flexible y ligeramente distorsionada, pero aún compacta en lugar de totalmente abierta. Así, no basta con la presencia de Pac1: importa exactamente cuántas moléculas de Pac1 se unen y dónde lo hacen.
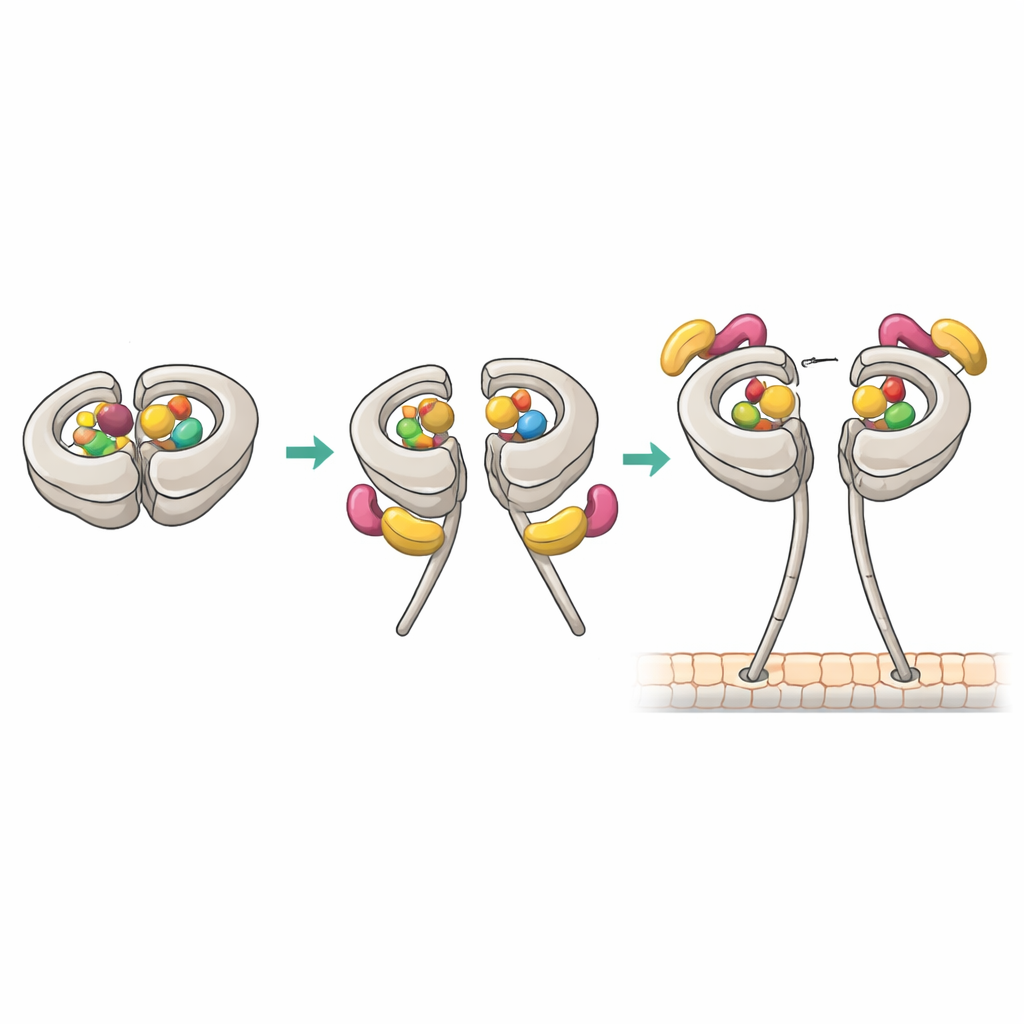
Nuevos puntos de contacto que desbloquean la abrazadera
La crio-microscopía electrónica a resolución casi atómica reveló cómo se construye el complejo productivo 1:1. En ese estado, el sitio primario AAA1 y un sitio regulatorio AAA4 de la dineína contienen ADP, mientras que AAA3 está vacío. Este patrón de nucleótidos se correlaciona con alta afinidad por Pac1. Una “hoja” WD40 de Pac1 se acopla en un sitio previamente conocido del anillo motor, pero la estructura también descubrió un segundo contacto en la región flexible del conector (linker) de la dineína. Estos dos puntos de agarre estabilizan una posición modificada de tipo “post-stroke” del conector y desplazan ligeramente a Pac1 hacia el tallo (stalk), lo que a su vez bloquea la unión en un segundo sitio adyacente al anillo que de otro modo alojaría otra WD40 de Pac1. Mutar el contacto del conector debilitó la capacidad de Pac1 para abrir la dineína, cambió la estequiometría de unión e impidió los movimientos del huso impulsados por dineína en células de levadura, aunque la actividad motora básica permaneció intacta.
Del interruptor bioquímico al movimiento celular
Uniendo estos resultados, los autores proponen una vía de activación por pasos. La dineína típicamente yace en phi con ADP en varios bolsillos, lo que permite que Pac1 se una de una forma que no abre el motor. Ocasionalmente, un bolsillo regulatorio (AAA3) libera ADP, permitiendo que el conector gire a una posición particular. En ese momento, Pac1 puede sujetarse tanto al anillo como al conector de cada cabeza motora, creando un dímero único de Pac1 que puentea el par de cabezas y estabiliza una conformación abierta con alta afinidad por los microtúbulos. Este estado abierto queda entonces preparado para acoplarse a la dinactina y a los adaptadores de carga para formar una máquina de transporte totalmente motora. Una vez que la dineína se engancha a un microtúbulo y comienza a caminar, el agarre de Pac1 se debilita y se disocia, cediendo el control a otros reguladores.
Por qué esto importa para la salud y la enfermedad
Para un público no especializado, el mensaje clave es que la dineína no se limita a estar simplemente activada o desactivada; su actividad se regula por una combinación de estados nucleotídicos y la unión de Lis1 que, juntos, forman una lógica de seguridad. Solo cuando aparece el código nucleotídico correcto actúa Lis1 como una cuña molecular, abriendo el motor y permitiéndole integrarse al equipo de transporte de larga distancia con la dinactina. Dado que Lis1 humano es esencial para el desarrollo cerebral y su malfuncionamiento causa lisencefalia y otros trastornos neurológicos, entender este código a detalle atómico ofrece una hoja de ruta de cómo cambios sutiles en Lis1 o la dineína pueden descarrilar la logística celular y, en última instancia, el desarrollo del organismo.
Cita: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Palabras clave: motor de dineína, Lis1 Pac1, transporte molecular, autoinhibición de proteínas, crioelectrónica (cryo-EM)