Clear Sky Science · ru
Нуклеотидный код управляет способностью Lis1 снимать автозатворение динеина
Как клетки держат под контролем своих крошечных грузоперевозчиков
В каждой клетке миниатюрные машины перемещают грузы по тонким рельсам, помогая формировать ткани, делить хромосомы и позиционировать ядро. Один из важнейших таких «грузчиков» — моторный белок динеин. Поскольку динеин очень мощный и широко используется, клетки должны удерживать его выключенным до тех пор, пока он не понадобится. В этой статье показано, как другой белок — Lis1 (в дрожжах называемый Pac1) — считывает тонкий «нуклеотидный код» в динеине, переводя его из сложенного, заблокированного состояния в раскрытую, активную форму, способную транспортировать грузы.
Молекулярный двигатель с предохранителем
Динеин — большой многокомпонентный мотор, который ходит по микротрубочкам, внутренним «рельсам» клетки, перенося везикулы, РНК и даже целые ядра. Чтобы избежать неправильной доставки, динеин обычно находится в самозакрывающейся, автоподавленной конформации, прозванной «фи»-частицей, в которой его две моторные головы складываются вместе и едва взаимодействуют с микротрубочками. Для дальних перемещений динеин сначала должен развернуться, а затем соединиться с другим комплексом — динaктином, — а также с адаптером груза. Ранее были указания, что Lis1 помогает разблокировать динеин, но детали оставались неясными, отчасти потому, что мотор динеина содержит несколько сайтов связывания нуклеотидов, каждый из которых может содержать разные формы АТФ или АДФ. Авторы поставили цель расшифровать, как эти сайты и связывание Lis1 вместе контролируют форму динеина.
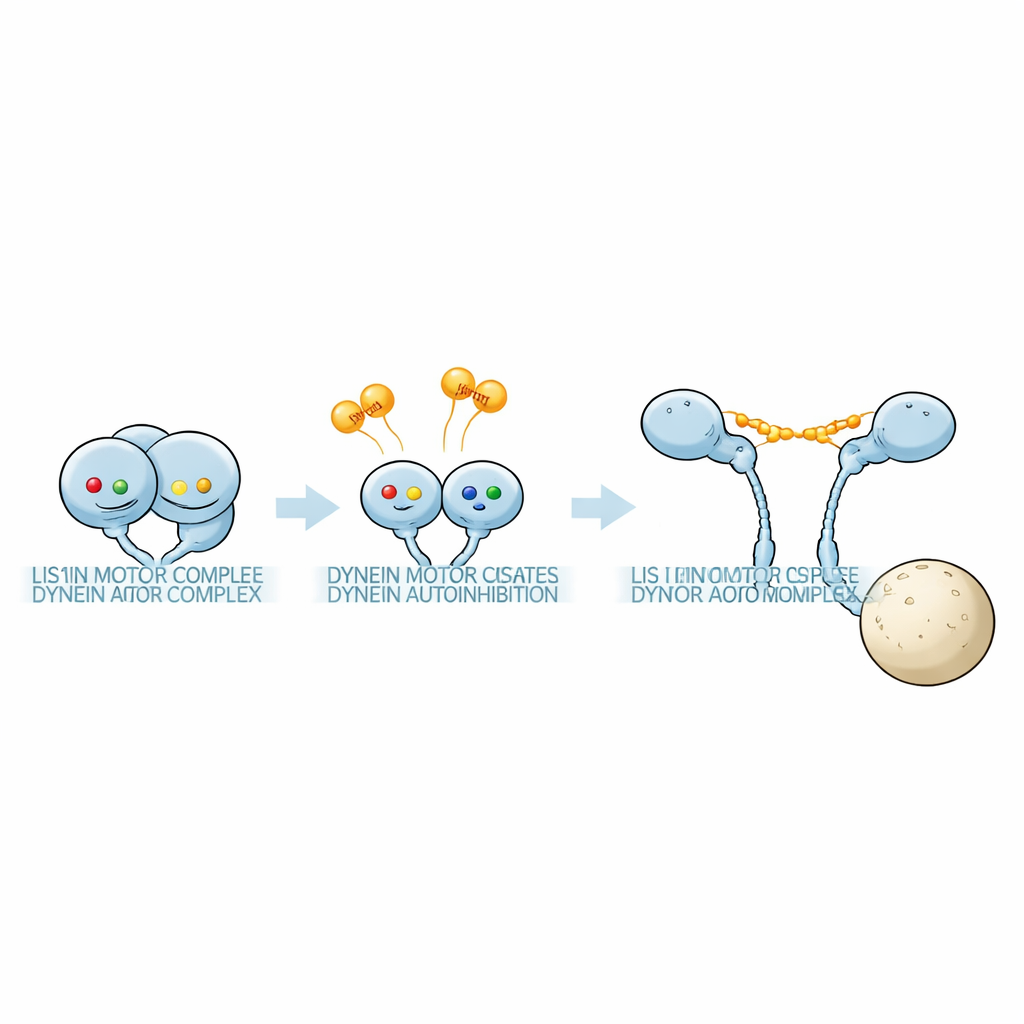
Открытие скрытого нуклеотидного «кода»
Группа использовала чувствительную масс-фотометрию, чтобы взвесить белковые комплексы в растворах, содержащих фрагменты моторного домена динеина и Pac1 при разных нуклеотидных условиях. Моторное кольцо динеина несет три активных кармана — AAA1, AAA3 и AAA4. Вводя точечные мутации, которые либо не позволяют нуклеотиду связываться, либо блокируют гидролиз АТФ в каждом кармане, исследователи могли зафиксировать отдельные сайты в определенных состояниях. Они обнаружили, что сочетание нуклеотидов в этих трех сайтах сильно влияет на то, насколько прочно связывается Pac1 и, что важно, сколько молекул Pac1 присоединяется к каждому динеину. При одних нуклеотидных комбинациях димер Pac1 мостил два отдельных динеина; при других он контактировал только с одним мотором; а в некоторых случаях практически не связывался вовсе. Эти закономерности показали, что разные нуклеотидные «коды» выбирают между комплексом динеин:Pac1 1:1 и комплексом 1:2 с дополнительным Pac1.
Как Lis1 перестраивает мотор
Электронная микроскопия затем связала режим связывания с формой молекулы. Когда Pac1 образовывал комплекс 1:1 с полноценным динеином, моторы почти полностью переходили из фи-конформации в открытую форму, с двумя головами, разнесенными на фиксированное расстояние. Негативное крашение показало димеры Pac1, мостящие две моторные домены, что соответствовало расстоянию, наблюдаемому для изолированных пар мотор–Pac1. Напротив, когда условия благоприятствовали комплексу 1:2, динеин оставался в фи-подобной компоновке: более гибкий и слегка искажённый, но всё ещё компактный, а не полностью раскрытый. Таким образом, важно не просто присутствие Pac1, а точное число молекул Pac1 и места их связывания.
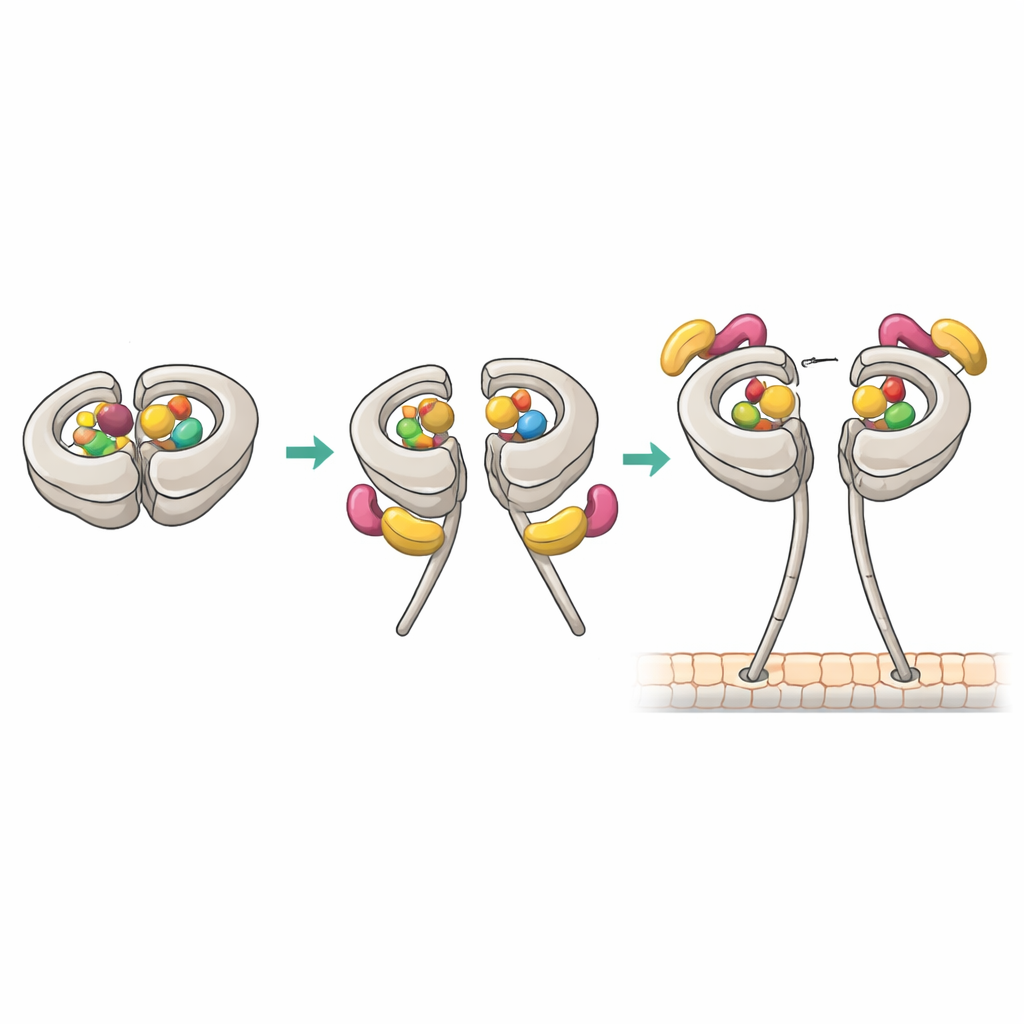
Новые точки контакта, которые разблокируют зажим
Крио-ЭМ с почти атомным разрешением показала, как устроен продуктивный комплекс 1:1. В этом состоянии основной сайт динеина AAA1 и регуляторный сайт AAA4 оба содержат АДФ, в то время как AAA3 пуст. Эта нуклеотидная схема коррелирует с высокой аффинностью к Pac1. Одна «лезвие» WD40 домена Pac1 докируется к ранее известному участку на моторном кольце, но структура также выявила второй контакт в гибком участке линкера динеина. Эти двойные точки захвата стабилизируют модифицированное «пост-ударное» положение линкера и смещают Pac1 немного в сторону стебля, что, в свою очередь, блокирует связывание на втором прилегающем к кольцу сайте, который в противном случае принял бы другой WD40 Pac1. Мутации в участке контакта с линкером ослабляли способность Pac1 раскрывать динеин, изменяли стехиометрию связывания и нарушали движения веретена, управляемые динеином, в дрожжевых клетках, хотя базовая моторная активность оставалась неизменной.
От биохимического переключателя к клеточному перемещению
Собрав эти данные воедино, авторы предлагают пошаговый путь активации. Обычно динеин находится в фи с АДФ в нескольких карманах, что позволяет Pac1 связываться так, что мотор не раскрывается. Временами один регуляторный карман (AAA3) освобождает АДФ, позволяя линкеру повернуться в определённое положение. В этот момент Pac1 может зажать и кольцо, и линкер каждой моторной головы, образуя один димер Pac1, мостящий пару голов и стабилизирующий открытую конформацию с высокой аффинностью к микротрубочкам. Это открытое состояние затем готово для присоединения к динaктину и адаптерам груза, чтобы сформировать полностью подвижную транспортную машину. Когда динеин сцепляется с микротрубочкой и начинает «идти», захват Pac1 ослабевает и он диссоциирует, передавая контроль другим регуляторам.
Почему это важно для здоровья и болезней
Для неспециалиста главный вывод таков: динеин не просто включается или выключается; его настраивает комбинация нуклеотидных состояний и связывания Lis1, которые вместе образуют логическую систему безопасности. Лишь при появлении правильного нуклеотидного кода Lis1 действует как молекулярная клинья, открывая мотор и позволяя ему присоединиться к «команде» для дальнего транспорта вместе с динaктином. Поскольку человеческий Lis1 необходим для развития мозга и его дисфункция вызывает лиссенцефалию и другие неврологические расстройства, понимание этого кода на атомном уровне дает дорожную карту того, как тонкие изменения в Lis1 или динеине могут сбивать с толку внутриклеточную логистику и в конечном итоге нарушать развитие организма.
Цитирование: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Ключевые слова: мотор динеин, Lis1 Pac1, молекулярный транспорт, автозатворение белков, криоэлектронная микроскопия