Clear Sky Science · ja
ヌクレオチドコードがLis1のダイニン自己不活性化解除能を制御する
細胞が小さな貨物運搬機をどう制御しているか
細胞内では、小さな機械が細いレールに沿って貨物を牽引し、組織形成、染色体分配、核の配置に寄与しています。その中でも特に重要なのがダイニンというモータータンパク質です。ダイニンは強力で用途が広いため、細胞は必要なとき以外はこれを安全にオフにしておく必要があります。本論文は、別のタンパク質であるLis1(酵母ではPac1と呼ばれる)が、ダイニンの微妙な「ヌクレオチドコード」を読み取り、折りたたまれてロックされた状態から貨物を動かせる開いた活性形へと切り替える仕組みを明らかにします。
安全ロックを備えた分子エンジン
ダイニンは大きく複数の部分からなるモーターで、細胞内部のレールである微小管に沿って小胞、RNA、さらには核全体を運ぶ働きをします。誤配達を防ぐため、ダイニンは通常「phi」粒子と呼ばれる自己クランプされた自己不活性構造で休止し、二つのモーターヘッドが折りたたまれて微小管とほとんど相互作用しません。長距離走行には、まずダイニンが展開してから、別の複合体であるダイナクチンと貨物アダプターと結合する必要があります。以前の研究はLis1がダイニンのロックを解除するのを助けることを示唆していましたが、ダイニンのモーターが複数のヌクレオチド結合ポケットを持ち、それぞれがATPやADPの異なる形を保持し得るため、詳細は不明な点が残っていました。著者らは、これらのポケットとLis1結合がどのように協調してダイニンの形状を制御するのかを解読しようとしました。
隠れたヌクレオチド「コード」の発見
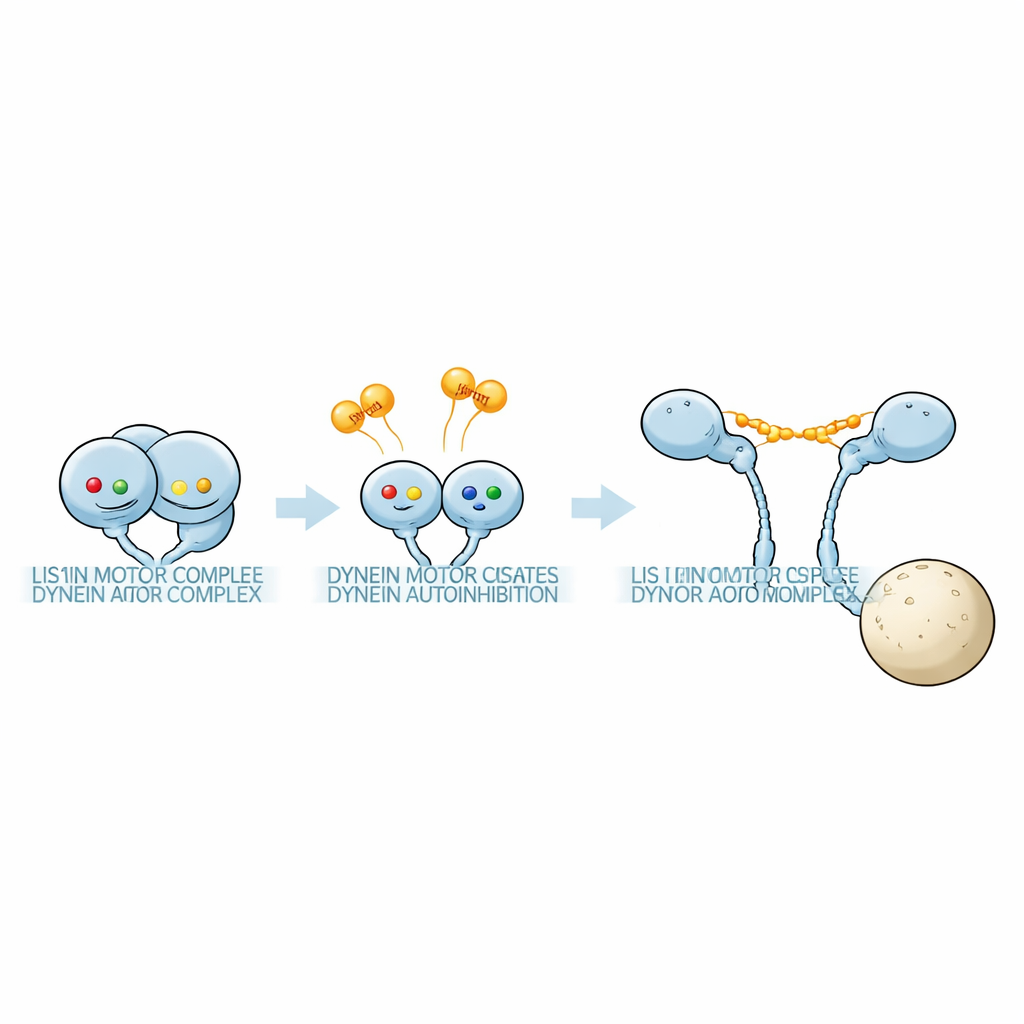
研究チームは感度の高い質量光計測(マスフォトメトリー)を用いて、さまざまなヌクレオチド条件下でダイニンのモーターフラグメントとPac1を含む溶液中のタンパク質複合体の質量を測定しました。ダイニンのモーターリングには三つの活性ポケット、AAA1、AAA3、AAA4があります。それぞれのポケットでヌクレオチド結合を阻止したりATP加水分解を遮断したりする精密な変異を導入することで、個々の部位を特定の状態に固定できました。彼らは、これら三つの部位のヌクレオチドの組み合わせがPac1の結合の強さ、そして決定的には各ダイニンに何個のPac1が結合するかに強く影響することを発見しました。あるヌクレオチドの組み合わせではPac1のダイマーが二つの別々のダイニンを橋渡しし、別の組み合わせでは一つのモーターにのみ接触し、さらに別の組み合わせではほとんど結合しませんでした。これらのパターンは、異なるヌクレオチド「コード」が1:1のダイニン:Pac1複合体と、余分なPac1が結合した1:2複合体を選択することを示しました。
Lis1がモーターをどう変形させるか
続いて電子顕微鏡により結合様式と形状が結び付けられました。Pac1が全長ダイニンと1:1複合体を形成すると、モーターはほぼ完全にphi構造から開いた形へと移行し、二つのヘッドは一定の距離で分離しました。ネガティブ・ステイン像はPac1ダイマーが二つのモータードメインを橋渡ししている様子を示し、単離したモーター–Pac1対で見られた間隔と一致しました。対照的に、1:2複合体を好む条件ではダイニンはphi様の配列のまま残り、より柔軟でわずかに歪んでいるものの完全に開くのではなくコンパクトな状態でした。つまり重要なのは単にPac1が存在するかどうかではなく、何個のPac1がどこに結合するかという点です。
クランプを解除する新たな接触点
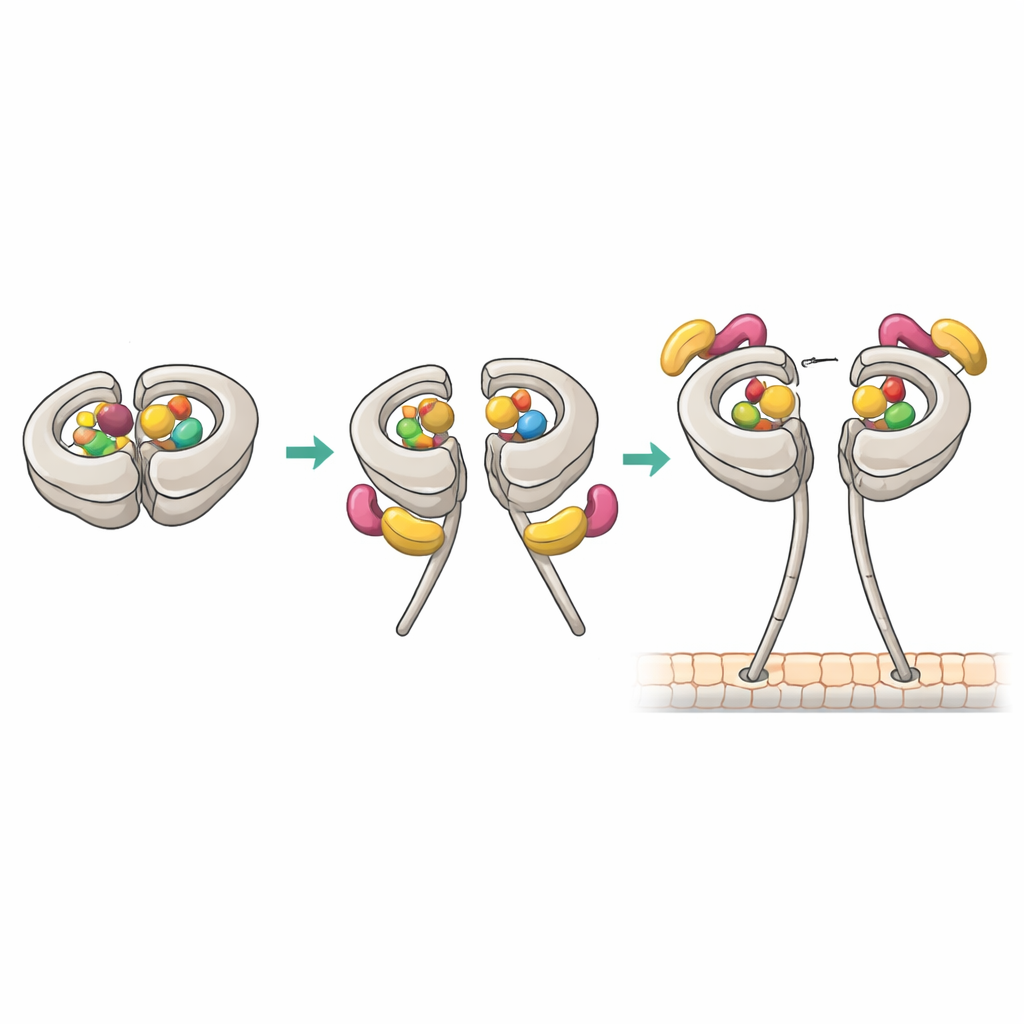
クライオ電子顕微鏡による原子近傍の解像度で、実効的な1:1複合体がどのように構築されるかが明らかになりました。その状態では、ダイニンの主要部位AAA1と調節部位AAA4はともにADPを保持し、AAA3は空の状態でした。このヌクレオチドパターンはPac1に対する高い親和性と相関します。Pac1の一つのWD40ブレードはモーターリング上の既知の部位にドッキングしますが、構造解析はダイニンの柔軟なリンカー領域に第二の接触点があることも明らかにしました。これら二つの把握点がリンカーの修飾された“ポストストローク”位置を安定化し、Pac1を茎(ストーク)方向へわずかに押しやることで、本来なら別のPac1 WD40が占めるはずのリング隣接部位への結合を阻害します。リンカー接触を変異させるとPac1のダイニンを開く能力が弱まり、結合の化学量論が変化し、酵母細胞におけるダイニン駆動の紡錘体移動が損なわれましたが、基礎的なモーター活性自体は損なわれませんでした。
生化学的スイッチから細胞レベルの運動へ
これらの結果をつなぎ合わせて、著者らは段階的な活性化経路を提案します。ダイニンは通常いくつかのポケットにADPを抱えたphi状態にあり、その状態ではPac1がモーターを開かない結合様式で結合できます。時折、ある調節ポケット(AAA3)がADPを放出し、リンカーが特定の位置に振れることがあります。その瞬間、Pac1は各モーターヘッドのリングとリンカーの両方にかしめるように結合でき、二つのヘッドを橋渡しする単一のPac1ダイマーを作り、微小管への高い親和性を持つ開いた構造を安定化します。この開いた状態はダイナクチンや貨物アダプターへのドッキングに備えられ、完全な輸送マシンとして機能します。いったんダイニンが微小管に取り付き歩行を始めると、Pac1の把握は弱まり解離し、制御は他の調節因子に引き渡されます。
健康と疾患にとっての意義
専門外の人への要点は、ダイニンが単純にオン・オフされるわけではなく、ヌクレオチド状態の組み合わせとLis1結合が連動して安全ロジックを形成しているということです。適切なヌクレオチドコードが出現したときにのみ、Lis1は分子のくさびとして働き、モーターを開いてダイナクチンとともに長距離輸送隊に参加できるようにします。ヒトのLis1は脳発達に不可欠で、その機能不全がリッサンセファリーや他の神経疾患を引き起こすため、このコードを原子レベルで理解することは、Lis1やダイニンのわずかな変化が細胞の物流をどのように狂わせ、最終的に個体の発達にどのように影響するかを示す羅針盤となります。
引用: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
キーワード: ダイニンモーター, Lis1 Pac1, 分子輸送, タンパク質の自己不活性化, クライオ電子顕微鏡