Clear Sky Science · nl
Een nucleotidecode bestuurt Lis1’s vermogen om dynein-autoinhibitie op te heffen
Hoe cellen hun kleine vrachtvervoerders onder controle houden
Binnen elke cel slepen miniatuurmachines lading langs fijne rails, waarmee ze helpen weefsels te vormen, chromosomen te verdelen en de plaats van de kern te bepalen. Een van de belangrijkste van deze transporteurs is het motorproteïne dynein. Omdat dynein zo krachtig en zo veelgebruikt is, moeten cellen het veilig uitgeschakeld houden totdat het nodig is. Dit onderzoek laat zien hoe een ander eiwit, Lis1 (in gist Pac1 genoemd), een subtiele "nucleotidecode" in dynein leest om het van een gevouwen, vergrendelde toestand naar een open, actieve vorm te schakelen die lading kan verplaatsen.
Een moleculaire motor met een veiligheidsslot
Dynein is een groot, samengesteld motorcomplex dat langs microtubuli loopt, de intracellulaire rails, en blaasjes, RNA en zelfs volledige kernen vervoert. Om mislevering te vermijden zit dynein meestal in een zelfgeklampte, autoinhiberende conformatie, de zogenaamde "phi"-deeltje, waarin de twee motorhoofden tegen elkaar gevouwen zijn en nauwelijks met microtubuli interageren. Voor langeafstandsritten moet dynein eerst ontvouwen en zich vervolgens binden aan een ander complex, dynactine, plus een ladingadapter. Eerder werk suggereerde dat Lis1 helpt dynein te ontgrendelen, maar de details waren onduidelijk, deels omdat de motor van dynein meerdere nucleotidebindende pockets bevat die elk verschillende vormen van ATP of ADP kunnen bevatten. De auteurs wilden ontcijferen hoe die pockets en Lis1-binding samen werken om dynein’s vorm te sturen.
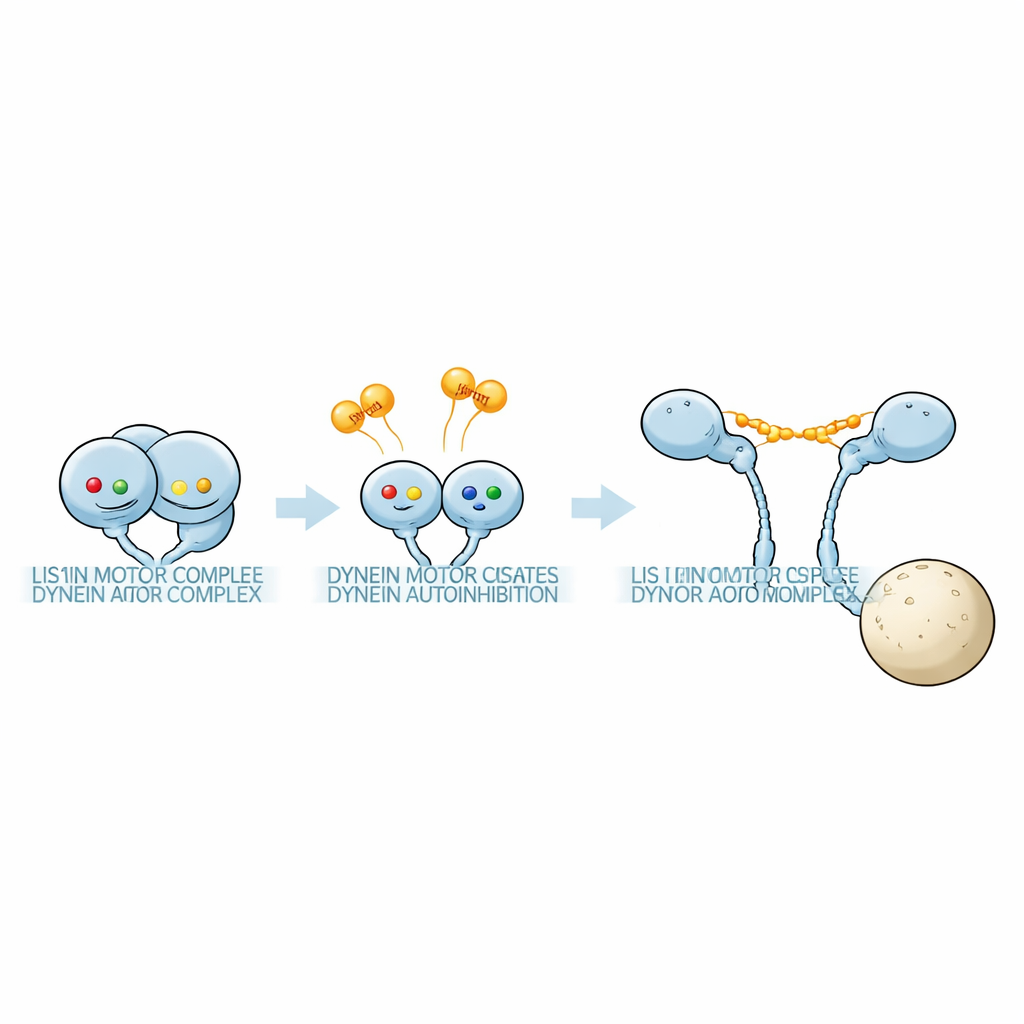
Een verborgen nucleotide “code” ontdekken
Het team gebruikte gevoelige massafotometrie om de massa van eiwitcomplexen te meten in oplossingen met dyneinmotorfragmenten en Pac1 onder verschillende nucleotidecondities. De motorring van dynein draagt drie actieve pockets, AAA1, AAA3 en AAA4. Door precieze mutaties in te voeren die óf nucleotidebinding verhinderen óf ATP-hydrolyse blokkeren in elk pocket, konden de onderzoekers individuele sites in gedefinieerde toestanden vergrendelen. Zij vonden dat de combinatie van nucleotiden in deze drie sites sterk bepaalde hoe strak Pac1 bond en, cruciaal, hoeveel Pac1-eenheden aan elk dynein hechtten. Bij sommige nucleotidecombinaties overbrugde een Pac1-dimeer twee afzonderlijke dyneinmotoren; bij andere raakte het slechts één motor; en in weer andere gevallen bond het nauwelijks. Deze patronen toonden aan dat verschillende nucleotide-"codes" kiezen tussen een 1:1 dynein:Pac1-complex en een 1:2-complex met extra gebonden Pac1.
Hoe Lis1 de motor hervormt
Elektronenmicroscopie koppelde vervolgens bindingsmodus aan vorm. Wanneer Pac1 een 1:1-complex vormde met volledig dynein, schakelden de motoren vrijwel volledig van de phi-conformatie naar een open vorm, waarbij de twee hoofden op een vaste afstand gescheiden waren. Negatiefgekleurd beeldmateriaal toonde Pac1-dimeer die de twee motordomeinen overbrugden, wat overeenkomt met de afstand gezien bij geïsoleerde motor–Pac1-paren. Daarentegen, wanneer de condities een 1:2-complex bevoordeelden, bleef dynein in een phi-achtige ordening: flexibeler en licht vervormd, maar nog steeds compact in plaats van volledig open. Het is dus niet louter de aanwezigheid van Pac1 die telt, maar precies hoeveel Pac1-moleculen binden en waar ze binden.
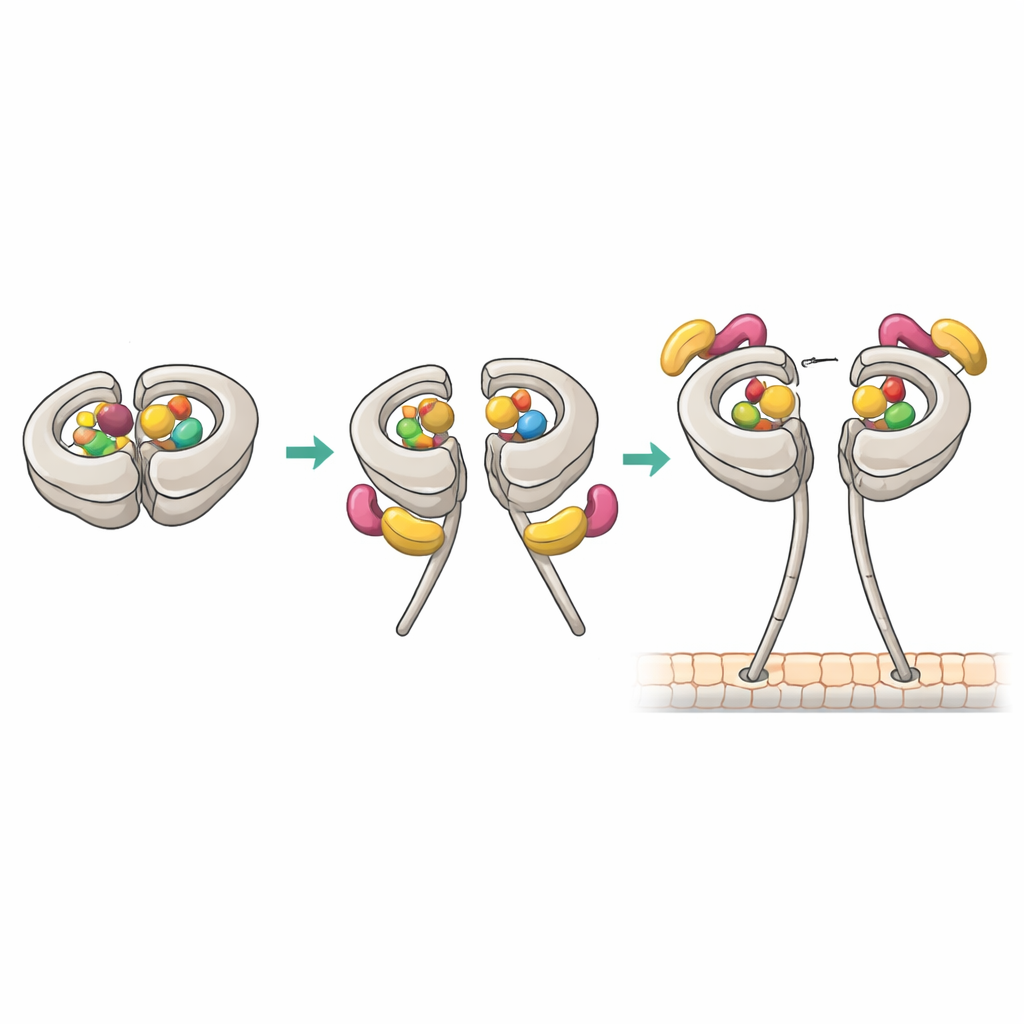
Nieuwe contactpunten die de klem ontgrendelen
Cryo-elektronenmicroscopie op bijna-atomaire resolutie toonde hoe het productieve 1:1-complex is opgebouwd. In die toestand houden het primaire site AAA1 en de regulatorische site AAA4 beide ADP vast, terwijl AAA3 leeg is. Dit nucleotidenpatroon correleert met hoge affiniteit voor Pac1. Eén WD40-"blad" van Pac1 dockt op een eerder bekend punt op de motorring, maar de structuur onthulde ook een tweede contact op de flexibele linkerregio van dynein. Deze dubbele greep stabiliseert een gewijzigde "post-stroke" positie van de linker en duwt Pac1 iets richting de stalk, wat op zijn beurt de binding blokkeert aan een tweede ringgrenzend oppervlak dat anders een andere Pac1-WD40 zou huisvesten. Het muteren van het linkercontact verzwakte Pac1’s vermogen om dynein te openen, verschuiftee de bindingsstoichiometrie en verstoorde dynein-gedreven spilbewegingen in gistcellen, hoewel de basale motoractiviteit intact bleef.
Van biochemische schakelaar naar cellulair transport
Aan de hand van deze resultaten stellen de auteurs een stapsgewijze activatieweg voor. Dynein zit gewoonlijk in phi met ADP in meerdere pockets, wat Pac1 toestaat te binden op een manier die de motor niet opent. Af en toe laat één regulatorisch pocket (AAA3) ADP los, waardoor de linker in een specifieke positie kan zwaaien. Op dat moment kan Pac1 zich vastklemmen aan zowel de ring als de linker van elk motorhoofd, waardoor een enkel Pac1-dimeer de paar hoofden overbrugt en een open conformatie stabiliseert met hoge affiniteit voor microtubuli. Deze open toestand is vervolgens klaargemaakt om aan dynactine en ladingadapters te docken en zo een volledig beweegbare transportmachine te vormen. Zodra dynein een microtubulus aangrijpt en begint te lopen, verzwakt Pac1’s greep en dissocieert het, waarmee de controle wordt overgedragen aan andere regulatoren.
Waarom dit belangrijk is voor gezondheid en ziekte
Voor niet-specialisten is de kernboodschap dat dynein niet simpelweg aan of uit staat; het wordt fijngestemd door een combinatie van nucleotidetoestanden en Lis1-binding die samen een veiligheidssysteem vormen. Alleen wanneer de juiste nucleotidecode verschijnt, fungeert Lis1 als een moleculaire wig die de motor opent en hem in staat stelt zich bij het langeafstandstransportcomplex met dynactine te voegen. Omdat humane Lis1 essentieel is voor hersenontwikkeling en functiestoornissen ervan lissencefalie en andere neurologische aandoeningen veroorzaken, biedt inzicht in deze code op atomair niveau een routekaart voor hoe subtiele veranderingen in Lis1 of dynein cellogistiek kunnen ontregelen en uiteindelijk de ontwikkeling van het organisme kunnen schaden.
Bronvermelding: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Trefwoorden: dyneinemotor, Lis1 Pac1, moleculair transport, eiwitautoinhibitie, cryo-elektronenmicroscopie