Clear Sky Science · sv
En nukleotidkod styr Lis1:s förmåga att lätta på dyneinens autoinhibering
Hur celler håller sina små transportörer under kontroll
Inuti varje cell drar miniatyrmaskiner last längs tunna spår och hjälper till att forma vävnader, dela kromosomer och placera cellkärnan. En av de viktigaste av dessa dragare är motorproteinet dynein. Eftersom dynein är så kraftfullt och så vanligt förekommande måste celler hålla det säkert avstängt tills det behövs. Denna artikel visar hur ett annat protein, Lis1 (i jäst kallat Pac1), läser en subtil ”nukleotidkod” i dynein för att växla det från ett hopfällt, låst tillstånd till en öppen, aktiv form som kan transportera last.
En molekylär motor med en säkerhetslåsning
Dynein är en stor, flerdelad motor som vandrar längs mikrotubuli, cellens interna skenor, och bär vesiklar, RNA och till och med hela kärnor. För att undvika felaktig leverans sitter dynein normalt i en självklämd, autoinhiberad konformation som fått smeknamnet ”phi”-partikeln, där dess två motorhuvuden viks ihop och knappt interagerar med mikrotubuli. För långtidsförflyttningar måste dynein först vecklas ut och sedan kombinera med ett annat komplex, dynactin, plus en lastadapter. Tidigare arbete antydde att Lis1 hjälper till att låsa upp dynein, men detaljerna var oklara, delvis därför att dyneinens motor innehåller flera nukleotidbindande fickor som var och en kan bära olika former av ATP eller ADP. Författarna försökte avkoda hur dessa fickor, och Lis1-bindning, samverkar för att styra dyneinens form.
Att upptäcka en dold nukleotid”kod”
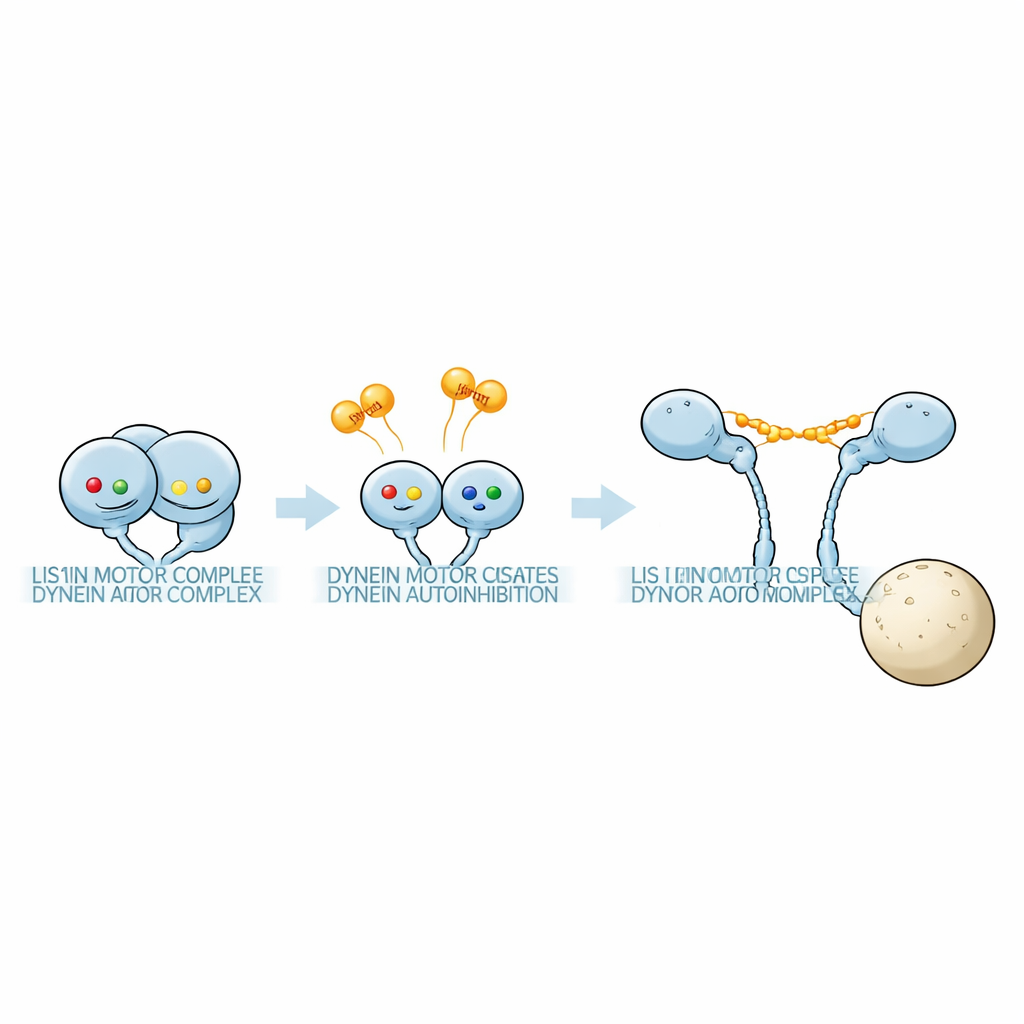
Gruppen använde känslig massfotometri för att väga proteinkomplex i lösningar som innehöll dyneinmotorfragment och Pac1 under många nukleotidförhållanden. Dyneinens motorring rymmer tre aktiva fickor, AAA1, AAA3 och AAA4. Genom att införa precisa mutationer som antingen förhindrar nukleotidbindning eller blockerar ATP-hydrolys i varje ficka kunde forskarna låsa individuella platser i definierade tillstånd. De fann att kombinationen av nukleotider i dessa tre platser starkt påverkade hur tätt Pac1 bundet och, avgörande, hur många Pac1-enheter som fäste vid varje dynein. I vissa nukleotidkombinationer länkade en Pac1-dimer ihop två separata dynein-motorer; i andra kontaktade den bara en motor; och i ytterligare andra band den knappt alls. Dessa mönster visade att distinkta nukleotid”koder” väljer mellan ett 1:1 dynein:Pac1-komplex och ett 1:2-komplex med extra Pac1 bundet.
Hur Lis1 omformar motorn
Elektronmikroskopi kopplade sedan bindningsläge till form. När Pac1 bildade ett 1:1-komplex med fullängdsdynein skiftade motorerna nästan fullständigt från phi-konformationen till en öppen form, med de två huvudena separerade i ett fast avstånd. Negativfärgade bilder visade Pac1-dimerer som länkade de två motordomänerna, vilket matchade den avståndsbild som setts med isolerade motor–Pac1-par. I kontrast, när förhållandena gynnade ett 1:2-komplex förblev dynein i en phi-liknande arrangemang: mer flexibel och något förvriden, men fortfarande kompakt snarare än fullt öppen. Alltså är det inte bara närvaron av Pac1 som spelar roll, utan exakt hur många Pac1-molekyler som binder och var de binder.
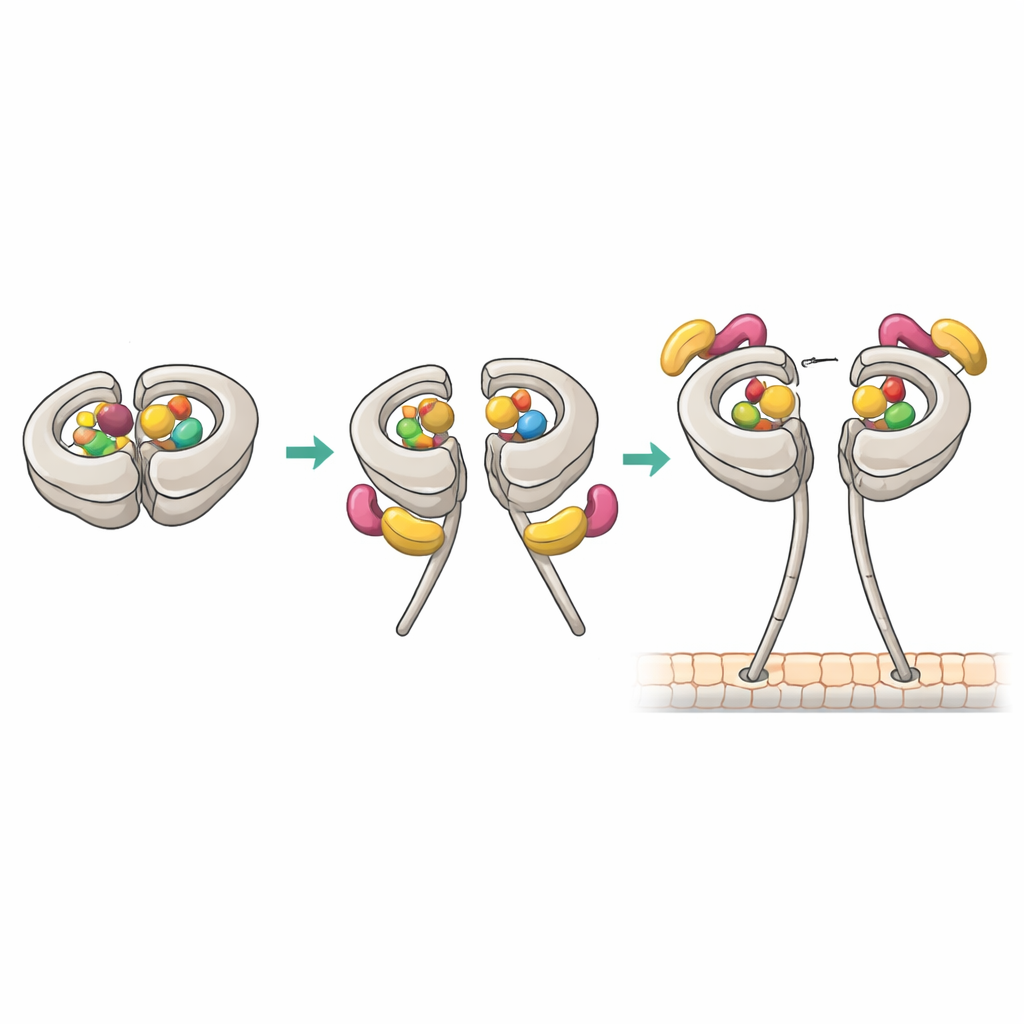
Nya kontaktpunkter som låser upp klämman
Kryo-elektronmikroskopi vid nästan atomupplösning avslöjade hur det produktiva 1:1-komplexet byggs upp. I detta tillstånd håller dyneinens primära site AAA1 och en regulatorisk site AAA4 båda ADP, medan AAA3 är tom. Detta nukleotidmönster korrelerar med hög affinitet för Pac1. En WD40 ”blad” av Pac1 dockar vid en tidigare känd plats på motorringen, men strukturen avslöjade också en andra kontakt på dyneinens flexibla länkregion. Dessa dubbla grepppunkter stabiliserar en modifierad ”post-stroke”-position av länken och skjuter Pac1 något mot stammen, vilket i sin tur blockerar bindning vid en andra ringadjacent plats som annars skulle hysa ytterligare en Pac1 WD40. Mutation av länkens kontakt försvagade Pac1:s förmåga att öppna dynein, förändrade bindningsstoikiometrin och försämrade dynein-drivna spindelrörelser i jästceller, även om den grundläggande motorns aktivitet förblev intakt.
Från biokemisk brytare till cellulär rörelse
Genom att pussla ihop dessa resultat föreslår författarna en stegvis aktiveringsväg. Dynein sitter typiskt i phi med ADP i flera fickor, vilket tillåter Pac1 att binda på ett sätt som inte öppnar motorn. Ibland släpper en regulatorisk ficka (AAA3) ADP, vilket låter länken svänga in i en särskild position. Vid det ögonblicket kan Pac1 klämma fast både vid ringen och länken på varje motorhuvud, skapa en enda Pac1-dimer som förbinder paren av huvudena och stabiliserar en öppen konformation med hög affinitet för mikrotubuli. Detta öppna tillstånd är sedan förberett för dockning på dynactin och lastadapterar för att bilda en fullt rörlig transportmaskin. När dynein väl engagerar en mikrotubuli och börjar gå försvagas Pac1:s grepp och det dissocierar, vilket överlämnar kontrollen till andra regulatorer.
Varför detta spelar roll för hälsa och sjukdom
För en icke-specialist är huvudbudskapet att dynein inte bara slås på eller av; det ställs in av en kombination av nukleotidstatus och Lis1-bindning som tillsammans bildar en säkerhetslogik. Först när rätt nukleotidkod uppträder fungerar Lis1 som en molekylär kil, öppnar motorn och möjliggör att den kan gå med i långdistanstransportteamet tillsammans med dynactin. Eftersom mänskligt Lis1 är avgörande för hjärnans utveckling och dess fel fungerar orsakar lissencefali och andra neurologiska störningar, ger förståelsen av denna kod i atomär detalj en vägkarta för hur subtila förändringar i Lis1 eller dynein kan sabotera cellulär logistik och i förlängningen organismens utveckling.
Citering: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Nyckelord: dyneinmotor, Lis1 Pac1, molekylär transport, proteinautoinhibering, kryoelektronmikroskopi