Clear Sky Science · pt
Um código de nucleotídeo governa a capacidade da Lis1 de aliviar a autoinibição da dineína
Como as células mantêm seus pequenos transportadores sob controle
Dentro de cada célula, máquinas em miniatura puxam cargas ao longo de trilhos delgados, ajudando a moldar tecidos, a dividir cromossomos e a posicionar o núcleo. Um dos mais importantes desses transportadores é uma proteína motora chamada dineína. Porque a dineína é tão poderosa e tão amplamente utilizada, as células precisam mantê‑la seguramente desligada até que seja necessária. Este artigo revela como outra proteína, Lis1 (chamada Pac1 em leveduras), lê um sutil “código de nucleotídeo” na dineína para alterá‑la de um estado dobrado e travado para uma forma aberta e ativa capaz de mover cargas.
Um motor molecular com um trava de segurança
A dineína é um grande motor multipartes que caminha ao longo dos microtúbulos, os trilhos internos da célula, carregando vesículas, RNA e até núcleos inteiros. Para evitar entregas equivocadas, a dineína normalmente permanece em uma conformação autoinibida e autoengatada apelidada de partícula “fi” (phi), na qual suas duas cabeças motoras se dobram uma sobre a outra e quase não interagem com os microtúbulos. Para percursos de longa distância, a dineína deve primeiro desdobrar‑se e então combinar‑se com outro complexo, a dinactina, além de um adaptador de carga. Trabalhos anteriores sugeriam que a Lis1 ajuda a destravar a dineína, mas os detalhes eram obscuros, em parte porque o motor da dineína contém vários bolsos de ligação de nucleotídeos que podem conter diferentes formas de ATP ou ADP. Os autores buscaram decodificar como esses bolsos, e a ligação de Lis1, atuam em conjunto para controlar a forma da dineína.
Descobrindo um “código” de nucleotídeo oculto
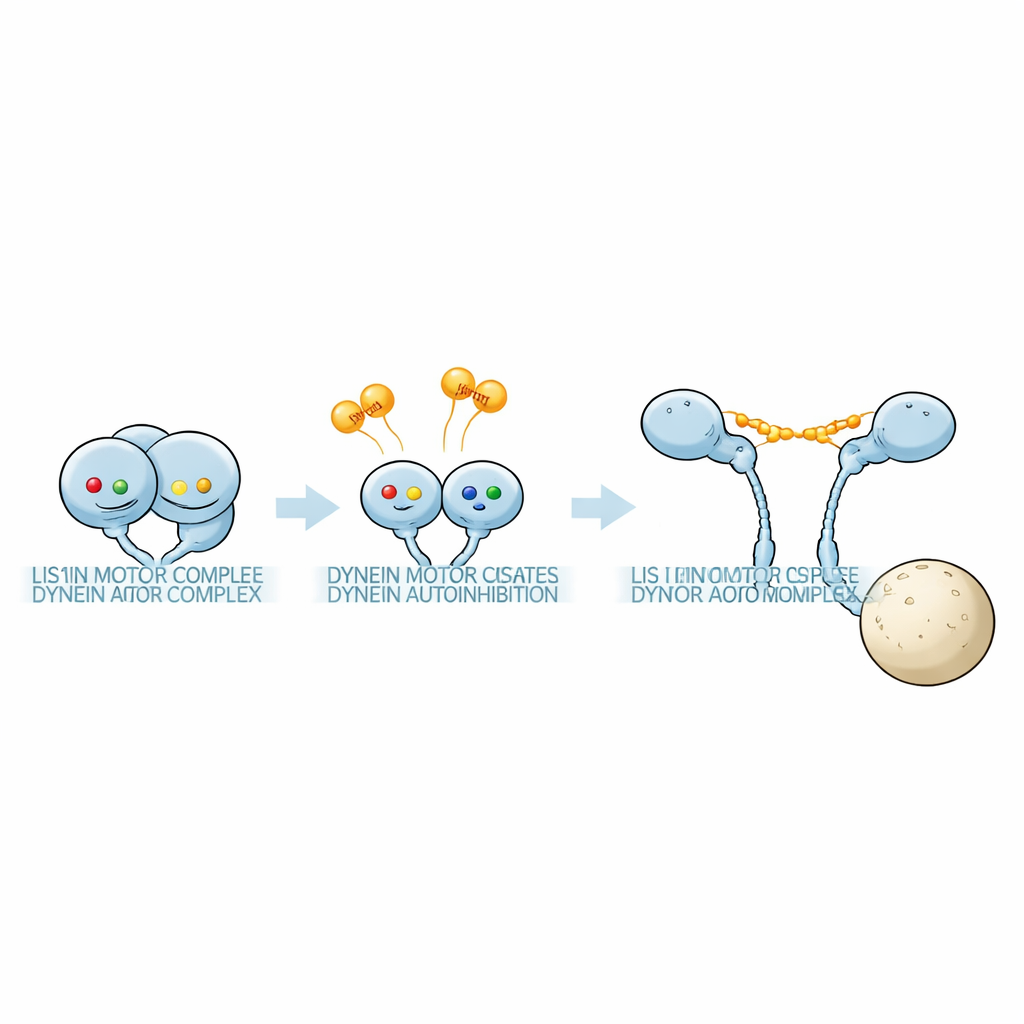
A equipe usou fotometria de massa sensível para pesar complexos proteicos em soluções contendo fragmentos do motor da dineína e Pac1 sob várias condições de nucleotídeos. O anel motor da dineína carrega três bolsos ativos, AAA1, AAA3 e AAA4. Ao introduzir mutações precisas que impediam a ligação de nucleotídeos ou bloqueavam a hidrólise de ATP em cada bolso, os pesquisadores puderam travar sítios individuais em estados definidos. Eles descobriram que a combinação de nucleotídeos nesses três sítios influenciava fortemente quão firmemente o Pac1 se ligava e, crucialmente, quantas unidades de Pac1 se ligavam a cada dineína. Em algumas combinações de nucleotídeos, um dímero de Pac1 fazia a ponte entre duas dineínas separadas; em outras, ele contatava apenas um motor; e em outras ainda, mal se ligava. Esses padrões revelaram que “códigos” de nucleotídeo distintos selecionam entre um complexo 1:1 dineína:Pac1 e um complexo 1:2 com Pac1 extra ligado.
Como a Lis1 remodela o motor
A microscopia eletrônica então relacionou o modo de ligação à conformação. Quando o Pac1 formava um complexo 1:1 com dineína de comprimento total, os motores praticamente mudavam da conformação fi para uma forma aberta, com as duas cabeças separadas a uma distância fixa. Imagens com coloração negativa mostraram dímeros de Pac1 fazendo a ponte entre os dois domínios motores, correspondendo ao espaçamento visto em pares isolados motor–Pac1. Em contraste, quando as condições favoreciam um complexo 1:2, a dineína permanecia em um arranjo semelhante ao fi: mais flexível e ligeiramente distorcida, mas ainda compacta em vez de totalmente aberta. Assim, não é simplesmente a presença de Pac1 que importa, e sim exatamente quantas moléculas de Pac1 se ligam e onde.
Novos pontos de contato que destravam a trava
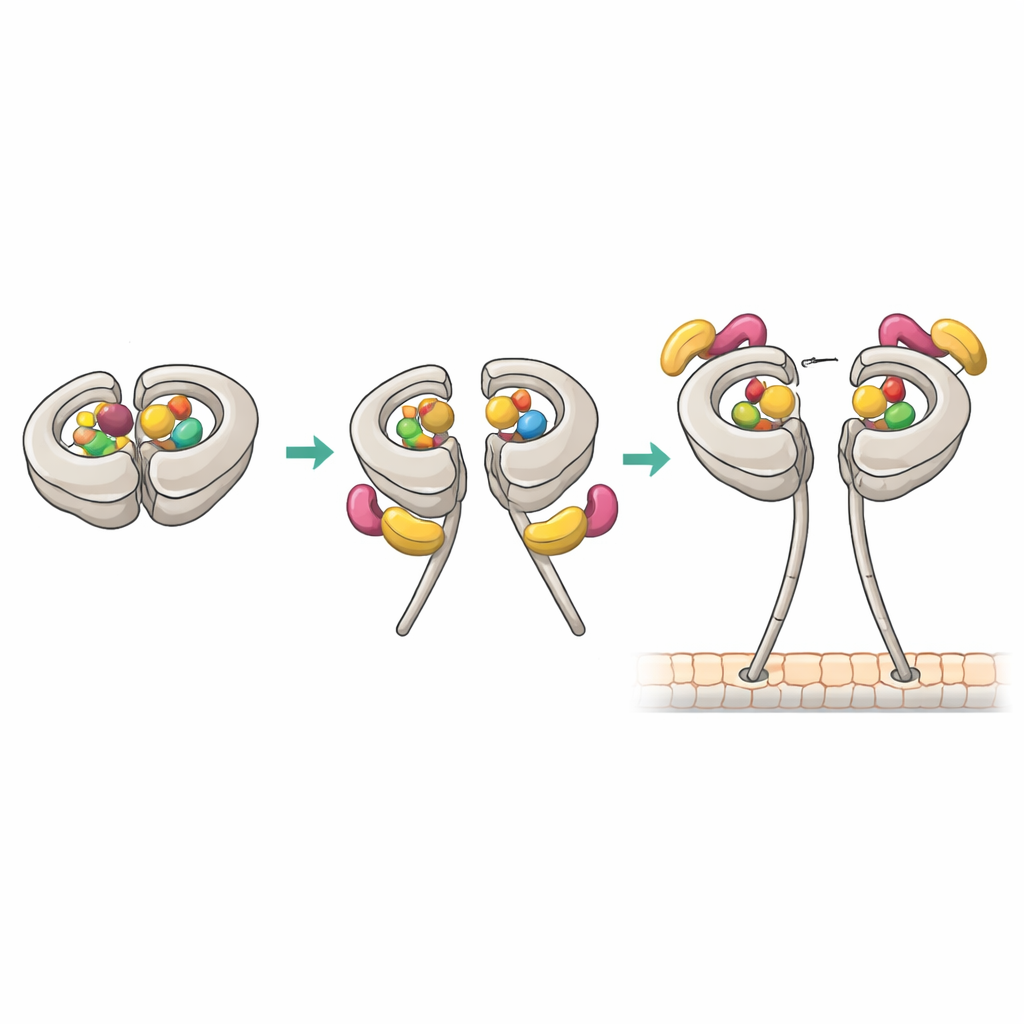
A criomicroscopia eletrônica em resolução quase atômica revelou como o complexo produtivo 1:1 é montado. Nesse estado, o sítio primário da dineína AAA1 e um sítio regulatório AAA4 ambos contêm ADP, enquanto o AAA3 está vazio. Esse padrão de nucleotídeos correlaciona‑se com alta afinidade pelo Pac1. Uma “lâmina” WD40 do Pac1 encaixa‑se em um sítio previamente conhecido no anel motor, mas a estrutura também revelou um segundo contato na região flexível do linker da dineína. Esses pontos de fixação duplos estabilizam uma posição modificada de “pós‑golpe” do linker e empurram o Pac1 ligeiramente em direção ao stalk, o que por sua vez bloqueia a ligação em um segundo sítio adjacente ao anel que de outra forma hospedaria outro WD40 de Pac1. Mutar o contato do linker enfraqueceu a capacidade do Pac1 de abrir a dineína, deslocou a estequiometria de ligação e prejudicou os movimentos do fuso dirigidos pela dineína em células de levedura, mesmo que a atividade motora básica permanecesse intacta.
Do interruptor bioquímico ao movimento celular
Reunindo esses resultados, os autores propõem uma via de ativação em etapas. A dineína tipicamente repousa em fi com ADP em vários bolsos, o que permite que o Pac1 se ligue de uma forma que não abre o motor. Ocasionalmente, um bolso regulatório (AAA3) libera ADP, permitindo que o linker oscile para uma posição particular. Nesse momento, o Pac1 pode prender‑se tanto ao anel quanto ao linker de cada cabeça motora, criando um dímero único de Pac1 que faz a ponte entre o par de cabeças e estabiliza uma conformação aberta com alta afinidade pelos microtúbulos. Esse estado aberto fica então pronto para acoplar‑se à dinactina e aos adaptadores de carga para formar uma máquina de transporte totalmente móvel. Uma vez que a dineína engage um microtúbulo e comece a caminhar, a aderência do Pac1 enfraquece e ele se dissocia, transferindo o controle para outros reguladores.
Por que isso importa para a saúde e a doença
Para um público não especializado, a mensagem-chave é que a dineína não está simplesmente ligada ou desligada; ela é ajustada por uma combinação de estados de nucleotídeos e da ligação de Lis1 que, em conjunto, formam uma lógica de segurança. Somente quando o código de nucleotídeo correto aparece é que a Lis1 atua como uma cunha molecular, abrindo o motor e permitindo que ele se junte à equipe de transporte de longa distância com a dinactina. Como a Lis1 humana é essencial para o desenvolvimento do cérebro e seu mau funcionamento causa lissencefalia e outros distúrbios neurológicos, entender esse código em detalhe atômico oferece um mapa de como mudanças sutis na Lis1 ou na dineína podem desviar a logística celular e, por fim, o desenvolvimento do organismo.
Citação: Geohring, I.C., Chai, P., Iyer, B.R. et al. A nucleotide code governs Lis1’s ability to relieve dynein autoinhibition. Nat Chem Biol 22, 649–662 (2026). https://doi.org/10.1038/s41589-025-02096-8
Palavras-chave: motor de dineína, Lis1 Pac1, transporte molecular, autoinibição de proteína, crio microscopia eletrônica