Clear Sky Science · tr
Damla mikroakışkanları kullanarak faj-konak dinamiklerini nicelleştirme
Neden küçük virüsler ve damlacıklar bizim için önemli
Bakterileri öldüren virüsler, yani bakteriyofajlar, ilaç direnci gösteren enfeksiyonlara karşı potansiyel müttefikler olarak yeniden değerlendiriliyor. Ancak bunları güvenilir ilaçlara dönüştürebilmek için, bilim insanlarının tek tek virüslerin bakterileri ne kadar etkin şekilde enfekte edip yok ettiğini ölçmesi gerekiyor; klasik laboratuvar yöntemleri bunu başarmakta zorlanıyor. Bu makale, binlerce küçük mücadeleyi aynı anda izleyen damla tabanlı bir yaklaşım sunuyor: tek virüs ile tek bakteri arasındaki savaşları gözlemleyerek enfeksiyonların ne kadar hızlı ve ne sıklıkla başarıya ulaştığını ortaya koyuyor. Bu düzeyde hassas bilgi, daha iyi faj terapilerine rehberlik edebilir ve dünyadaki mikrobiyal yaşamı şekillendiren gizli viral dünyayı daha derinlemesine anlamamıza yardımcı olabilir.
Geleneksel petri kabı testlerinin sınırları
On yıllardır araştırmacılar plak testi adı verilen yönteme dayanıyor: virüsleri yumuşak agar içindeki bakteri tabakasıyla karıştırın, bir gece bekleyin ve sonra bakterilerin yok olduğu temiz noktaları sayın. Bu lekeler, mevcut enfektif virüs sayısını tahmin eder. Dayanıklı olmakla birlikte, bu yöntem yavaştır, esnek değildir ve yalnızca nihai bir anlık görüntü sunar. Enfeksiyonların zaman içinde nasıl geliştiğini izleyemez ve sayısız enfeksiyon ve yeniden enfeksiyon turunu birbirine karıştırır. Toplu floresan veya DNA tabanlı testler gibi diğer yaklaşımlar da büyük popülasyonlar üzerinde ortalama alır; bu da tek bir enfeksiyon olayını görmek veya her bir bakteriye kaç virüs düştüğünü gibi koşulları ayarlamakta zorluk çıkarır.
Her enfeksiyonu küçük bir deney tüpüne dönüştürmek
Yazarlar, bakterileri ve fajları yağ içinde süspansiyon halinde mikroskobik su damlacıklarına paketleyen yüksek verimli bir platform kuruyor. Bakteri taşıyan bir akış ile virüs taşıyan başka bir akış—iki ayrı sıvı akımı—damlacıkların oluştuğu dar kavşakta buluşur; böylece maruz kalma süresi kapsülleme anında kesin olarak başlar. Her damlacık, iyi tanımlanmış hacimli ve kontrollü bir faj‑bakteri oranına sahip izole bir reaksiyon odacığı haline gelir. Ekip, hücre parçalanmasından sonra bakteriyel DNA açığa çıktığında güçlü şekilde ışıldayan özel bir floresan boya ekler; bu, yalnızca viral genetik materyalin varlığından ziyade başarılı lizisin doğrudan okumalarını sağlar.
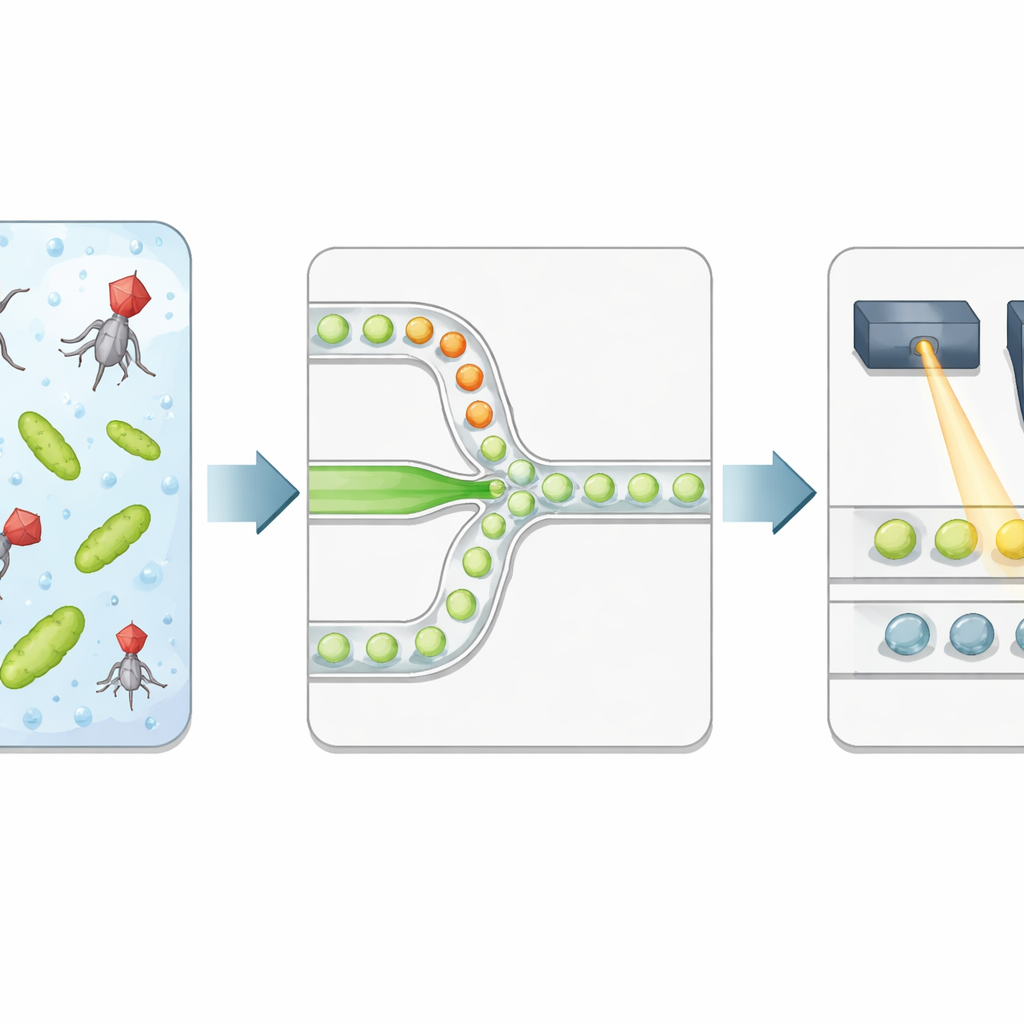
Damlacık sonuçlarını ışıkla okuma
Kontrollü bir inkübasyonun ardından emülsiyon, damlacıkları odaklanmış bir lazerin altına tek tek hizalayan ikinci bir mikroakışkan çipten geçirilir. Hızlı bir detektör, DNA boyasından gelen yeşil floresanı ve damla üretimi sırasında eklenen referans boyadan gelen kırmızı floresanı kaydeder. Kırmızı sinyal damlacık boyutunu ve her damlacığın ne kadar virüs çözeltisi aldığı hakkında bilgi verirken, yeşil sinyal lizisin olup olmadığını bildirir. Otomatik bir istatistiksel yöntem, loş damlacıkları (lizis yok) parlak damlacıklardan (en az bir enfekte olmuş ve lizis olmuş bakteri) ayırarak deneyi dijital 0 ve 1 dizisine çevirir. Parlak damlacıkların kesrini, damlacık başına beklenen virüs ve bakteri sayılarıyla ilişkilendirerek araştırmacılar virüs konsantrasyonunu yeniden elde eder ve bunu klasik plak sayımlarıyla karşılaştırır.
Koşulları ayarlamak ve gizli kinetikleri araştırmak
Platform basit sayımın ötesine geçer. Virüs ve bakteri çözeltilerinin karışım oranını kasıtlı olarak değiştirerek ekip, tek bir deney içinde farklı virüs‑konak oranlarına sahip alt popülasyonlar oluşturur. Bu, analizinin hassas sonuç verdiği konsantrasyon aralığını etkili şekilde genişletir ve toplu optik ölçümlerde görülen tüm bakterilerin gerçekte enfekte edilebilir olmadığını bile açığa çıkarır. Yazarlar ayrıca damlacık boyutunu ve inkübasyon süresini değiştirerek lizis olmuş damlacıkların payının nasıl arttığını izler. Damlacık içindeki bakterilere virüslerin adsorpsiyonunu modelleyen yaklaşımları, lizisin zamanlaması ve başarısının enfeksiyon yapabilen gerçek hücre sayısına ve virüs parçacıklarının onlarla ne sıklıkla çarpıştığına bağlı olduğunu, ancak damlacık hacminin kendisine çok güçlü bir şekilde bağlı olmadığını gösterir.
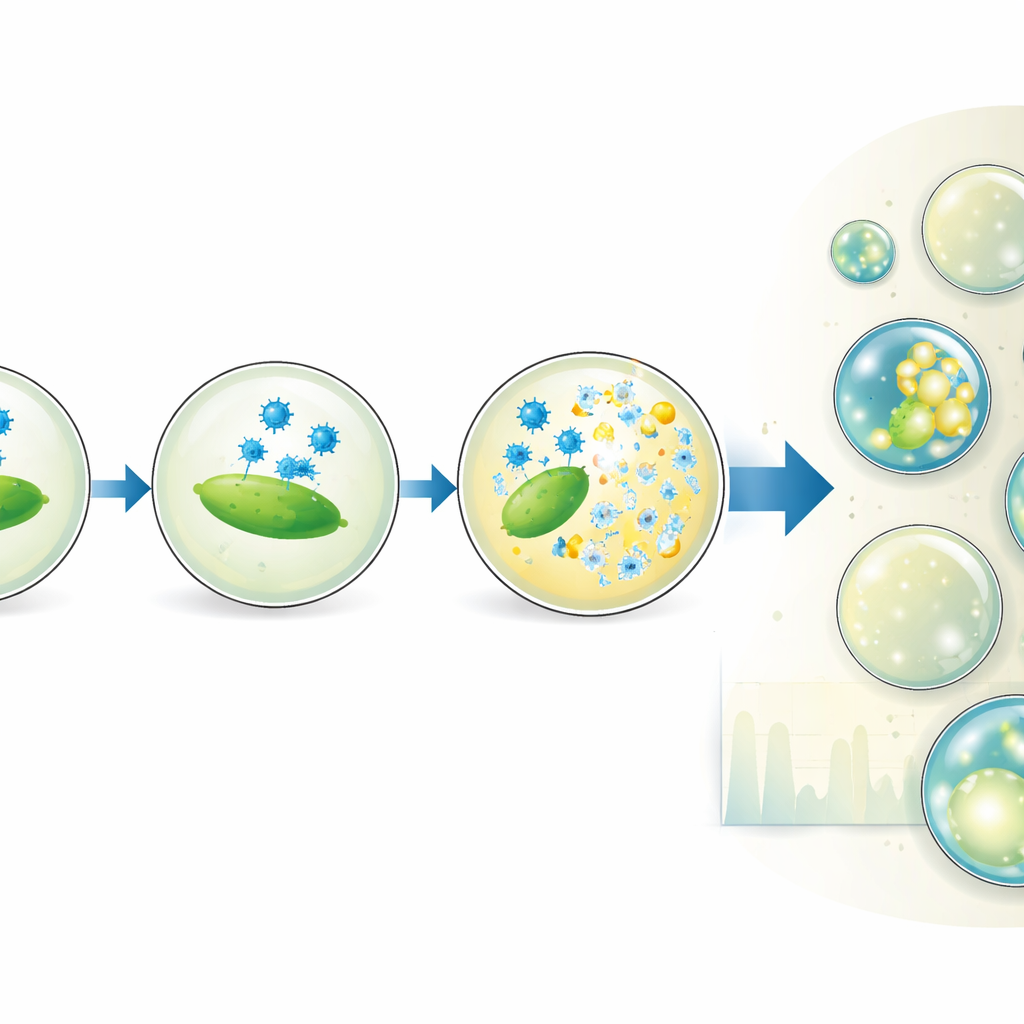
Laboratuvar aracından gelecekteki terapilere
Bireysel enfeksiyon olaylarını izole edip dijitalleştirerek, bu damla yöntemi geleneksel plak testleriyle yakından eşleşen doğru virüs sayımları sunar; buna ek olarak zaman çözünürlüklü bilgi ve deney koşulları üzerinde ince kontrol sağlar. Birçok farklı lizojenik olmayan faj–bakteri eşine uygulanabilir ve milyonlarca damla ölçeğine çıkarılabilir; bu da faj varyantlarının, ortamların veya sıcaklıkların yüksek verimli taramasına kapı açar. Pratik açıdan bu çalışma, terapötik fajların hedeflerini ne kadar iyi enfekte ettiğini karakterize etmenin güçlü yeni bir yolunu sağlar; bu, doğal bakteriyal yırtıcıları antibiyotiğe dirençli enfeksiyonlarla mücadelede kullanma yönündeki önemli bir adımdır.
Atıf: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Anahtar kelimeler: bakteriyofajlar, mikroakışkan damlacıklar, faj tedavisi, tek hücre enfeksiyonu, antibiyotik direnci