Clear Sky Science · he
כימות דינמיקות פאג‑מארח באמצעות מיקרו‑נוזליות בטיפות
למה וירוסים זעירים וטיפות חשובים לנו
וירוסים ההורגים חיידקים, המכונים בקטריופאגים, זוכים להתעניינות מחודשת כעמיתים פוטנציאליים במאבק בזיהומים עמידים לתרופות. אך כדי להפוך אותם לתרופות מהימנות, על המדענים למדוד כמה ביעילות כל וירוס יחיד מדביק והורס חיידקים — דבר ששיטות מעבדה קלאסיות מתקשות לבצע. מאמר זה מציג שיטה מבוססת טיפות שעוקבת בו‑זמנית אחרי אלפי קרבות מיקרוסקופיים בין וירוס יחיד לחיידק, וחושפת כמה מהר וכמה לעיתים נדירות ההדבקות מצליחות. תובנות מדויקות כאלה יכולות להנחות תרפיות פאג טובות יותר ולהעמיק את הבנתנו על העולם הויראלי הנסתר שעושה עיצוב לחיי המיקרובים על פני כדור הארץ.
מגבלות בדיקות פטרי‑דיש מסורתיות
עשרות שנים חוקרים נשענים על מבחני פלאק: מערבבים וירוסים עם שטח חיידקי בג'ל רך, מחכים למשך הלילה ואז סופרים נקודות בהירות שבהן החיידקים נמחקו. נקודות אלו מעריכות כמה וירוסים מדבקים היו נוכחים. למרות שזו שיטה מוצקה, היא איטית, לא גמישה ומספקת רק תמונת מצב סופית. היא אינה יכולה לעקוב אחר התפתחות ההדבקה בזמן, ומערבבת יחד סבבים רבים של הדבקה והדבקה חוזרת. גישות אחרות, כמו פלורוסנציה במאקרו או בדיקות מבוססות DNA, עדיין ממוצעות על אוכלוסיות ענק, מה שהופך קשה לראות אירועי הדבקה בודדים או לכוונן תנאים כגון כמה וירוסים פוגשים כל חיידק.
להפוך כל הדבקה לצינור מבחנה זעיר
המחברים בונים פלטפורמה בריבוי גבוה שמארזת חיידקים ופאגים לטיפות מים מיקרוסקופיות התלויות בשמן. שתי זרמי נוזל נפרדים — אחד נושא חיידקים והשני וירוסים — נפגשים רק בצומת הצר שבו נוצרות הטיפות, כך שזמן החשיפה מתחיל בדיוק ברגע הסגירה. כל טיפה הופכת לתא תגובה מבודד בנפח מוגדר וביחס פאג‑לחיידק מבוקר. הצוות מוסיף צבע פלורסנטי מיוחד שמתמגנט בעוצמה כאשר DNA חיידקי משתחרר לאחר שהתא מתפרק, ומשמש כתוצאה ישירה של ליזיס מוצלח ולא רק כנוכחות חומר גנטי ויראלי.
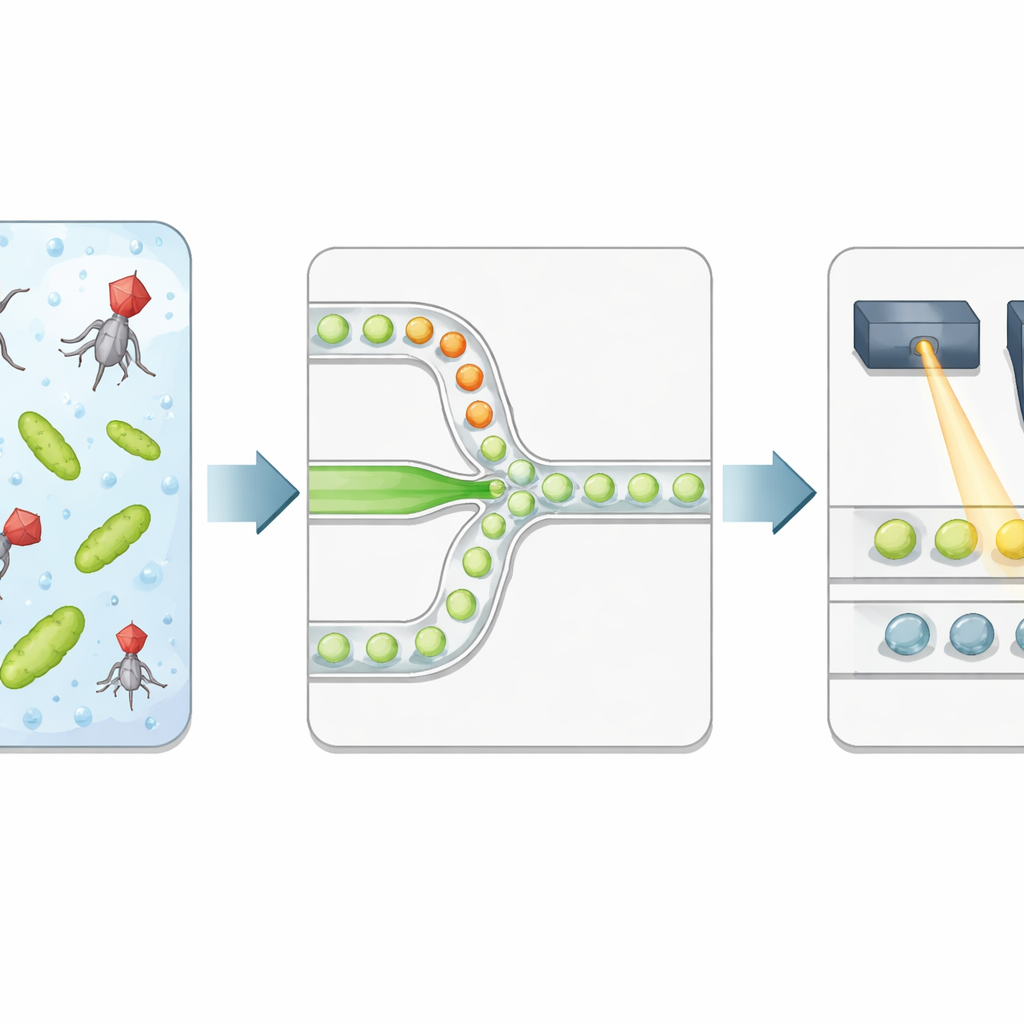
קריאת תוצאות הטיפות באמצעות אור
לאחר דגירה מבוקרת, האמולסיה מונחת דרך שבב מיקרו‑נוזליות שני שמסדרת את הטיפות אחת אחרי השנייה תחת לייזר ממוקד. גלאי מהיר רושם פלורוסנציה ירוקה מהצבע של ה‑DNA ופלורוסנציה אדומה מצבע ייחוס שנוסף בעת יצירת הטיפות. האות האדום מציין את גודל הטיפה וכמה מתמיסת הוירוס כל טיפה קיבלה, בעוד האות הירוק מדווח אם התרחש ליזיס. שיטה סטטיסטית אוטומטית מפרידה טיפות כהות (ללא ליזיס) מטיפות בוהקות (לפחות חיידק אחד נדבק והליזיס התרחש), והופכת את הניסוי למחרוזת דיגיטלית של 0ים ו‑1ים. על ידי קישור החלק של הטיפות הבוהקות למספר הצפוי של וירוסים וחיידקים לכל טיפה, החוקרים משחזרים את ריכוז הוירוס ומשווים אותו למספרי פלאק קלאסיים.
כוונון תנאים וחקר קינטיקה נסתרת
הפלטפורמה חורגת מעבר לספירה פשוטה. על‑ידי שינוי מכוון של יחס התערובת בין תמיסת הוירוס לזו של החיידק, הצוות מייצר תת‑אוכלוסיות של טיפות עם יחסים שונים של וירוס‑אל‑מארח, הכל בתוך ניסוי יחיד. הדבר מרחיב בפועל את טווח הריכוזים שבו המבחן נותן תוצאות מדויקות ואף מגלה שלא כל החיידקים הנראים במדידות אופטיות גורפות אכן ניתנים להדבקה. המחברים גם משנים את גודל הטיפות ואת זמן הדגירה כדי לצפות כיצד חלק הטיפות הליזיות גדל. המודל שלהם לאופן שבו וירוסים נספגים לחיידקים בתוך טיפות מראה שזמן והצלחת הליזיס תלוים במספר האמיתי של תאים בעלי יכולת הדבקה ובתדירות שבה חלקיקי וירוס מתנגשים בהם, אך לא בהשפעה חזקה של נפח הטיפה עצמו.
מכלי מעבדה לכלים טיפוליים עתידיים
על‑ידי הבידוד והדיגיטיזציה של אירועי הדבקה בודדים, שיטת הטיפות הזו מספקת ספירות וירוס מדויקות התואמות במידה רבה למבחני פלאק מסורתיים, ובו‑בזמן מוסיפה מידע תלוי‑זמן ושליטה עדינה בתנאי הניסוי. ניתן להחיל אותה על זוגות פאג‑חיידק ליזיים שונים ולהרחיבה למיליוני טיפות, ופתיחת הדלת למסננות בריבוי גבוה של וריאנטים של פאגים, מדיומים או טמפרטורות. במונחים מעשיים, העבודה מספקת דרך חדשה חזקה לתאר כמה טוב פאגים טיפוליים מדביקים את מטרותיהם — צעד חשוב בדרך לשימוש בטורפים החיידקיים הטבעיים הללו במאבק בזיהומים עמידים לאנטיביוטיקה.
ציטוט: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
מילות מפתח: בקטריופאגים, טיפות מיקרו‑נוזליות, תרפיית פאגים, זיהום תא‑יחיד, עמידות אנטיביוטית