Clear Sky Science · fr
Quantification des dynamiques phage‑hôte par microfluidique en gouttelettes
Pourquoi les petits virus et les gouttelettes nous concernent
Les virus qui tuent les bactéries, appelés bactériophages, sont réexaminés comme alliés potentiels contre les infections résistantes aux médicaments. Mais pour les transformer en traitements fiables, les scientifiques doivent mesurer à quel point des virus individuels infectent et détruisent des bactéries — une chose que les méthodes de laboratoire classiques peinent à accomplir. Cet article présente une approche basée sur des gouttelettes qui observe des milliers de mini‑batailles entre virus uniques et bactéries simultanément, révélant la vitesse et la fréquence auxquelles les infections réussissent. De tels renseignements précis pourraient orienter de meilleures thérapies phagiques et approfondir notre compréhension du monde viral caché qui façonne la vie microbienne sur Terre.
Limites des tests traditionnels en boîte de Pétri
Pendant des décennies, les chercheurs ont utilisé les essais de plaques : mélanger des virus avec un tapis bactérien dans de l’agar mou, attendre une nuit, puis compter les zones claires où les bactéries ont été éliminées. Ces zones estiment le nombre de virus infectieux présents. Bien que robuste, cette méthode est lente, peu souple et n’offre qu’un instantané final. Elle ne peut pas suivre le déroulement des infections dans le temps et mélange de multiples cycles d’infection et de réinfection. D’autres approches, comme la fluorescence en masse ou les tests basés sur l’ADN, moyennent encore sur d’immenses populations, rendant difficile la détection d’événements d’infection uniques ou l’ajustement de conditions telles que le nombre de virus par bactérie.
Transformer chaque infection en un petit tube à essai
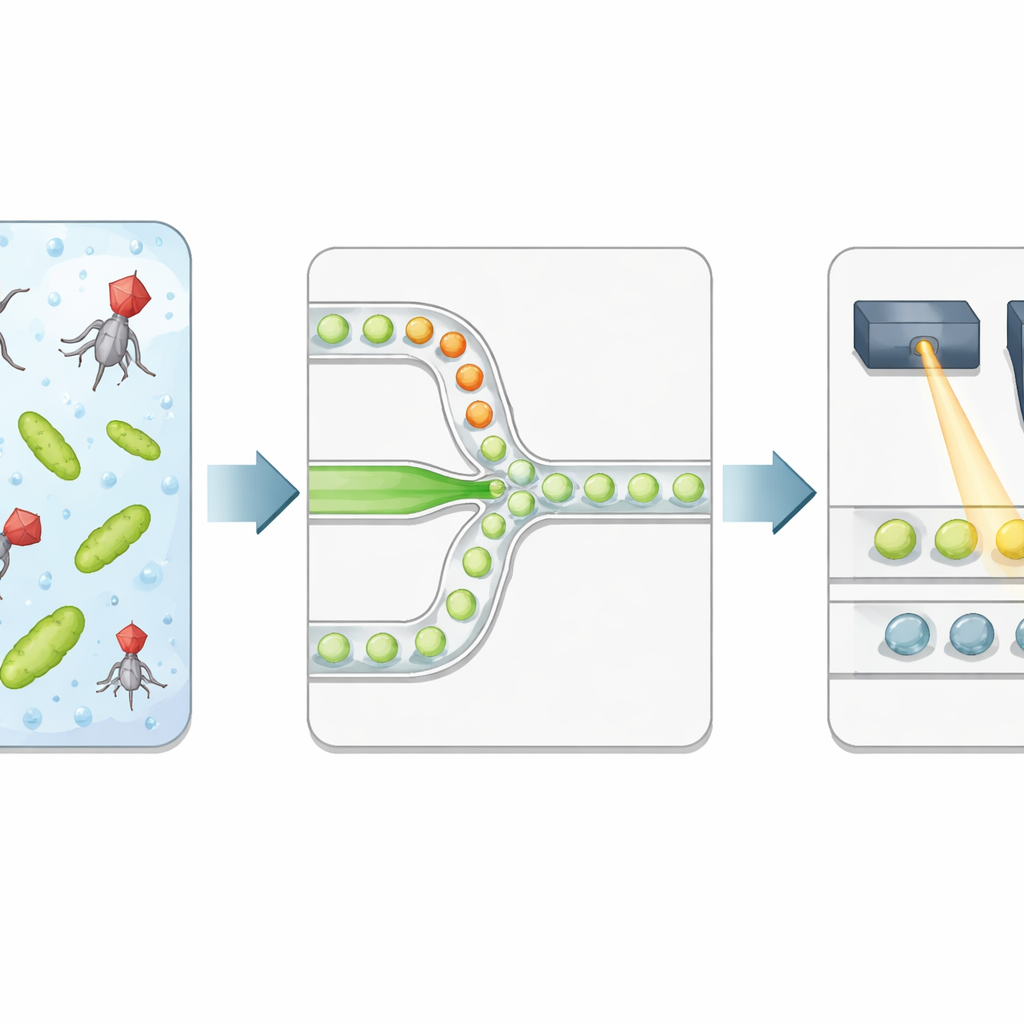
Les auteurs construisent une plate‑forme à haut débit qui enferme bactéries et phages dans des gouttelettes microscopiques d’eau en suspension dans l’huile. Deux flux liquides séparés — l’un transportant les bactéries, l’autre les virus — se rejoignent uniquement au niveau de l’étroite jonction où se forment les gouttelettes, de sorte que le temps d’exposition commence précisément à l’encapsulation. Chaque gouttelette devient une chambre de réaction isolée avec un volume bien défini et un rapport phages/bactéries contrôlé. L’équipe ajoute un colorant fluorescent particulier qui s’allume fortement lorsque l’ADN bactérien est libéré après l’éclatement de la cellule, servant de lecture directe de la lyse réussie plutôt que de la seule présence de matériel génétique viral.
Lire les résultats des gouttelettes avec la lumière
Après une incubation contrôlée, l’émulsion est acheminée à travers une seconde puce microfluidique qui aligne les gouttelettes une par une sous un laser focalisé. Un détecteur rapide enregistre la fluorescence verte du colorant de l’ADN et la fluorescence rouge d’un colorant de référence inclus lors de la production des gouttelettes. Le signal rouge renseigne sur la taille de la gouttelette et sur la quantité de solution virale reçue par chacune, tandis que le signal vert indique si une lyse a eu lieu. Une méthode statistique automatisée sépare les gouttelettes peu lumineuses (pas de lyse) des gouttelettes brillantes (au moins une bactérie infectée et lysée), convertissant l’expérience en une chaîne de 0 et 1 numériques. En reliant la fraction de gouttelettes brillantes au nombre attendu de virus et de bactéries par gouttelette, les chercheurs reconstituent la concentration virale et la comparent aux dénombrements classiques par plaques.
Ajuster les conditions et sonder des cinétiques cachées
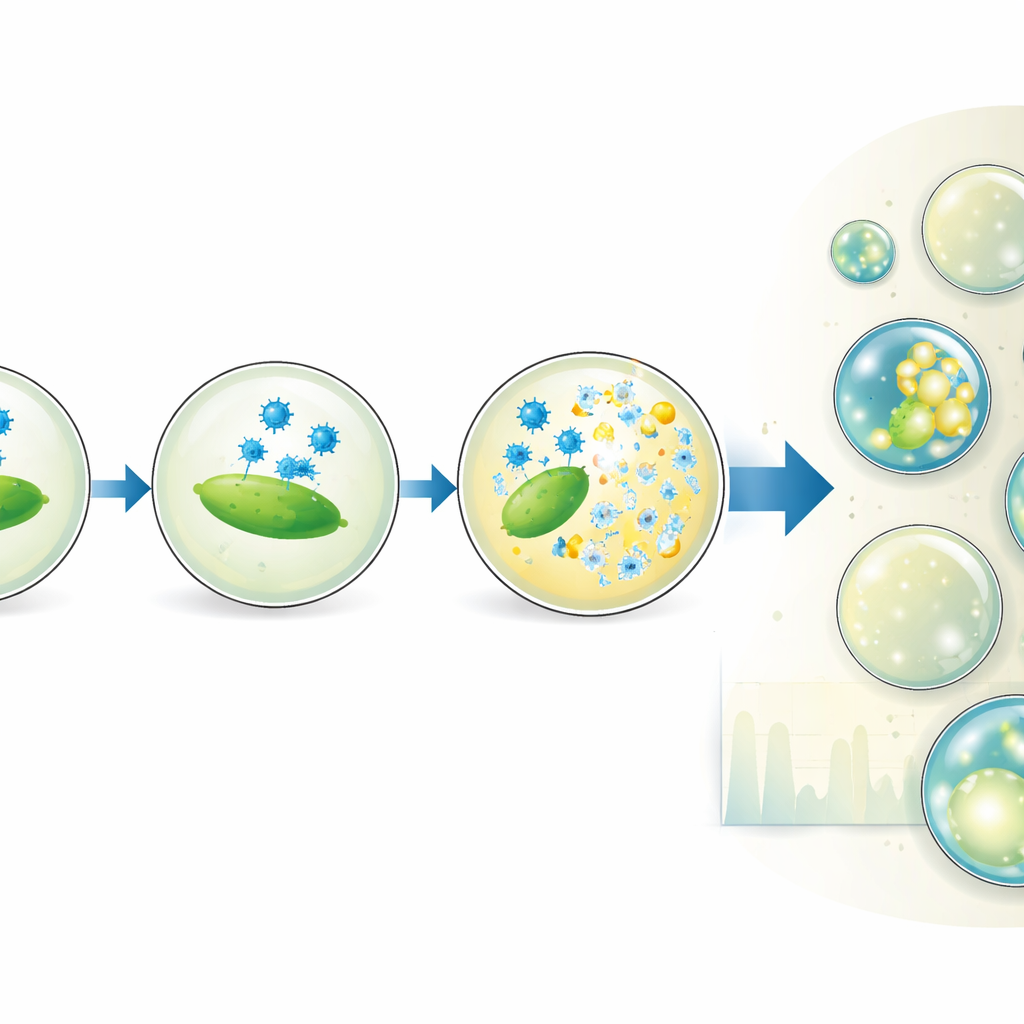
La plate‑forme va au‑delà du simple comptage. En modifiant délibérément le ratio de mélange des solutions virale et bactérienne, l’équipe génère des sous‑populations de gouttelettes avec différents rapports virus‑/hôte, le tout dans une seule expérience. Cela étend efficacement la plage de concentrations sur laquelle l’essai donne des résultats précis et révèle même que toutes les bactéries détectées par des mesures optiques en masse ne sont pas réellement infectables. Les auteurs font aussi varier la taille des gouttelettes et le temps d’incubation pour observer comment la part de gouttelettes lysées augmente. Leur modèle d’adsorption des virus sur les bactéries à l’intérieur des gouttelettes montre que le moment et le succès de la lyse dépendent du nombre réel de cellules capables d’être infectées et de la fréquence des collisions des particules virales avec elles, mais pas fortement du volume de la gouttelette lui‑même.
D’un outil de laboratoire aux thérapies futures
En isolant et en numérisant les événements d’infection individuels, cette méthode par gouttelettes fournit des comptes viraux précis qui correspondent étroitement aux essais de plaques traditionnels, tout en ajoutant des informations temporelles et un contrôle fin des conditions expérimentales. Elle peut être appliquée à de nombreux couples phage–bactérie lytique différents et montée à l’échelle jusqu’à des millions de gouttelettes, ouvrant la voie au criblage à haut débit de variantes de phages, de milieux ou de températures. En termes pratiques, ce travail offre une nouvelle façon puissante de caractériser l’efficacité des phages thérapeutiques à infecter leurs cibles, une étape importante vers l’utilisation de ces prédateurs naturels des bactéries pour aider à combattre les infections résistantes aux antibiotiques.
Citation: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Mots-clés: bactériophages, gouttelettes microfluidiques, thérapie phagique, infection unicellulaire, résistance aux antibiotiques