Clear Sky Science · nl
Fag-gastheerdynamiek kwantificeren met druppelmicrofluïdica
Waarom kleine virussen en druppels voor ons belangrijk zijn
Bacteriedodende virussen, bacteriofagen genoemd, worden heroverwogen als potentiële bondgenoten tegen medicijnresistente infecties. Maar om ze betrouwbare geneesmiddelen te maken, moeten wetenschappers meten hoe effectief individuele virussen bacteriën infecteren en vernietigen — iets waar klassieke laboratoriummethoden moeite mee hebben. Dit artikel introduceert een op druppels gebaseerd traject dat duizenden miniatuurslagen tussen individuele virussen en bacteriën tegelijk observeert, en onthult hoe snel en hoe vaak infecties slagen. Zulke precieze inzichten kunnen leiden tot betere fagtherapieën en ons begrip verdiepen van de verborgen virale wereld die microbieel leven op aarde vormgeeft.
Beperkingen van traditionele petrischaaltesten
Decennialang vertrouwen onderzoekers op plaque-assays: meng virussen met een laagje bacteriën in zacht agar, wacht een nacht en tel vervolgens de heldere plekken waar bacteriën zijn vernietigd. Die plekken schatten het aantal infectieuze virussen dat aanwezig was. Hoewel robuust, is deze methode traag, inflexibel en biedt slechts een eindsnapshot. Ze kan niet volgen hoe infecties zich in de tijd ontwikkelen en vermengt talloze rondes van infectie en herinfectie. Andere benaderingen, zoals bulkfluorescentie- of DNA-gebaseerde tests, middelen nog steeds over grote populaties, waardoor het moeilijk is individuele infectiegebeurtenissen te zien of condities af te stemmen, zoals hoeveel virussen elke bacterie ontmoet.
Elke infectie tot een klein reageerbuisje maken
De auteurs bouwen een hoge-doorvoerplatform dat bacteriën en fagen verpakt in microscopische waterdruppels opgesloten in olie. Twee aparte vloeistofstromen — één met bacteriën en de ander met virussen — ontmoeten elkaar pas bij het smalle knooppunt waar druppels gevormd worden, zodat de blootstellingstijd precies bij encapsulatie begint. Elke druppel wordt een geïsoleerde reactiekamer met een goed gedefinieerd volume en een gecontroleerde verhouding van fagen tot bacteriën. Het team voegt een speciale fluorescente kleurstof toe die sterk oplicht wanneer bacterieel DNA vrijkomt nadat de cel barst, en dient als directe lezing van succesvolle lysis in plaats van alleen de aanwezigheid van viraal genetisch materiaal.
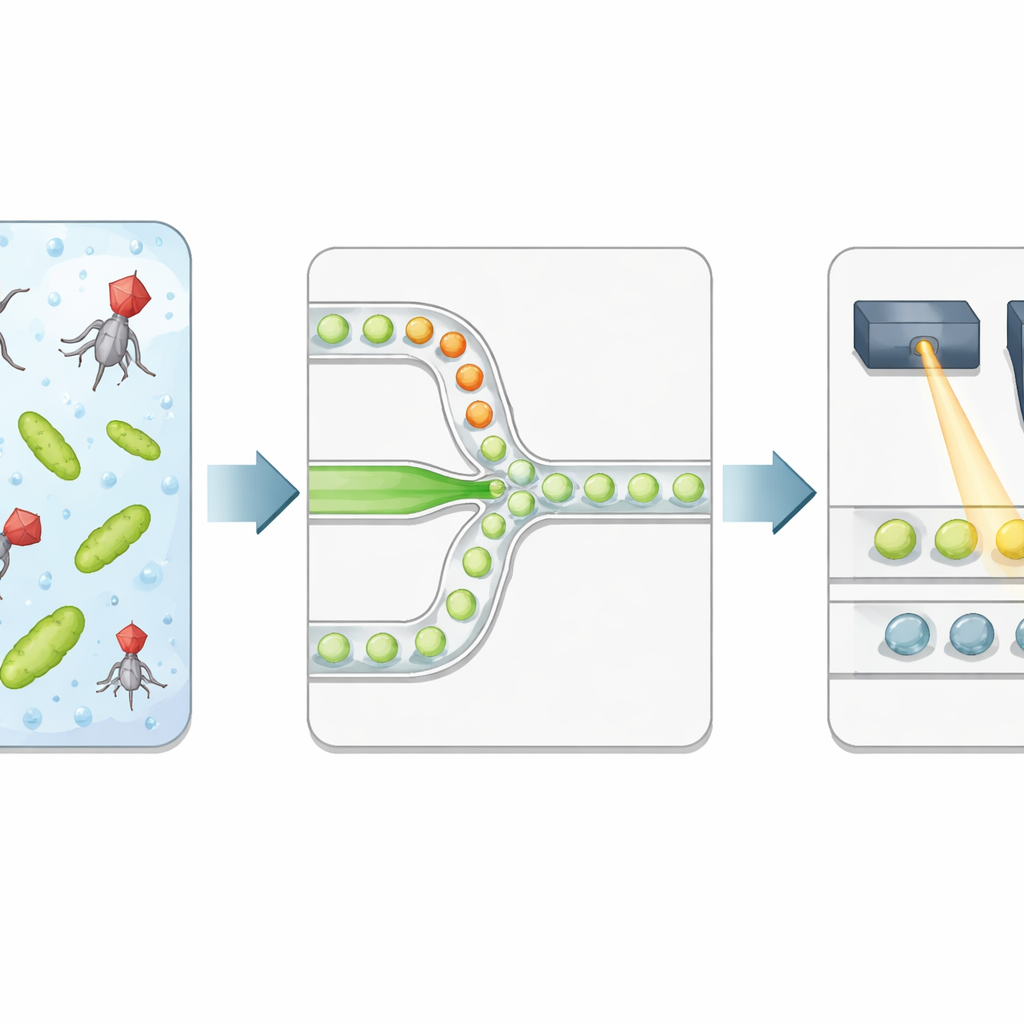
Druppeluitkomsten lezen met licht
Na een gecontroleerde incubatie stroomt de emulsie door een tweede microfluïdische chip die druppels één voor één onder een gefocusseerde laser uitlijnt. Een snelle detector registreert groene fluorescentie van de DNA-kleurstof en rode fluorescentie van een referentiekleurstof die tijdens dropproduktie is toegevoegd. Het rode signaal geeft de druppelgrootte en hoeveel van de virusoplossing elke druppel ontving weer, terwijl het groene signaal rapporteert of lysis heeft plaatsgevonden. Een geautomatiseerde statistische methode scheidt donkere druppels (geen lysis) van heldere (minstens één geïnfecteerde en gelyste bacterie), waarmee het experiment wordt omgezet in een reeks digitale 0-en en 1-en. Door het aandeel heldere druppels te relateren aan het verwachte aantal virussen en bacteriën per druppel, halen de onderzoekers de virusconcentratie terug en vergelijken die met klassieke plaque-tellingen.
Condities afstemmen en verborgen kinetiek onderzoeken
Het platform gaat verder dan eenvoudig tellen. Door doelbewust de mengverhouding van virus- en bacterieoplossingen te veranderen, genereert het team subpopulaties druppels met verschillende virus‑tot‑gastheerverhoudingen, allemaal binnen één experiment. Dit vergroot effectief het concentratiebereik waarbinnen de test nauwkeurige resultaten geeft en onthult zelfs dat niet alle bacteriën die in bulkoptische metingen zichtbaar zijn daadwerkelijk vatbaar zijn voor infectie. De auteurs variëren ook druppelgrootte en incubatietijd om te observeren hoe het aandeel gelyste druppels groeit. Hun model van hoe virussen adsorberen aan bacteriën binnen druppels laat zien dat de timing en het succes van lysis afhangen van het werkelijke aantal infectie‑capabele cellen en hoe vaak virusdeeltjes met hen botsen, maar niet sterk van het druppelvolume zelf.
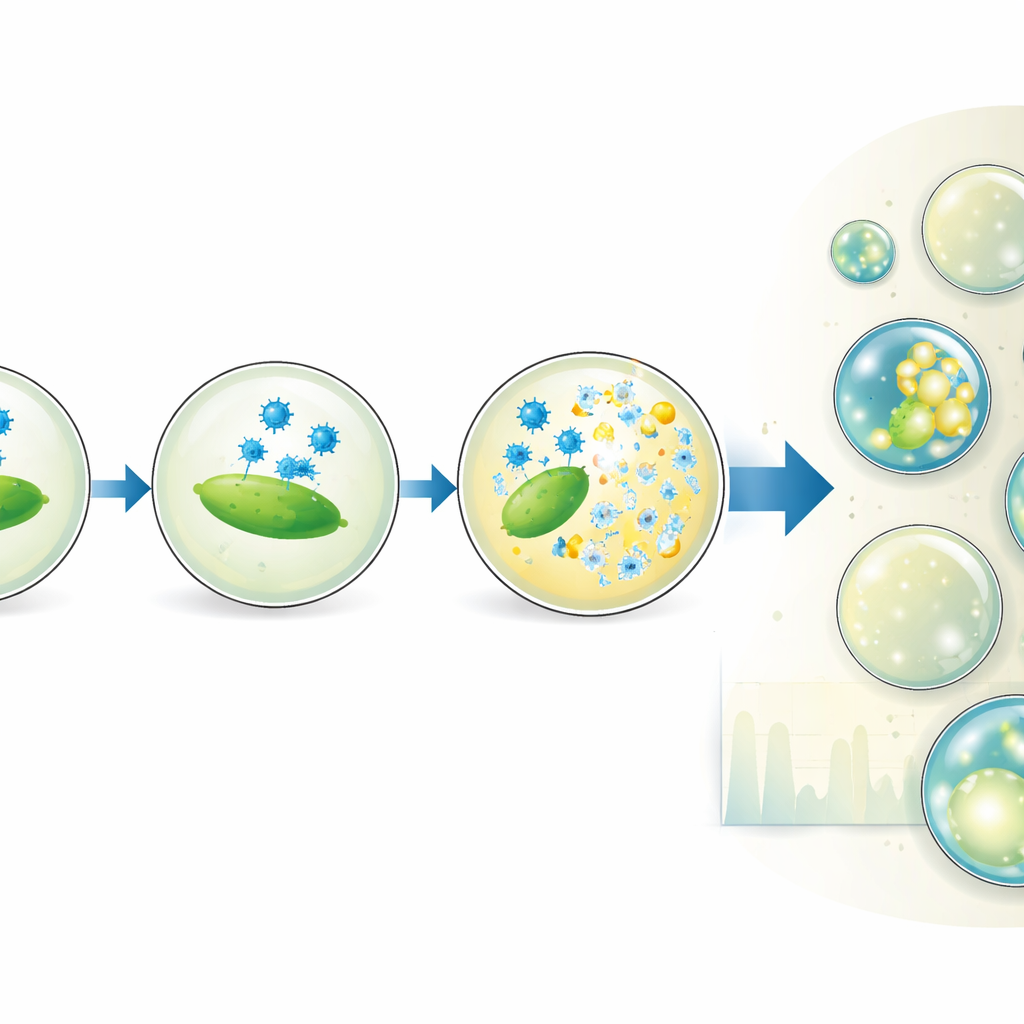
Van labinstrument naar toekomstige therapieën
Door individuele infectiegebeurtenissen te isoleren en te digitaliseren levert deze druppelmethode nauwkeurige virusmetingen die nauw overeenkomen met traditionele plaque-assays, terwijl ze tijdsresolutie en fijne controle over experimentele condities toevoegen. Ze is toepasbaar op veel verschillende lytische fag–bacterieparen en schaalbaar tot miljoenen druppels, wat de deur opent naar hoge-doorvoersscreening van fagvarianten, media of temperaturen. Praktisch gezien biedt het werk een krachtig nieuw middel om te karakteriseren hoe goed therapeutische fagen hun doelwit infecteren — een belangrijke stap richting het gebruik van deze natuurlijke bacteriepredatoren ter bestrijding van antibioticaresistente infecties.
Bronvermelding: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Trefwoorden: bacteriofagen, microfluïdische druppels, fagtherapie, infectie op enkelcelniveau, antibioticaresistentie