Clear Sky Science · pl
Kwantyfikacja dynamiki bakteriofag–gospodarz przy użyciu mikrofluidyki kroplowej
Dlaczego drobne wirusy i krople mają dla nas znaczenie
Wirusy zabijające bakterie, zwane bakteriofagami, zyskują ponownie uwagę jako potencjalni sojusznicy w walce z infekcjami opornymi na leki. Aby jednak przekształcić je w wiarygodne leki, naukowcy muszą zmierzyć, jak skutecznie pojedyncze wirusy infekują i niszczą bakterie — co klasyczne metody laboratoryjne robią z trudem. W artykule przedstawiono podejście oparte na kroplach, które jednocześnie obserwuje tysiące miniaturowych pojedynków między pojedynczymi wirusami a bakteriami, ujawniając, jak szybko i jak często zakażenia odnoszą sukces. Takie precyzyjne wnioski mogą prowadzić do lepszych terapii fagowych i pogłębić nasze zrozumienie ukrytego świata wirusów kształtujących życie mikrobiologiczne na Ziemi.
Ograniczenia tradycyjnych testów na płytkach Petriego
Przez dekady badacze polegali na testach płytkowych: mieszają wirusy z „trawnikiem” bakterii w miękkim agaru, czekają noc, a potem liczą przejrzyste plamy, gdzie bakterie zostały zniszczone. Te plamy szacują, ile zakaźnych wirusów było obecnych. Choć metoda jest solidna, jest powolna, mało elastyczna i daje tylko końcowy obraz. Nie pozwala śledzić przebiegu zakażeń w czasie i scala niezliczone rundy zakażeń i reinfekcji. Inne podejścia, takie jak pomiary fluorescencyjne w zbiorze czy testy oparte na DNA, nadal uśredniają dane po ogromnych populacjach, co utrudnia dostrzeżenie pojedynczych zdarzeń infekcyjnych lub precyzyjne dobranie warunków, np. liczby wirusów przypadającej na każdą bakterię.
Przekształcanie każdej infekcji w miniaturową probówkę
Autorzy zbudowali wydajną platformę, która pakuje bakterie i fagii do mikroskopijnych kropli wody zawieszonych w oleju. Dwa oddzielne strumienie cieczy — jeden z bakteriami, drugi z wirusami — spotykają się dopiero w wąskim złączu, gdzie powstają krople, dzięki czemu czas ekspozycji rozpoczyna się precyzyjnie w momencie enkapsulacji. Każda kropla staje się izolowaną komorą reakcyjną o dobrze określonej objętości i kontrolowanym stosunku fagów do bakterii. Zespół dodaje specjalny barwnik fluorescencyjny, który mocno świeci, gdy DNA bakteryjne zostaje uwolnione po pęknięciu komórki, służąc jako bezpośredni wskaźnik udanej lizy, a nie jedynie obecności materiału genetycznego wirusa.
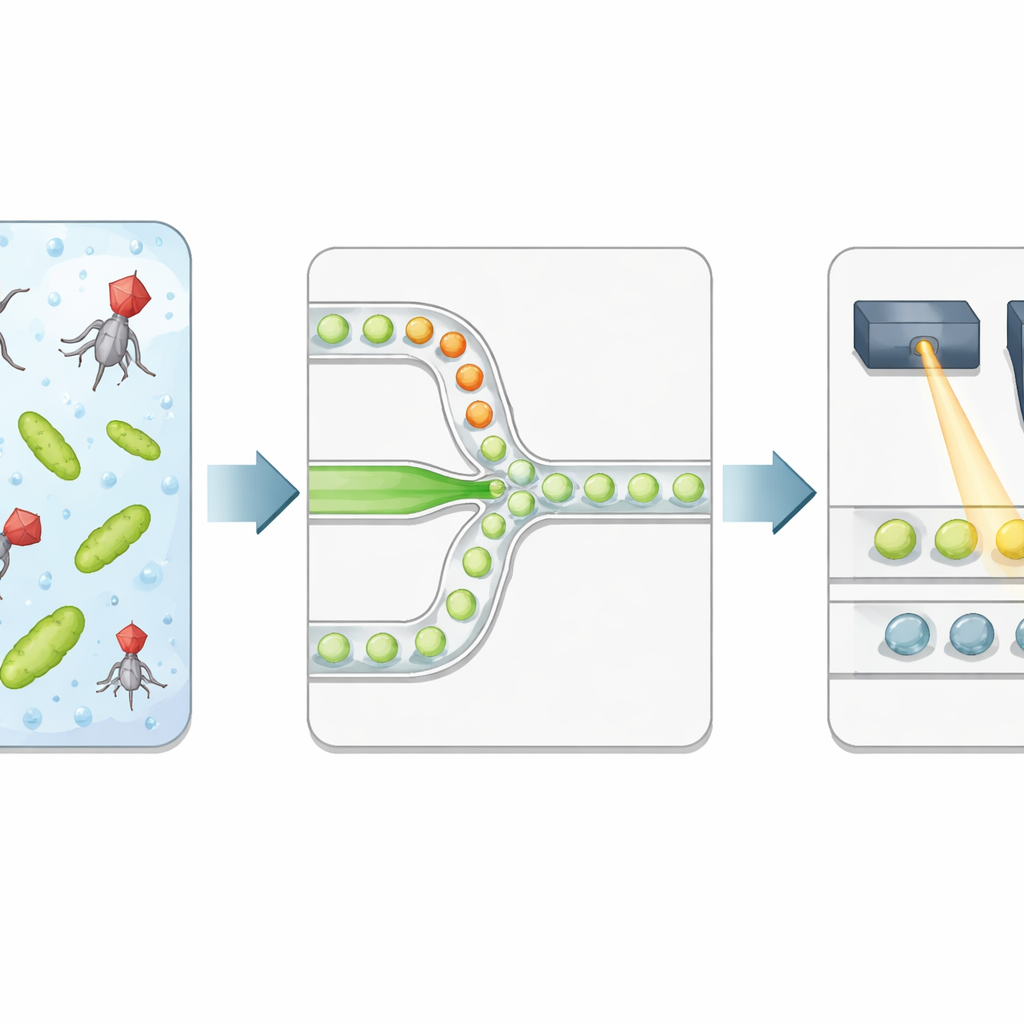
Odczytywanie wyników kropli światłem
Po kontrolowanej inkubacji emulsję przepuszcza się przez drugi chip mikrofluidyczny, który ustawia krople jedna za drugą pod skupionym laserem. Szybki detektor rejestruje zieloną fluorescencję barwnika DNA i czerwoną fluorescencję barwnika referencyjnego dołączonego podczas tworzenia kropli. Sygnał czerwony informuje o rozmiarze kropli i o tym, ile roztworu z wirusami każda kropla otrzymała, podczas gdy zielony sygnał wskazuje, czy zaszła liza. Zautomatyzowana metoda statystyczna rozdziela ciemne krople (brak lizy) od jasnych (przynajmniej jedna zainfekowana i zlysisowana bakteria), przekształcając eksperyment w ciąg cyfrowych 0 i 1. Poprzez powiązanie ułamka jasnych kropli z oczekiwaną liczbą wirusów i bakterii na kroplę, badacze odzyskują stężenie wirusów i porównują je z klasycznymi wynikami płytkowymi.
Dopasowywanie warunków i badanie ukrytej kinetyki
Platforma wykracza poza proste liczenie. Poprzez celowe zmienianie stosunku mieszaniny wirusów do bakterii, zespół generuje subpopulacje kropli z różnymi stosunkami wirus–gospodarz, wszystkie w ramach jednego eksperymentu. To efektywnie rozszerza zakres stężeń, dla których test daje precyzyjne wyniki, i ujawnia nawet to, że nie wszystkie bakterie widziane w pomiarach optycznych masowych są rzeczywiście zdolne do zakażenia. Autorzy zmieniają też rozmiar kropli i czas inkubacji, aby obserwować, jak rośnie udział kropli z lizą. Ich model adsorpcji wirusów na bakteriach w kroplach pokazuje, że czas i sukces lizy zależą od rzeczywistej liczby komórek zdolnych do zakażenia oraz od częstotliwości zderzeń z cząstkami wirusa, a nie silnie od samej objętości kropli.
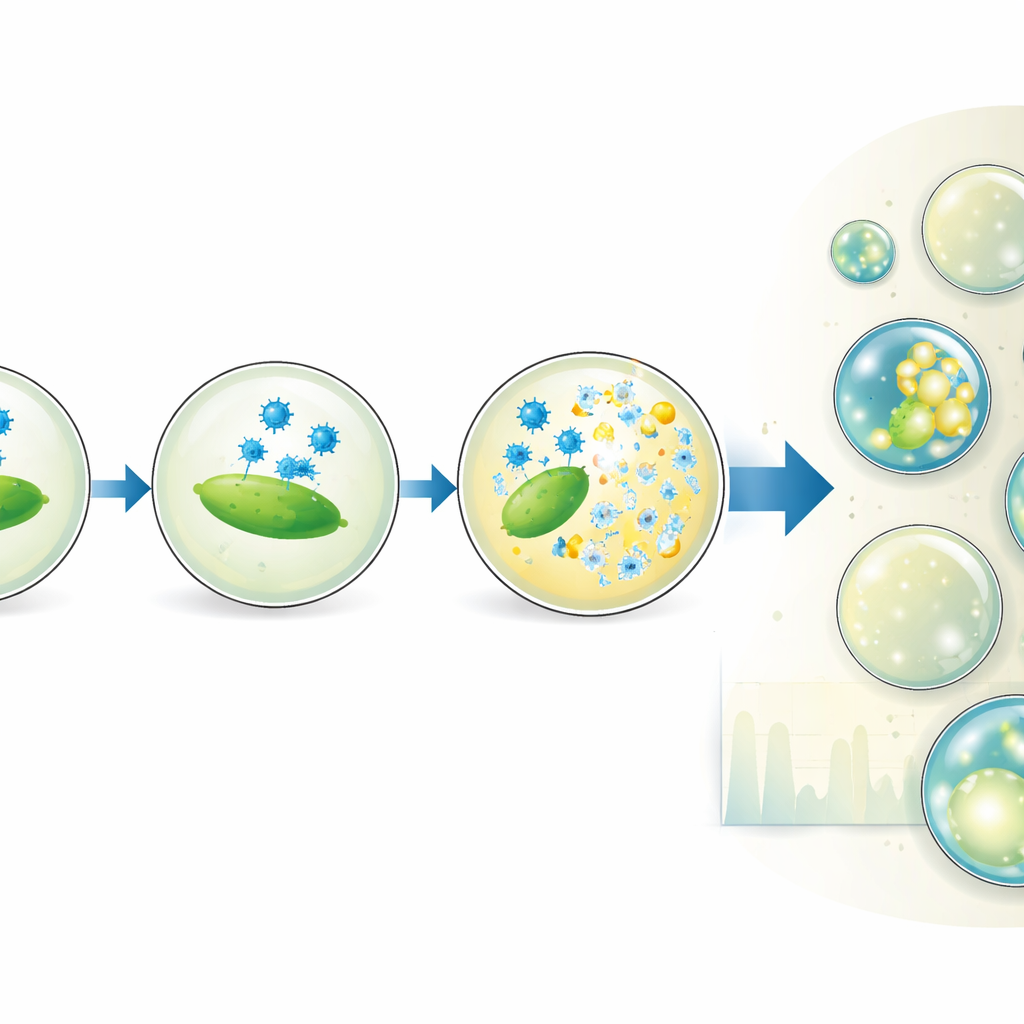
Od narzędzia laboratoryjnego do przyszłych terapii
Izolując i digitalizując pojedyncze zdarzenia infekcyjne, metoda kroplowa dostarcza dokładnych pomiarów liczby wirusów, które ściśle zgadzają się z tradycyjnymi testami płytkowymi, a przy tym dodaje informacje rozdzielcze w czasie i precyzyjną kontrolę warunków eksperymentalnych. Można ją zastosować do wielu par fag–bakteria o charakterze litycznym i skalować do milionów kropli, otwierając drzwi do wysokoprzepustowego przesiewu wariantów fagów, podłoży czy temperatur. W praktycznym wymiarze praca dostarcza potężnego nowego sposobu charakteryzacji, jak dobrze terapeutyczne fagii infekują swoje cele — istotny krok w kierunku wykorzystania tych naturalnych drapieżników bakterii w walce z infekcjami opornymi na antybiotyki.
Cytowanie: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Słowa kluczowe: bakteriofagi, mikrofluidyczne krople, terapia fagowa, infekcja pojedynczej komórki, oporność na antybiotyki