Clear Sky Science · it
Quantificare le dinamiche fago‑ospite usando la microfluidica a gocce
Perché per noi contano i virus e le gocce microscopiche
I virus che uccidono i batteri, detti batteriofagi, sono di nuovo considerati possibili alleati contro le infezioni resistenti ai farmaci. Ma per trasformarli in medicinali affidabili, gli scienziati devono misurare quanto efficacemente singoli virus infettano e distruggono i batteri, cosa che i metodi classici di laboratorio faticano a fare. Questo articolo presenta un approccio basato su gocce che osserva migliaia di piccoli scontri tra singoli virus e batteri contemporaneamente, rivelando con quale rapidità e con quale frequenza le infezioni hanno successo. Informazioni così precise potrebbero guidare terapie con fagi migliori e approfondire la nostra comprensione del mondo virale nascosto che plasma la vita microbica sulla Terra.
Limiti dei test tradizionali su piastre Petri
Per decenni i ricercatori si sono affidati alle saggi delle placche: mescolare i virus con un tappeto di batteri in agar morbido, aspettare una notte e poi contare i punti chiari dove i batteri sono stati eliminati. Questi punti stimano quanti virus infettivi erano presenti. Pur essendo robusto, questo metodo è lento, poco flessibile e offre solo un’istantanea finale. Non può seguire come le infezioni si sviluppano nel tempo e mescola insieme innumerevoli cicli di infezione e reinfezione. Altri approcci, come la fluorescenza in massa o i test basati sul DNA, fanno ancora la media su enormi popolazioni, rendendo difficile osservare singoli eventi di infezione o regolare condizioni come il numero di virus per batterio.
Trasformare ogni infezione in una provetta minuscola
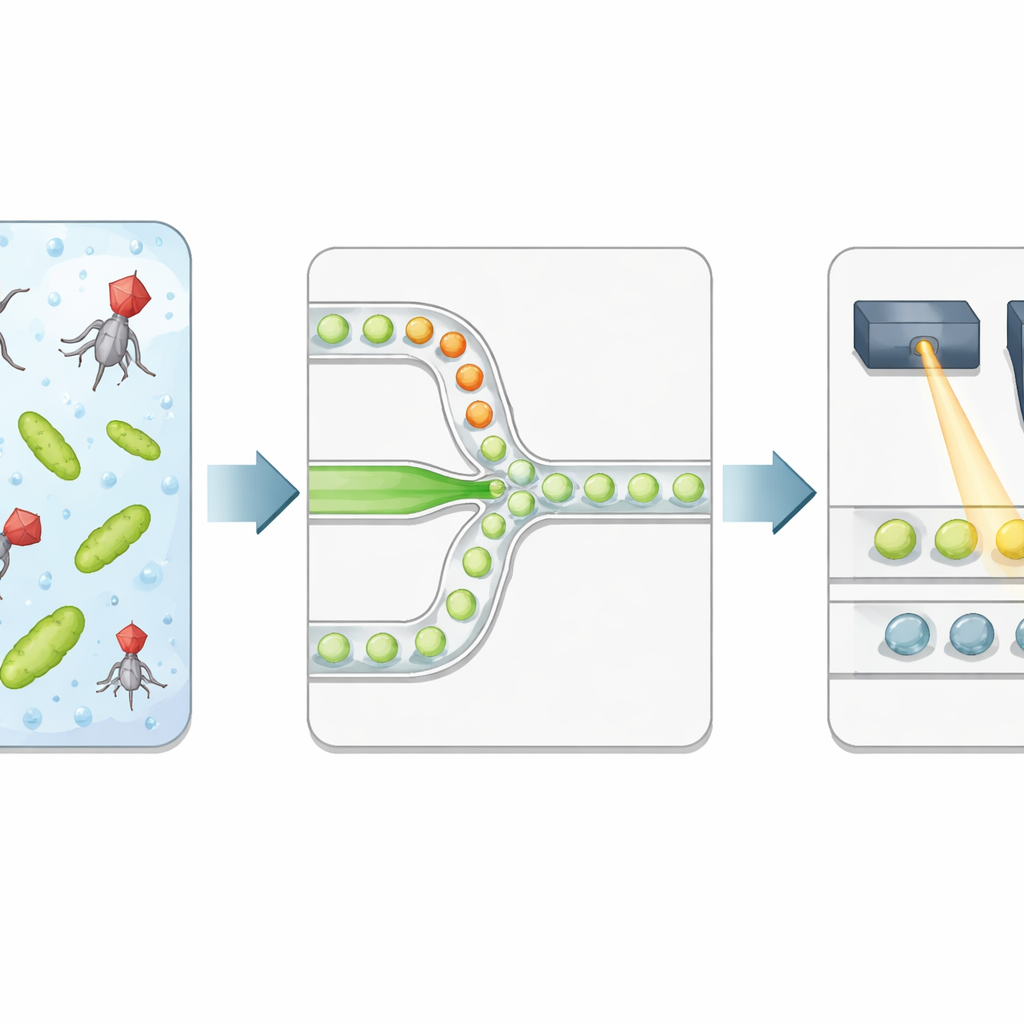
Gli autori costruiscono una piattaforma ad elevata produttività che incapsula batteri e fagi in gocce microscopiche d’acqua sospese in olio. Due flussi liquidi separati—uno che trasporta i batteri, l’altro i virus—si incontrano solo al giunto stretto dove si formano le gocce, così il tempo di esposizione inizia con precisione al momento dell’incapsulamento. Ogni goccia diventa una camera di reazione isolata con un volume ben definito e un rapporto controllato di fagi per batteri. Il team aggiunge un colorante fluorescente speciale che si illumina fortemente quando il DNA batterico viene rilasciato dopo la lisi cellulare, servendo come lettura diretta della lisi riuscita piuttosto che della sola presenza di materiale genetico virale.
Leggere gli esiti nelle gocce con la luce
Dopo un’incubazione controllata, l’emulsione viene fatta fluire attraverso un secondo chip microfluidico che allinea le gocce una per una sotto un laser focalizzato. Un rivelatore veloce registra la fluorescenza verde del colorante per il DNA e la fluorescenza rossa di un colorante di riferimento incluso durante la produzione delle gocce. Il segnale rosso indica la dimensione della goccia e quanto della soluzione virale ogni goccia ha ricevuto, mentre il segnale verde indica se è avvenuta la lisi. Un metodo statistico automatizzato separa le gocce deboli (nessuna lisi) da quelle luminose (almeno un batterio infettato e lisato), convertendo l’esperimento in una sequenza digitale di 0 e 1. Relazionando la frazione di gocce luminose con il numero atteso di virus e batteri per goccia, i ricercatori ricavano la concentrazione virale e la confrontano con il conteggio classico delle placche.
Regolare le condizioni e sondare la cinetica nascosta
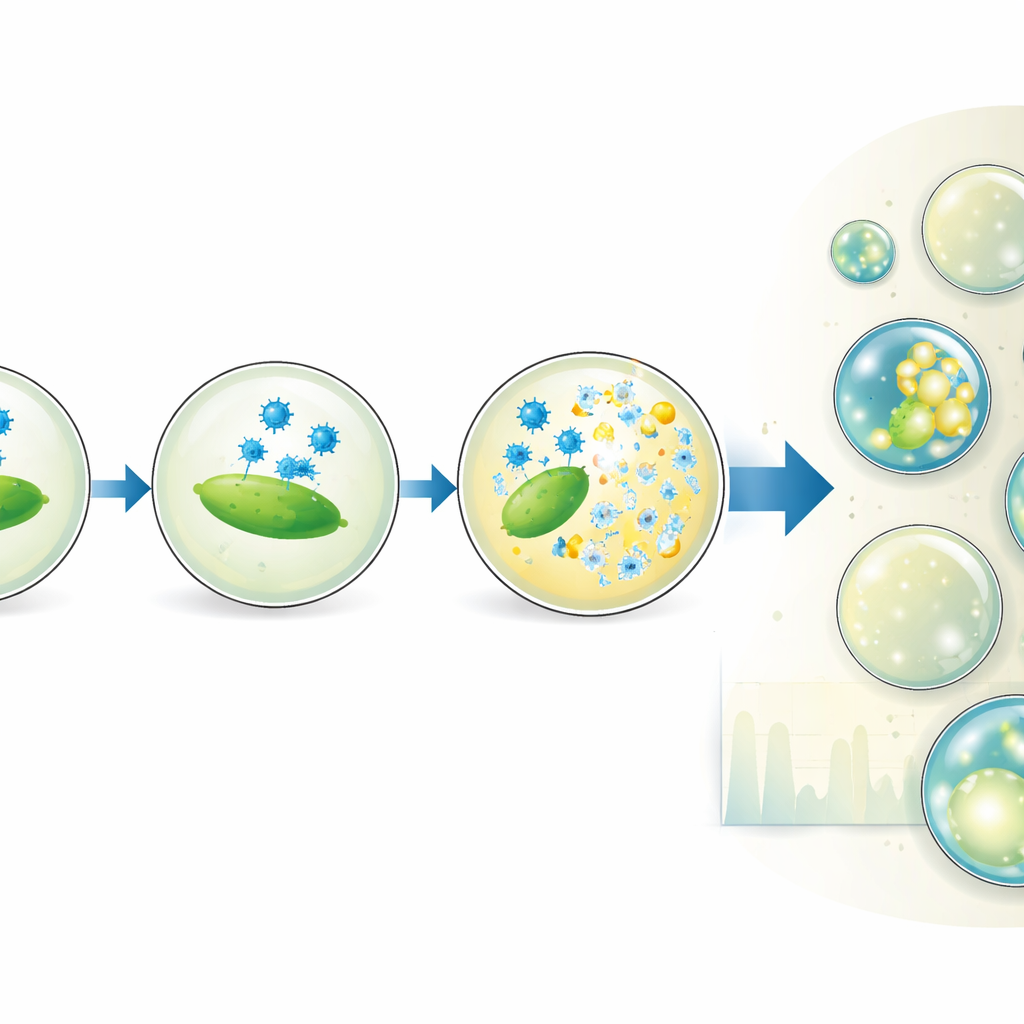
La piattaforma va oltre il semplice conteggio. Modificando intenzionalmente il rapporto di miscelazione delle soluzioni di virus e batteri, il team genera sottopopolazioni di gocce con diversi rapporti virus‑ospite, il tutto all’interno di un singolo esperimento. Questo estende efficacemente la gamma di concentrazioni su cui il saggio fornisce risultati precisi e rivela persino che non tutti i batteri misurati da rilevamenti ottici in bulk sono effettivamente suscettibili all’infezione. Gli autori variano anche la dimensione delle gocce e il tempo di incubazione per osservare come cresce la percentuale di gocce lisate. Il loro modello di adsorbimento dei virus sui batteri all’interno delle gocce mostra che i tempi e il successo della lisi dipendono dal numero reale di cellule capaci di essere infettate e da quanto spesso le particelle virali entrano in collisione con esse, ma non dipendono fortemente dal volume della goccia stesso.
Da strumento di laboratorio a terapie future
Isolando e digitalizzando singoli eventi di infezione, questo metodo a gocce fornisce conteggi virali accurati che corrispondono da vicino ai saggi tradizionali delle placche, aggiungendo al contempo informazioni risolte nel tempo e controllo fine delle condizioni sperimentali. Può essere applicato a molte coppie fagiche‑batteriche litiche diverse e scalato a milioni di gocce, aprendo la strada a screening ad alto rendimento di varianti di fagi, terreni di coltura o temperature. In termini pratici, il lavoro offre un nuovo potente modo per caratterizzare quanto bene i fagi terapeutici infettano i loro bersagli, un passo importante verso l’uso di questi predatori naturali dei batteri per contribuire a combattere le infezioni resistenti agli antibiotici.
Citazione: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Parole chiave: batteriofagi, gocce microfluidiche, terapia con fagi, infezione a singola cellula, resistenza agli antibiotici