Clear Sky Science · sv
Kvantifiering av fager‑värddynamik med droppmikrofluidik
Varför små virus och droppar spelar roll för oss
Virus som dödar bakterier, så kallade bakteriofager, utforskas på nytt som potentiella allierade mot läkemedelsresistenta infektioner. Men för att förvandla dem till pålitliga läkemedel måste forskare mäta hur effektivt enskilda virus infekterar och förstör bakterier — något klassiska laboratoriemetoder har svårt att göra. Denna artikel presenterar en droppbaserad metod som iakttar tusentals miniatyrstrider mellan enskilda virus och bakterier samtidigt, och avslöjar hur snabbt och hur ofta infektioner lyckas. Sådan precis kunskap kan vägleda bättre fagterapier och fördjupa vår förståelse av den dolda virusvärlden som formar mikrobiellt liv på jorden.
Begränsningar med traditionella petriskålsprov
I årtionden har forskare förlitat sig på plack‑analyser: blanda virus med ett bakterielager i mjukagar, vänta över natten och räkna sedan klara fläckar där bakterierna utplånats. Dessa fläckar uppskattar hur många infektiösa virus som fanns. Metoden är robust men långsam, oflexibel och ger bara en slutlig ögonblicksbild. Den kan inte följa hur infektioner utvecklas över tid och den blandar ihop otaliga rundor av infektion och reinfektion. Andra tillvägagångssätt, som bulkfluorescens eller DNA‑baserade tester, summerar fortfarande över stora populationer, vilket gör det svårt att se enskilda infektionstillfällen eller att finjustera förhållanden som hur många virus som möter varje bakterie.
Att göra varje infektion till ett litet provrör
Författarna bygger en höggenomströmningplattform som förpackar bakterier och fager i mikroskopiska vattendroppar suspenderade i olja. Två separata vätskeströmmar — en med bakterier, den andra med virus — möts först vid den smala korsningen där dropparna bildas, så exponeringstiden börjar exakt vid inkapsling. Varje droppe blir en isolerad reaktionskammare med väl definierad volym och ett kontrollerat förhållande mellan fager och bakterier. Teamet tillsätter en särskild fluorescerande färg som lyser starkt när bakterie‑DNA släpps ut efter att cellen spruckit, vilket fungerar som en direkt avläsning av lyckad lysering snarare än bara närvaro av viralt genetiskt material.
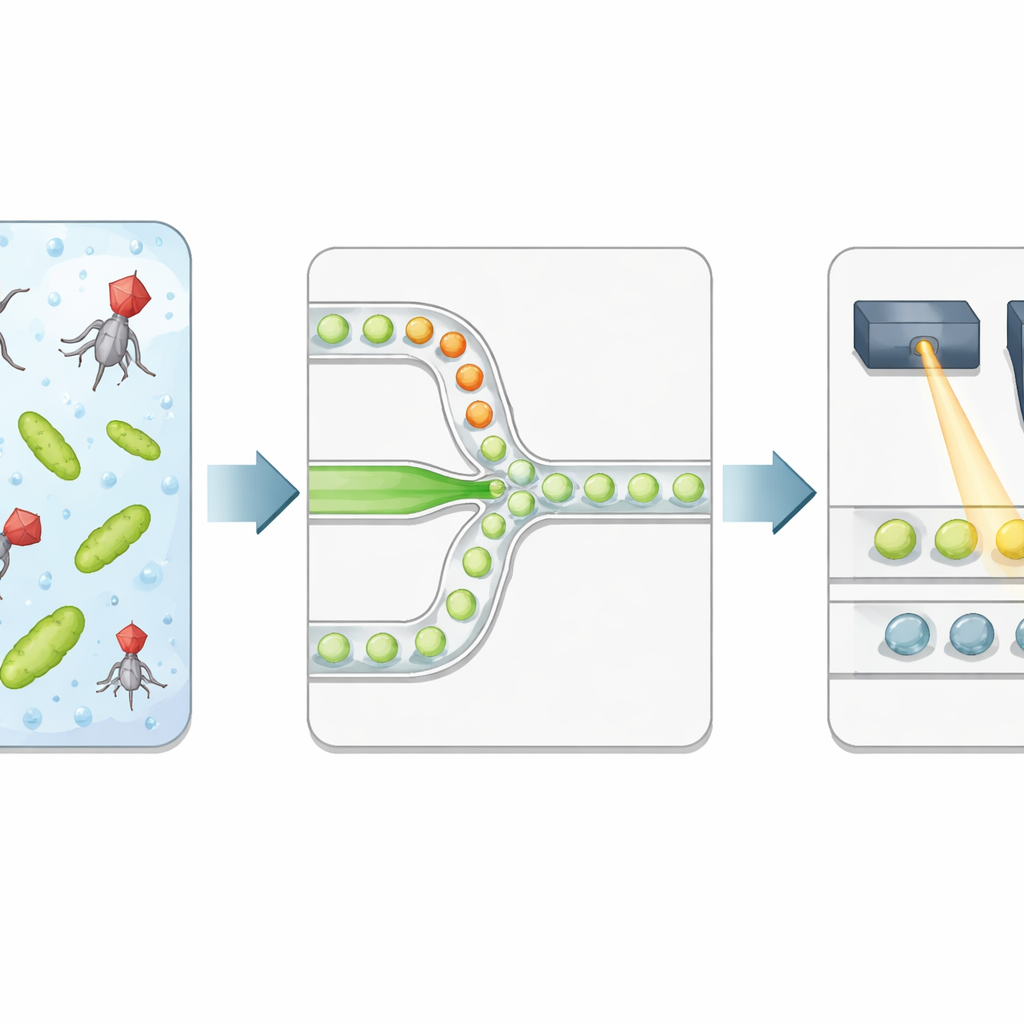
Läsa dropputfall med ljus
Efter en kontrollerad inkubation leds emulsionen genom en andra mikrofluidisk chip som rada upp droppar en och en under en fokuserad laser. En snabb detektor registrerar grön fluorescens från DNA‑färgen och röd fluorescens från en referensfärg som tillsatts vid droppproduktionen. Den röda signalen rapporterar droppstorlek och hur mycket av virallösningen varje droppe fick, medan den gröna signalen indikerar om lysering har skett. En automatiserad statistisk metod skiljer svaga droppar (ingen lysering) från ljusa (minst en infekterad och tilltufsad bakterie), och konverterar experimentet till en sträng av digitala 0:or och 1:or. Genom att relatera andelen ljusa droppar till det förväntade antalet virus och bakterier per droppe återvinner forskarna viruskoncentrationen och jämför den med klassiska plackräkningar.
Justera förhållanden och utforska dold kinetik
Plattformen går bortom enkel räkning. Genom att medvetet ändra blandningsförhållandet mellan virus‑ och bakterielösningarna skapar teamet subpopulationer av droppar med olika virus‑till‑värd‑kvoter, allt inom ett enda experiment. Detta sträcker effektivt intervallet av koncentrationer där analysen ger precisa resultat och visar till och med att inte alla bakterier som syns i bulkoptiska mätningar faktiskt kan infekteras. Författarna varierar också droppstorlek och inkubationstid för att följa hur andelen lysade droppar växer. Deras modell för hur virus adsorberas till bakterier inne i droppar visar att tidpunkten och framgången för lysering beror på det verkliga antalet infektionseffektiva celler och på hur ofta viruspartiklar kolliderar med dem, men inte starkt på droppvolymen i sig.
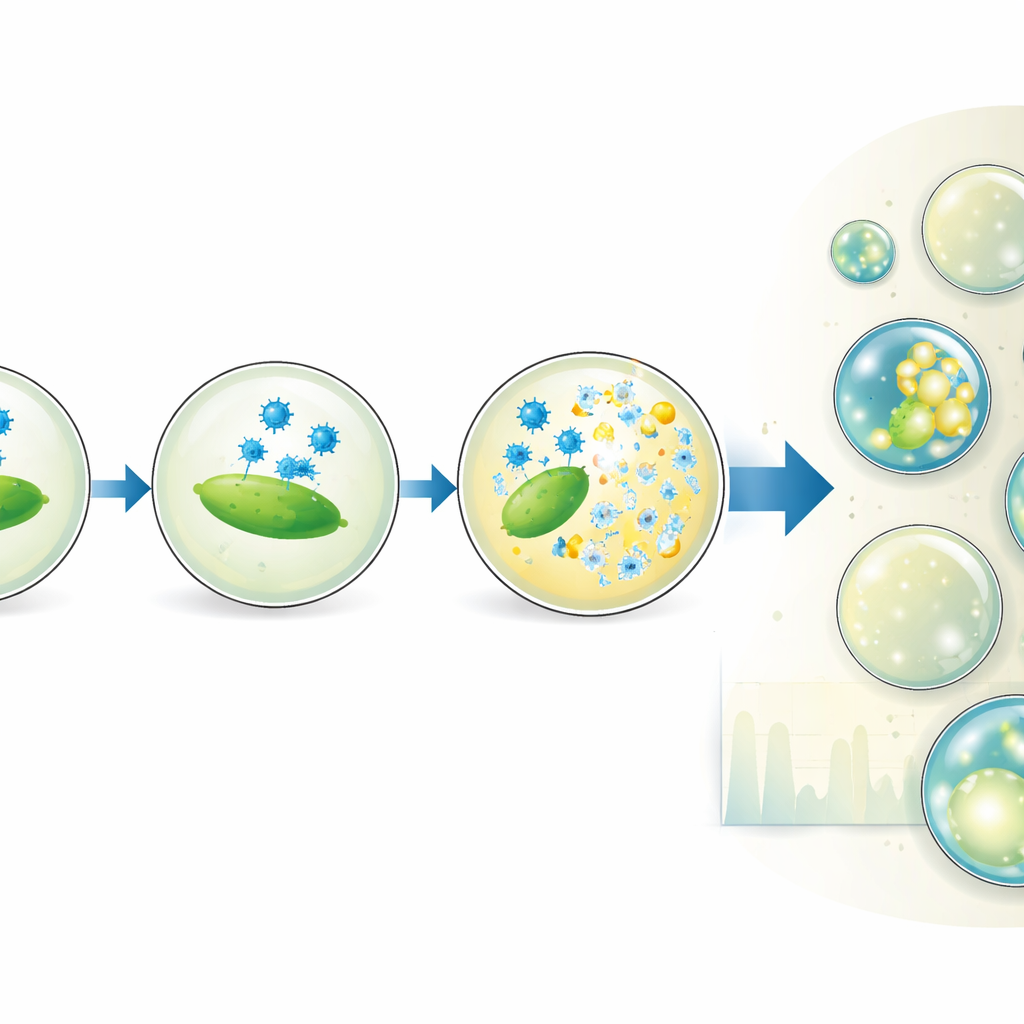
Från labbverktyg till framtida terapier
Genom att isolera och digitalisera enskilda infektionstillfällen levererar denna droppmetod noggranna virusräkningar som ligger nära traditionella plackanalyser, samtidigt som den tillför tidsupplöst information och fin kontroll över experimentella förhållanden. Den kan tillämpas på många olika lytiska fag–bakterie‑par och skalas upp till miljontals droppar, vilket öppnar dörren för höggenomströmningsscreening av fagvarianter, medier eller temperaturer. I praktiska termer ger arbetet ett kraftfullt nytt sätt att karakterisera hur väl terapeutiska fager infekterar sina mål, ett viktigt steg mot att använda dessa naturliga bakteriepredatorer för att bekämpa antibiotikaresistenta infektioner.
Citering: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Nyckelord: bakteriofager, mikrofluidiska droppar, fagterapi, infektion på enskild cellnivå, antibiotikaresistens