Clear Sky Science · de
Quantifizierung von Phagen‑Wirt‑Dynamiken mittels Tropfen‑Mikrofluidik
Warum winzige Viren und Tropfen für uns wichtig sind
Bakterienabtötende Viren, sogenannte Bakteriophagen, werden als mögliche Helfer gegen medikamentenresistente Infektionen neu bewertet. Um sie jedoch in verlässliche Medikamente zu verwandeln, müssen Forschende messen, wie effizient einzelne Viren Bakterien infizieren und zerstören — etwas, das klassische Laborverfahren schwer leisten. Diese Arbeit stellt einen tropfenbasierten Ansatz vor, der Tausende winziger Gefechte zwischen einzelnen Viren und Bakterien gleichzeitig beobachtet und aufzeigt, wie schnell und wie häufig Infektionen erfolgreich sind. Solch präzise Erkenntnisse könnten zu besseren Phagentherapien führen und unser Verständnis der verborgenen Virenwelt vertiefen, die mikrobielles Leben auf der Erde prägt.
Grenzen traditioneller Petrischalen‑Tests
Jahrzehntelang verließen sich Forschende auf Plaque‑Assays: Man mischt Viren mit einem Bakterienrasen in weichem Agar, wartet über Nacht und zählt dann die klaren Stellen, an denen Bakterien ausgelöscht wurden. Diese Flecken schätzen, wie viele infektiöse Viren vorhanden waren. Zwar robust, ist diese Methode langsam, unflexibel und liefert nur einen Endzustand. Sie kann nicht verfolgen, wie sich Infektionen über die Zeit entwickeln, und sie vermischt zahllose Runden von Infektion und Reinfection. Andere Ansätze, etwa Fluoreszenz‑Messungen im Bulk oder DNA‑basierte Tests, mitteln ebenfalls über große Populationen, wodurch einzelne Infektionsereignisse schwer zu erkennen sind oder Bedingungen wie das Verhältnis von Viren zu Bakterien nicht präzise variiert werden können.
Jede Infektion in ein winziges Reagenzglas verwandeln
Die Autorinnen und Autoren bauen eine Hochdurchsatzplattform, die Bakterien und Phagen in mikroskopische Wassertröpfchen in Öl einschließt. Zwei separate Flüssigkeitsströme — einer mit Bakterien, der andere mit Viren — treffen erst an der engen Stelle zusammen, an der Tropfen gebildet werden, sodass die Expositionszeit genau bei der Einkapselung beginnt. Jeder Tropfen wird zu einer isolierten Reaktionskammer mit definiertem Volumen und kontrolliertem Phagen‑zu‑Bakterien‑Verhältnis. Das Team fügt einen speziellen Fluoreszenzfarbstoff hinzu, der stark aufleuchtet, wenn bakterielle DNA freigesetzt wird, nachdem die Zelle geplatzt ist, und so direkt erfolgreichen Lyseereignissen anzeigt statt nur das Vorhandensein viraler Erbinformation.
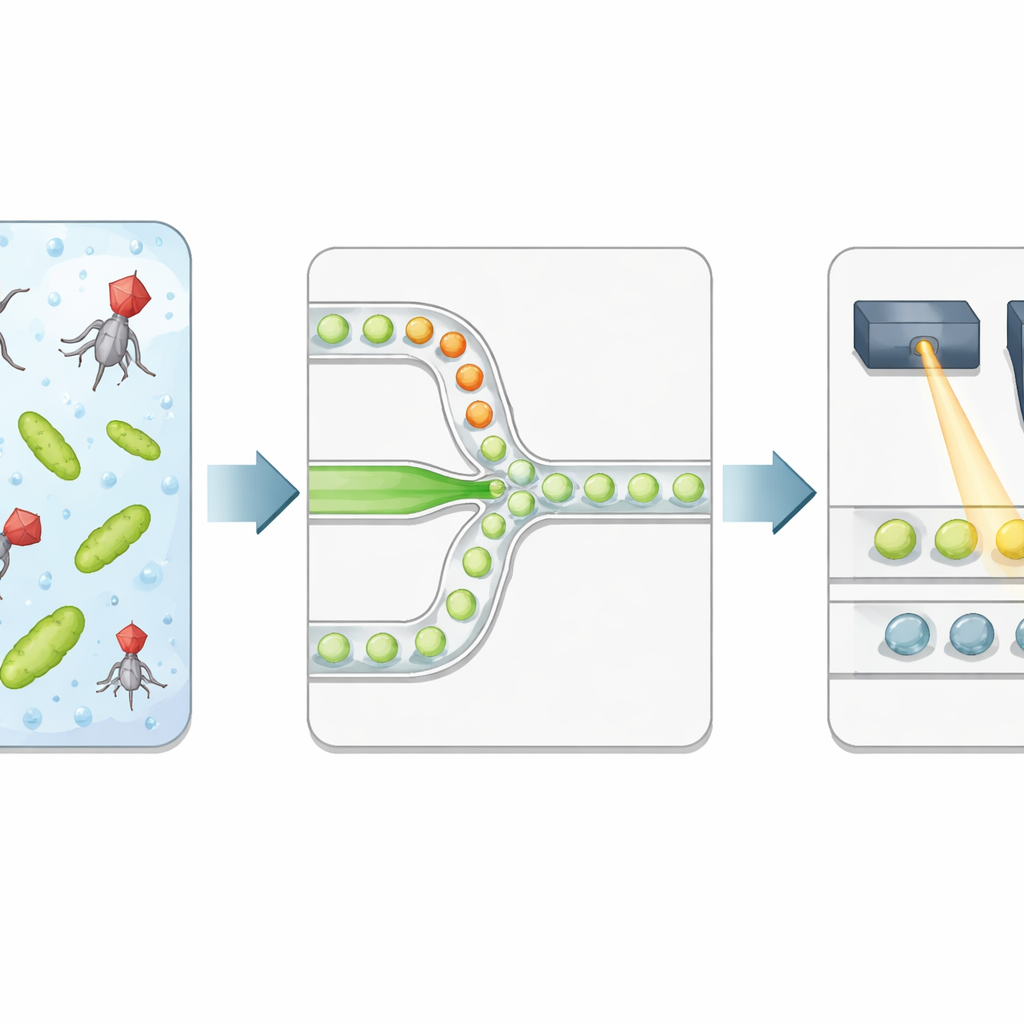
Ergebnisse der Tropfen mit Licht lesen
Nach einer kontrollierten Inkubation wird die Emulsion durch einen zweiten mikrofluidischen Chip geführt, der Tropfen einzeln unter einen fokussierten Laser ausrichtet. Ein schneller Detektor zeichnet grünes Fluoreszenzsignal des DNA‑Färbemittels und rotes Fluoreszenzsignal eines Referenzfarbstoffs auf, der während der Tropfenproduktion zugegeben wurde. Das rote Signal informiert über Tropfengröße und darüber, wie viel von der Viruslösung jeder Tropfen erhalten hat, während das grüne Signal anzeigt, ob Lyse stattgefunden hat. Eine automatisierte statistische Methode trennt dunkle Tropfen (keine Lyse) von hellen (mindestens ein infiziertes und lysiertes Bakterium) und wandelt das Experiment in eine Folge digitaler 0en und 1en um. Indem der Anteil heller Tropfen mit den erwarteten Zahlen von Viren und Bakterien pro Tropfen in Beziehung gesetzt wird, bestimmen die Forschenden die Viruskonzentration und vergleichen sie mit klassischen Plaque‑Zählungen.
Bedingungen anpassen und verborgene Kinetiken untersuchen
Die Plattform geht über einfaches Zählen hinaus. Durch gezielte Veränderung des Mischverhältnisses von Virus‑ und Bakterienlösungen erzeugt das Team Subpopulationen von Tropfen mit unterschiedlichen Virus‑zu‑Wirt‑Verhältnissen, alles innerhalb eines Experiments. Das dehnt effektiv den Konzentrationsbereich, über den der Test präzise Ergebnisse liefert, und zeigt sogar, dass nicht alle in Bulk‑optischen Messungen sichtbaren Bakterien tatsächlich infizierbar sind. Die Autorinnen und Autoren variieren außerdem Tropfengröße und Inkubationszeit, um zu beobachten, wie der Anteil lysierter Tropfen wächst. Ihr Modell zur Adsorption von Viren an Bakterien innerhalb der Tropfen zeigt, dass Zeitpunkt und Erfolg der Lyse von der tatsächlichen Zahl infektiöser Zellen und davon abhängen, wie häufig Viruspartikel mit ihnen zusammenstoßen, nicht aber stark vom Tropfenvolumen selbst.
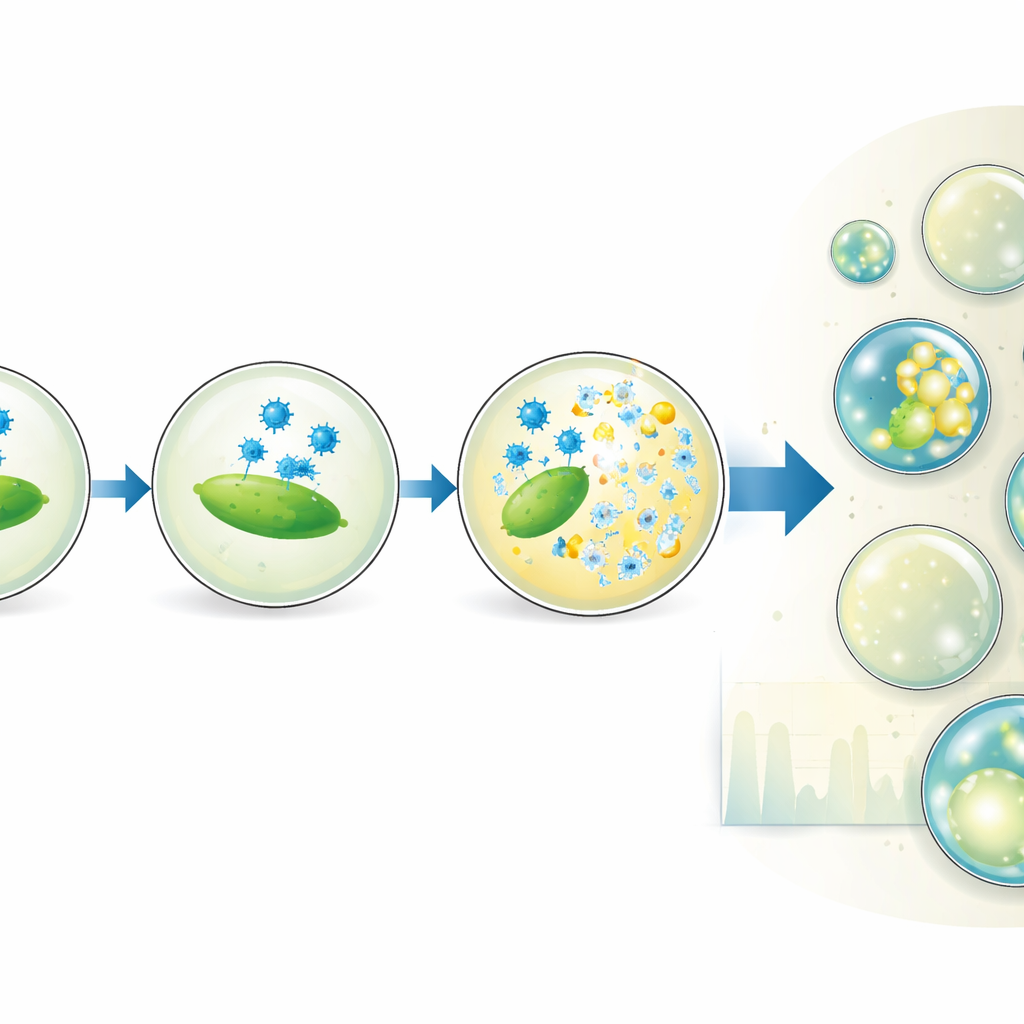
Vom Labortool zu künftigen Therapien
Indem einzelne Infektionsereignisse isoliert und digitalisiert werden, liefert diese Tropfenmethode genaue Viruszählungen, die gut mit traditionellen Plaque‑Assays übereinstimmen, und ergänzt sie um zeitaufgelöste Informationen und präzise Kontrolle über Versuchsbedingungen. Sie lässt sich auf viele verschiedene lytische Phage–Bakterien‑Paare anwenden und auf Millionen Tropfen skalieren, was den Weg für Hochdurchsatz‑Screenings von Phagenvarianten, Nährmedien oder Temperaturen öffnet. Praktisch betrachtet bietet die Arbeit eine leistungsfähige neue Möglichkeit, wie gut therapeutische Phagen ihre Ziele infizieren, zu charakterisieren — ein wichtiger Schritt, um diese natürlichen Bakterienfeinde im Kampf gegen antibiotikaresistente Infektionen einzusetzen.
Zitation: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Schlüsselwörter: Bakteriophagen, Mikrofluidische Tropfen, Phagentherapie, Einzelzellinfektion, Antibiotikaresistenz