Clear Sky Science · ja
ドロップレット・マイクロフルイディクスを用いたファージと宿主の動態の定量化
なぜ小さなウイルスとドロップレットが重要なのか
細菌を殺すウイルス、バクテリオファージは、薬剤耐性感染症に対する有望な味方として再評価されています。しかし、それらを信頼できる医薬品にするには、個々のウイルスがどれだけ効率的に細菌に感染し破壊するかを測定する必要があり、従来の実験法ではそれが難しいことが多い。本論文は、単一のウイルスと細菌が繰り広げる何千もの小さな戦いを同時に観察するドロップレット法を紹介し、感染がどれくらい速く、どれくらいの頻度で成功するかを明らかにします。こうした精密な知見は、より良いファージ療法の指針となり、微生物の生態を形作る見えないウイルス世界の理解を深める可能性があります。
伝統的なシャーレ試験の限界
数十年にわたって研究者はプラークアッセイを頼りにしてきました:ウイルスと軟寒天上の細菌層を混ぜ、翌日まで待ち、細菌が消失した明瞭な斑点を数える。これらの斑点は存在した感染性ウイルスの数を推定します。堅牢ではあるものの、この方法は遅く柔軟性に欠け、最終的なスナップショットしか提供しません。感染が時間経過でどのように進むかを追跡できず、感染と再感染の無数のラウンドを混ぜ合わせてしまいます。バルク蛍光やDNAベースの他の手法も大きな集団を平均化してしまうため、単一の感染事象を捉えたり、ウイルスが各細菌に出会う数のような条件を精密に調整したりすることは困難です。
各感染を小さな試験管に変える
著者らは高スループットなプラットフォームを構築し、細菌とファージを油中に懸濁した微小な水滴に封入します。細菌を運ぶ液流とウイルスを含む液流の2つが、ドロップレットが形成される狭い接合部でのみ出会うため、暴露時間は封入時に正確に始まります。各ドロップレットは、定義された体積と制御されたファージ対細菌比を持つ孤立した反応室になります。チームは、細胞が破裂して細菌のDNAが放出された際に強く発光する特別な蛍光色素を加え、ウイルス遺伝物質の存在だけではなく、溶菌が成功したかどうかを直接検出します。
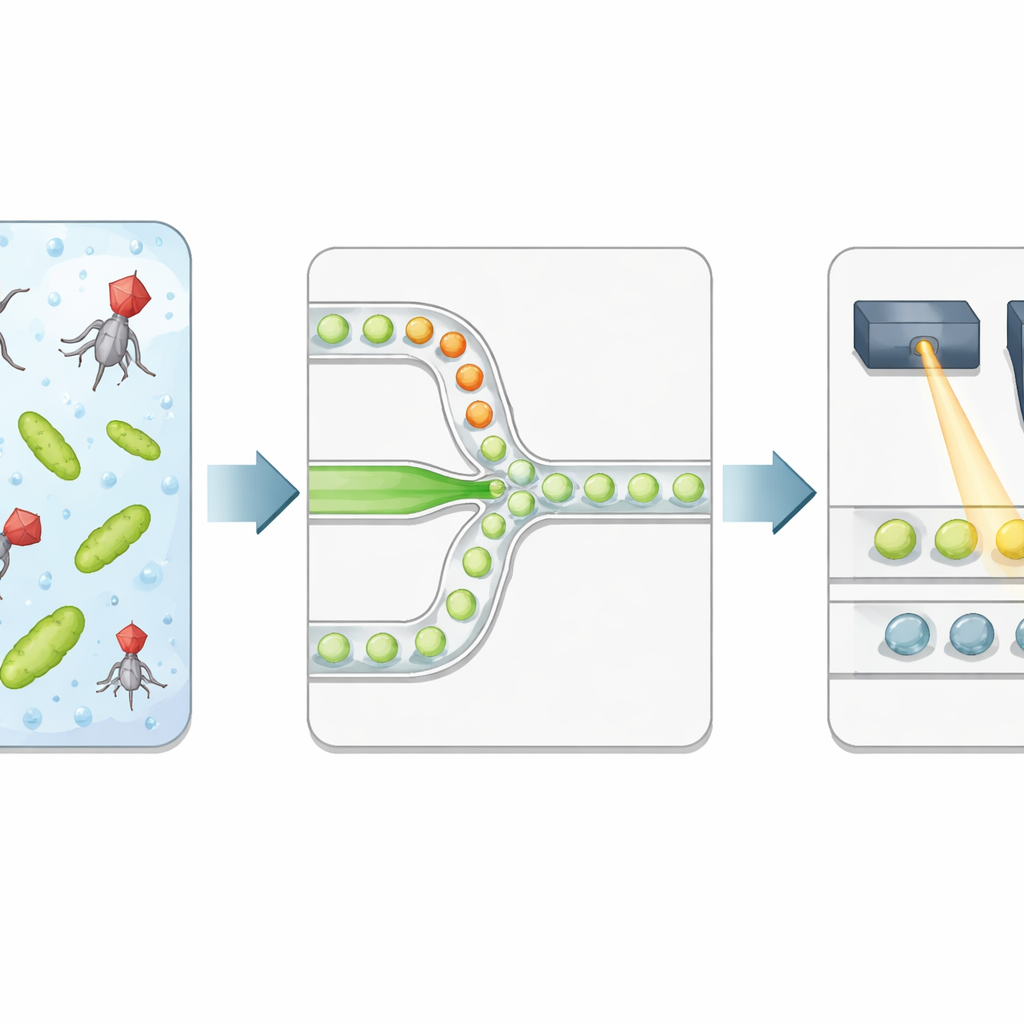
光でドロップレットの結果を読む
制御されたインキュベーションの後、エマルジョンは第2のマイクロフルイディックチップを通して流され、ドロップレットが1つずつ焦点を合わせたレーザーの下に整列します。高速検出器がDNA色素からの緑色蛍光と、ドロップレット製造時に加えられた参照色素からの赤色蛍光を記録します。赤い信号はドロップレットのサイズと各ドロップレットが受け取ったウイルス溶液の量を示し、緑の信号は溶菌が起きたかどうかを報告します。自動化された統計手法により、暗いドロップレット(溶菌なし)と明るいドロップレット(少なくとも1個の細菌が感染し溶菌した)を分離し、実験を0と1のデジタル列に変換します。明るいドロップレットの割合をドロップレットあたりの期待ウイルス数と細菌数に関連付けることで、研究者はウイルス濃度を復元し、従来のプラークカウントと比較します。
条件を調整し隠れた動力学を探る
このプラットフォームは単なるカウント以上のことを行います。ウイルスと細菌の溶液の混合比を意図的に変えることで、チームは単一の実験内で異なるウイルス対宿主比をもつドロップレットのサブ集団を生成します。これによりアッセイが精密な結果を与える濃度レンジが効果的に拡張され、バルク光学測定で見えているすべての細菌が実際に感染可能であるわけではないことさえ明らかになります。著者らはまた、ドロップレットサイズとインキュベーション時間を変えて、溶菌したドロップレットの割合がどのように増加するかを観察します。ドロップレット内部でウイルスが細菌に吸着する仕組みを記述する彼らのモデルは、溶菌のタイミングと成功が感染可能な実際の細胞数やウイルス粒子がそれらと衝突する頻度に依存するが、ドロップレットの体積自体には強く依存しないことを示しています。
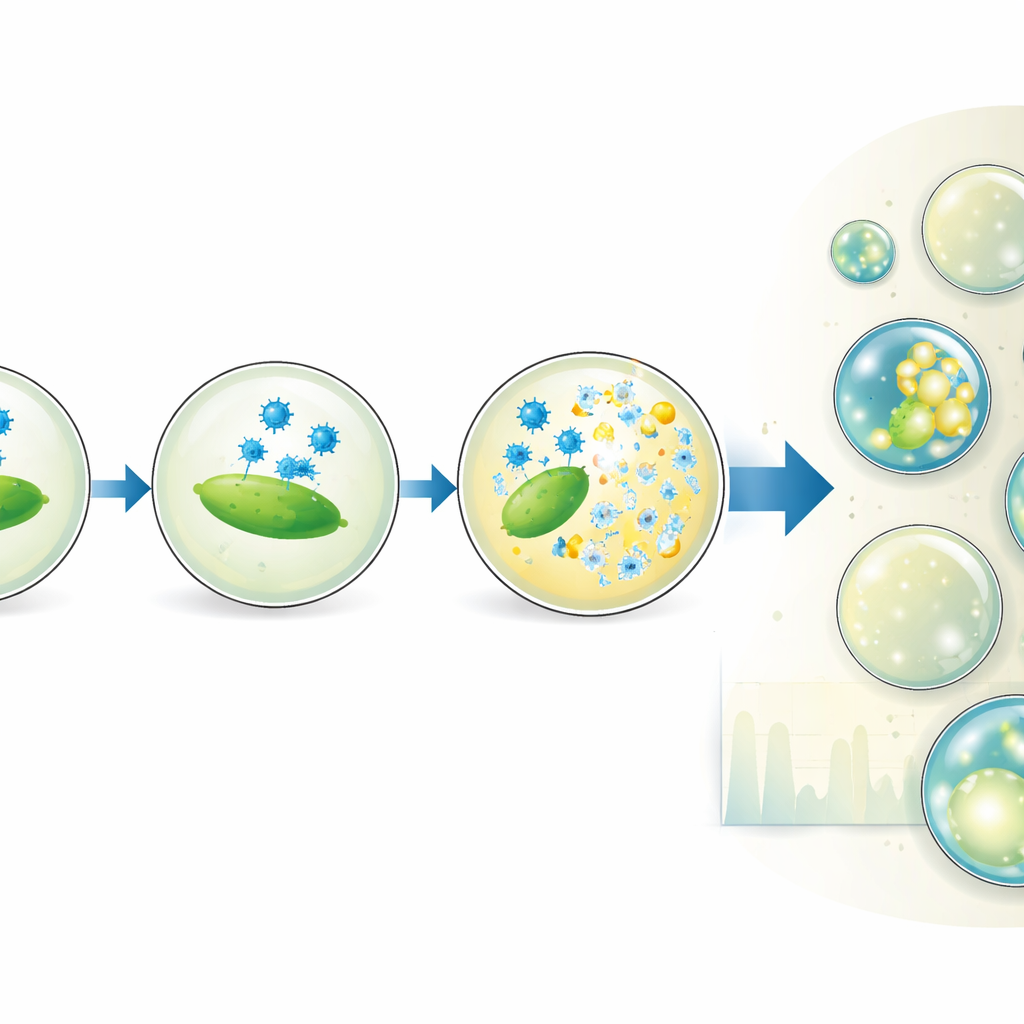
研究ツールから将来の療法へ
個々の感染事象を孤立化してデジタル化することで、このドロップレット法は従来のプラークアッセイとよく一致する正確なウイルスカウントを提供すると同時に、時間分解能のある情報と実験条件の精密な制御を付加します。多くの溶菌性ファージ–細菌ペアに適用でき、数百万個のドロップレットへスケールアップ可能であるため、ファージ変異体、培地、温度のハイスループットスクリーニングへの道を開きます。実務的には、この研究は治療用ファージが標的にどれほどよく感染するかを特徴付ける強力な新手法を提供し、これらの天然の細菌捕食者を用いて抗生物質耐性感染症と戦うための重要な一歩となります。
引用: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
キーワード: バクテリオファージ, マイクロフルイディック・ドロップレット, ファージ療法, 単一細胞感染, 抗生物質耐性