Clear Sky Science · es
Cuantificación de la dinámica fag-huésped mediante microfluidos en gotas
Por qué nos importan los virus y las gotas diminutas
Los virus que matan bacterias, llamados bacteriófagos, vuelven a considerarse aliados potenciales frente a infecciones resistentes a los fármacos. Pero para transformarlos en medicinas fiables, los científicos deben medir con precisión cuán eficientemente infectan y destruyen bacterias los virus individuales, algo que los métodos clásicos de laboratorio dificultan. Este trabajo presenta un enfoque basado en gotas que observa miles de pequeñas batallas entre virus individuales y bacterias a la vez, revelando con qué rapidez y con qué frecuencia tienen éxito las infecciones. Estos conocimientos precisos podrían guiar mejores terapias con fagos y profundizar nuestra comprensión del mundo viral oculto que moldea la vida microbiana en la Tierra.
Límites de las pruebas tradicionales en placas
Durante décadas, los investigadores han recurrido a ensayos de placas: mezclar virus con un tapiz de bacterias en agar blando, esperar una noche y contar las zonas claras donde las bacterias han sido eliminadas. Esos puntos estiman cuántos virus infecciosos había. Aunque robusto, este método es lento, poco flexible y ofrece solo una instantánea final. No puede seguir cómo se desarrollan las infecciones a lo largo del tiempo y mezcla numerosas rondas de infección y reinfección. Otros enfoques, como la fluorescencia a granel o las pruebas basadas en ADN, siguen promediando sobre grandes poblaciones, lo que dificulta ver eventos de infección individuales o ajustar condiciones como cuántos virus encuentra cada bacteria.
Convertir cada infección en un pequeño tubo de ensayo
Los autores construyen una plataforma de alto rendimiento que empaqueta bacterias y fagos en gotas microscópicas de agua suspendidas en aceite. Dos corrientes líquidas separadas —una que transporta bacterias y otra virus— se encuentran solo en la estrecha unión donde se generan las gotas, de modo que el tiempo de exposición comienza de forma precisa al encapsularse. Cada gota se convierte en una cámara de reacción aislada con un volumen bien definido y una relación controlada de fagos por bacteria. El equipo añade un tinte fluorescente especial que se ilumina fuertemente cuando el ADN bacteriano se libera tras la lisis celular, sirviendo como una señal directa de lisis exitosa en lugar de solo la presencia de material genético viral.
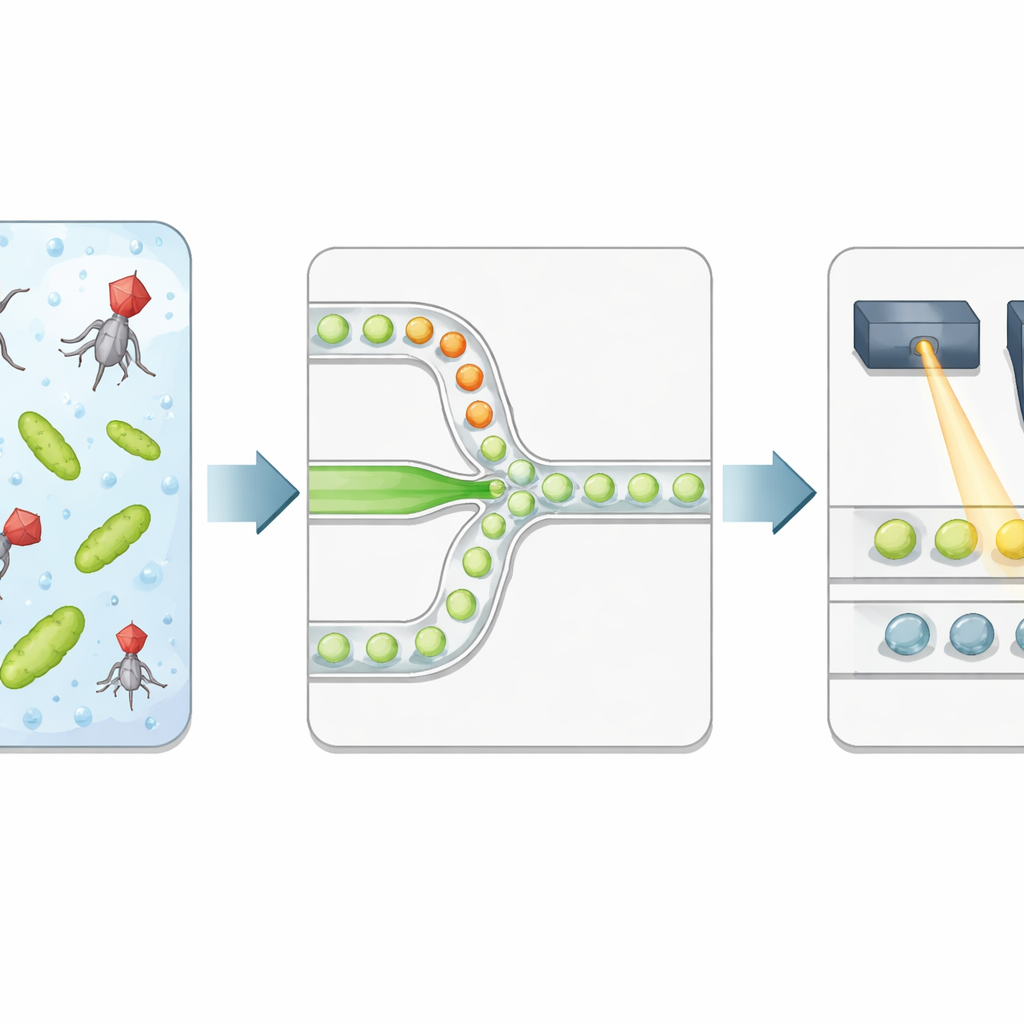
Leer los resultados de las gotas con luz
Tras una incubación controlada, la emulsión se hace pasar por un segundo chip microfluídico que alinea las gotas una por una bajo un láser enfocado. Un detector rápido registra la fluorescencia verde del tinte de ADN y la fluorescencia roja de un tinte de referencia incluido durante la producción de las gotas. La señal roja informa del tamaño de la gota y de cuánto de la solución viral recibió cada gota, mientras que la señal verde indica si se produjo lisis. Un método estadístico automatizado separa las gotas tenues (sin lisis) de las brillantes (al menos una bacteria infectada y lisada), convirtiendo el experimento en una cadena digital de 0s y 1s. Relacionando la fracción de gotas brillantes con los números esperados de virus y bacterias por gota, los investigadores recuperan la concentración viral y la comparan con los recuentos clásicos de placas.
Ajustar condiciones y sondear cinéticas ocultas
La plataforma va más allá del simple recuento. Al cambiar deliberadamente la proporción de mezcla de las soluciones de virus y bacterias, el equipo genera subpoblaciones de gotas con diferentes razones virus:huésped, todo dentro de un mismo experimento. Esto amplía efectivamente el rango de concentraciones en el que el ensayo ofrece resultados precisos e incluso revela que no todas las bacterias detectadas por mediciones ópticas a granel son realmente infectables. Los autores también varían el tamaño de las gotas y el tiempo de incubación para observar cómo crece la proporción de gotas lisadas. Su modelo de cómo los virus se adsorben a las bacterias dentro de las gotas muestra que el momento y el éxito de la lisis dependen del número real de células capaces de ser infectadas y de la frecuencia de colisiones de partículas virales con ellas, pero no dependen de forma fuerte del volumen de la gota en sí.
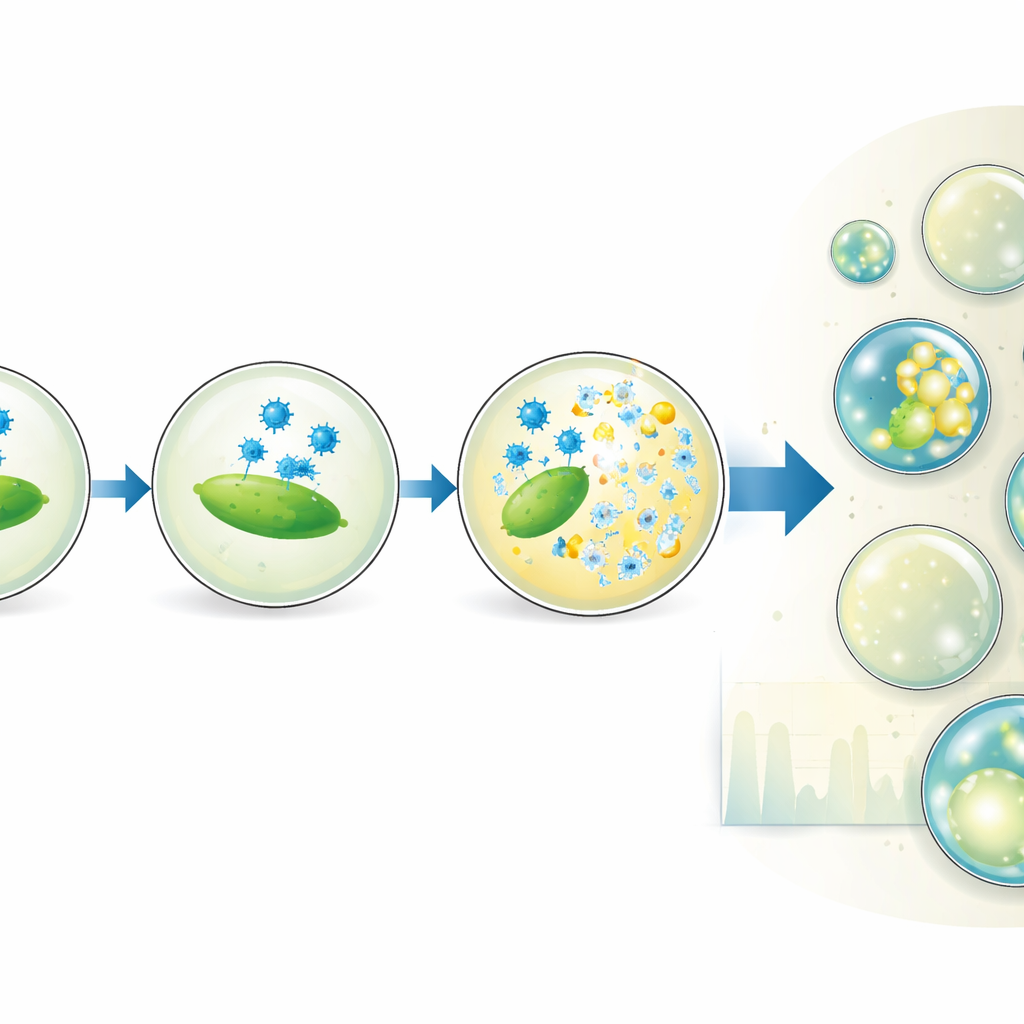
Del instrumento de laboratorio a futuras terapias
Al aislar y digitalizar eventos de infección individuales, este método en gotas ofrece recuentos virales precisos que coinciden estrechamente con los ensayos de placas tradicionales, a la vez que añade información con resolución temporal y un control fino de las condiciones experimentales. Puede aplicarse a muchos pares fag–bacteria líticos diferentes y escalarse a millones de gotas, abriendo la puerta al cribado de alto rendimiento de variantes de fagos, medios o temperaturas. En términos prácticos, el trabajo proporciona una nueva forma potente de caracterizar cuán bien los fagos terapéuticos infectan sus objetivos, un paso importante hacia el uso de estos depredadores bacterianos naturales para ayudar a combatir las infecciones resistentes a los antibióticos.
Cita: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Palabras clave: bacteriófagos, gotas microfluídicas, terapia con fagos, infección a nivel unicelular, resistencia a antibióticos